SES School, Studie en Onderwijs
Wiskunde in de brugklas, Frans voor het examen of een studie Personeel en Arbeid? Moeilijke formulieren van DUO? Iets weten over studiefinanciering of studentenverenigingen? Dit is het forum voor leerkrachten, scholieren en studenten, van brugklas tot uni



Vorige deel: [Bèta overig] 'Huiswerk- en vragentopic'.
Post hier weer al je vragen, passies, trauma's en andere dingen die je uit je slaap houden met betrekking tot de vakken:
• Natuurkunde
• Informatica
• Scheikunde
• Biologie
• Algemene Natuurwetenschappen
• ... en alles wat verder in de richting komt.
Van MBO tot WO, hier is het topic waar je een antwoord kunt krijgen op je vragen.
Opmaak: http://betahw.mine.nu/index.php: site van GlowMouse om formules te kunnen gebruiken in je posts (op basis van Latexcode wordt een plaatje gegenereerd dat je vervolgens via het aangegeven linkje kunt opnemen).
Post hier weer al je vragen, passies, trauma's en andere dingen die je uit je slaap houden met betrekking tot de vakken:
• Natuurkunde
• Informatica
• Scheikunde
• Biologie
• Algemene Natuurwetenschappen
• ... en alles wat verder in de richting komt.
Van MBO tot WO, hier is het topic waar je een antwoord kunt krijgen op je vragen.
Opmaak: http://betahw.mine.nu/index.php: site van GlowMouse om formules te kunnen gebruiken in je posts (op basis van Latexcode wordt een plaatje gegenereerd dat je vervolgens via het aangegeven linkje kunt opnemen).


Iemand verstand van Electronica?
Parallel schakeling Weerstand Spoel Condensator (RLC) en dan frequentie bepalen zodat er resonantie optreedt.
R=100ohm
L=2H
C=10uF
In serie snap ik (resonantie is daar XL=XC) het maar parallel is nog vaag.
Parallel schakeling Weerstand Spoel Condensator (RLC) en dan frequentie bepalen zodat er resonantie optreedt.
R=100ohm
L=2H
C=10uF
In serie snap ik (resonantie is daar XL=XC) het maar parallel is nog vaag.
Blues ain't nothing but a good man feeling bad...


Als de volumeknop harder wordt gezet tot het geluid 30 dB is toegenomen,
hoeveel maal hoger is dan de geluidsintensiteit geworden?
Voor elke verdubbeling in intensiteit krijg je toch een verhoging van 3dB? Dan is de intensiteit toch met 2^10 = 1024. Met een factor 1024 toegenomen?
Antwoordmodel van dit tentamen geeft dit antwoord namelijk niet als optie.
hoeveel maal hoger is dan de geluidsintensiteit geworden?
Voor elke verdubbeling in intensiteit krijg je toch een verhoging van 3dB? Dan is de intensiteit toch met 2^10 = 1024. Met een factor 1024 toegenomen?
Antwoordmodel van dit tentamen geeft dit antwoord namelijk niet als optie.


Die 3dB is een benadering, het is niet precies 3dBquote:Op donderdag 14 april 2011 20:47 schreef Physics het volgende:
Als de volumeknop harder wordt gezet tot het geluid 30 dB is toegenomen,
hoeveel maal hoger is dan de geluidsintensiteit geworden?
Voor elke verdubbeling in intensiteit krijg je toch een verhoging van 3dB? Dan is de intensiteit toch met 2^10 = 1024. Met een factor 1024 toegenomen?
Antwoordmodel van dit tentamen geeft dit antwoord namelijk niet als optie.
The biggest argument against democracy is a five minute discussion with the average voter.


Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Goede link opzich, staan alleen een paar foutjes in de tabel, bij 30 dB (ook bij 40 dB) zijn de waardes in zowel de eerste als de tweede kolom een factor tien te laagquote:Op vrijdag 15 april 2011 04:09 schreef Lyrebird het volgende:
http://www.natuurkunde.nl/artikelen/view.do?supportId=398485
The biggest argument against democracy is a five minute discussion with the average voter.


Klopt - iets te aggressief met de nullen.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Ik heb een aantal vragen m.b.t. natuurkunde (5havo).
In mijn lesboek natuurkunde stond volgens mij een fout over een brekingsindex. Er stond namelijk dat nlucht->water = nlucht/nwater. Maar dit hoort toch: nlucht->water = nwater/nlucht te zijn?
Verder heb ik nog een vraag over verval (straling). Er zijn isotopen van stoffen die via meerdere soorten straling vervallen. Een voorbeeld hiervan is O-19. Dit vervalt via ß- straling en γ straling. Maar moet je in de vervalreactie dan allebei deze stralingen zetten, of twee vervalvergelijken waarbij in de één bèta min straling voorkomt, en in de ander gammastraling? Want bij veel isotopen staan er meerdere soorten stralingen waarin het vervalt, en aangezien dit op het CSE gaat komen, wil ik dit goed snappen.
Bij voorbaat dank
[ Bericht 0% gewijzigd door #ANONIEM op 03-05-2011 17:28:22 ]
In mijn lesboek natuurkunde stond volgens mij een fout over een brekingsindex. Er stond namelijk dat nlucht->water = nlucht/nwater. Maar dit hoort toch: nlucht->water = nwater/nlucht te zijn?
Verder heb ik nog een vraag over verval (straling). Er zijn isotopen van stoffen die via meerdere soorten straling vervallen. Een voorbeeld hiervan is O-19. Dit vervalt via ß- straling en γ straling. Maar moet je in de vervalreactie dan allebei deze stralingen zetten, of twee vervalvergelijken waarbij in de één bèta min straling voorkomt, en in de ander gammastraling? Want bij veel isotopen staan er meerdere soorten stralingen waarin het vervalt, en aangezien dit op het CSE gaat komen, wil ik dit goed snappen.
Bij voorbaat dank
[ Bericht 0% gewijzigd door #ANONIEM op 03-05-2011 17:28:22 ]


Bedoel je met nlucht de geluids- of lichtsnelheid in lucht? In dat geval lijkt mij dat het gewoon klopt wat in het boek staat, als je van medium 1 naar medium 2 gaat, geldt n=c1/c2 (met c de geluidssnelheid in het betreffende medium).quote:Op dinsdag 3 mei 2011 17:09 schreef Mark94 het volgende:
Ik heb een aantal vragen m.b.t. natuurkunde (5havo).
In mijn lesboek natuurkunde stond volgens mij een fout over een brekingsindex. Er stond namelijk dat nlucht->water = nlucht/nwater. Maar dit hoort toch: nlucht->water = nwater/nlucht te zijn?
Staat er niets in de vraag welke straling er vrijkomt? Ik dacht dat dat er bij ons altijd bij stond namelijk, als het er niet bij staat zou ik het zo ook niet direct weten.quote:Verder heb ik nog een vraag over verval (straling). Er zijn isotopen van stoffen die via meerdere soorten straling vervallen. Een voorbeeld hiervan is O-19. Dit vervalt via ß- straling en γ straling. Maar moet je in de vervalreactie dan allebei deze stralingen zetten, of twee vervalvergelijken waarbij in de één bèta min straling voorkomt, en in de ander gammastraling? Want bij veel isotopen staan er meerdere soorten stralingen waarin het vervalt, en aangezien dit op het CSE gaat komen, wil ik dit goed snappen.
Bij voorbaat dank
The biggest argument against democracy is a five minute discussion with the average voter.


In je vervalreactie zet je alleen deeltjes met massa en/of lading, gamma straling heeft dit beide niet en hoef je dus nooit in de vergelijking te zetten. In dit geval krijg je dus 19/8 O -> 0/-1 e + 19/9 Fquote:Op dinsdag 3 mei 2011 17:09 schreef Mark94 het volgende:
Verder heb ik nog een vraag over verval (straling). Er zijn isotopen van stoffen die via meerdere soorten straling vervallen. Een voorbeeld hiervan is O-19. Dit vervalt via ß- straling en γ straling. Maar moet je in de vervalreactie dan allebei deze stralingen zetten, of twee vervalvergelijken waarbij in de één bèta min straling voorkomt, en in de ander gammastraling? Want bij veel isotopen staan er meerdere soorten stralingen waarin het vervalt, en aangezien dit op het CSE gaat komen, wil ik dit goed snappen.
Bij voorbaat dank


Oh lichtsnelheid. Maar als licht via lucht naar een andere stof gaat, breekt hij naar de normaal toe. Dan zou de brekingsindex groter dan 1 moeten zijn. Want de brekingsindex van lucht is ongeveer 1 en die van water is ongeveer 1,3. Dus als het nlucht->water = nlucht/nwater zou zijn dan zou er 1/1,3 = 0.8 uit komen. En dat is kleiner dan 1, dus klopt toch niet? Daarom hoort het toch nlucht->water = nwater/nlucht te zijn?quote:Op dinsdag 3 mei 2011 18:06 schreef M.rak het volgende:
[..]
Bedoel je met nlucht de geluids- of lichtsnelheid in lucht? In dat geval lijkt mij dat het gewoon klopt wat in het boek staat, als je van medium 1 naar medium 2 gaat, geldt n=c1/c2 (met c de geluidssnelheid in het betreffende medium).
[..]
Staat er niets in de vraag welke straling er vrijkomt? Ik dacht dat dat er bij ons altijd bij stond namelijk, als het er niet bij staat zou ik het zo ook niet direct weten.
[..]
Nee het gaat zeg maar over een bepaalde isotoop (bijvoorbeeld O-19 of Ba-140) en dan moet je in je BINAS (informatieboek met onder andere gegevens van stoffen) opzoeken via welke straling het vervalt en daar moet je bijvoorbeeld de vervalreactie van opschrijven.
[ Bericht 6% gewijzigd door #ANONIEM op 04-05-2011 18:55:50 ]


Ja maar wat nou als je een isotoop krijgt, bijvoorbeeld Po-216. Die vervalt via alfa- en bètastraling. Die hebben allebei massa en lading, dus hoe zit het dan?quote:Op dinsdag 3 mei 2011 21:48 schreef bert_van_dirkjan het volgende:
[..]
In je vervalreactie zet je alleen deeltjes met massa en/of lading, gamma straling heeft dit beide niet en hoef je dus nooit in de vergelijking te zetten. In dit geval krijg je dus 19/8 O -> 0/-1 e + 19/9 F
[ Bericht 0% gewijzigd door #ANONIEM op 04-05-2011 18:55:13 ]


De brekingsindex geeft de verhouding tussen de lichtsnelheid in een vacuüm en in een medium, er is dus niet zoiets als nlucht -> water. Wat jij bedoelt is denk ik gewoon de wet van Snellius, n1*sin(B1)=n2*sin(B2)?quote:Op woensdag 4 mei 2011 18:50 schreef Mark94 het volgende:
[..]
Oh lichtsnelheid. Maar als licht via lucht naar een andere stof gaat, breekt hij naar de normaal toe. Dan zou de brekingsindex groter dan 1 moeten zijn. Want de brekingsindex van lucht is ongeveer 1 en die van water is ongeveer 1,3. Dus als het nlucht->water = nlucht/nwater zou zijn dan zou er 1/1,3 = 0.77 uit komen. En dat is kleiner dan 1, dus klopt toch niet? Daarom hoort het toch nlucht->water = nwater/nlucht te zijn?
The biggest argument against democracy is a five minute discussion with the average voter.


Aah, ze hebben hier de verhouding van de brekingsindices ook weer brekingsindex genoemd. De definitie van brekingsindex (van één enkel medium, dus niet van het ene naar het andere medium) is, zoals ik net al zei, de verhouding tussen de lichtsnelheid in vacuüm en de lichtsnelheid in het medium. De wet van Snellius zegt nuquote:Op woensdag 4 mei 2011 19:05 schreef Mark94 het volgende:
Hier dit bedoel ik:
http://www.natuurkunde.nl/artikelen/view.do?supportId=73
dit kunnen we ook schrijven als
Die laatste term,
The biggest argument against democracy is a five minute discussion with the average voter.


Geen idee waar ik dit moet plaatsen. Maar het heeft met school te maken.
Wat betekend de volgende zin precies:
The Earth is mean so I plot mad schemes
Gr.
Wat betekend de volgende zin precies:
The Earth is mean so I plot mad schemes
Gr.
Op maandag 20 januari 2014 14:20 schreef BozeHaas het volgende:
Ik ken porsche1 alleen als een doorwinterde Braddie-basher eigenlijks.
Ik ken porsche1 alleen als een doorwinterde Braddie-basher eigenlijks.


Het alfa-huiswerktopic is gesloten, omdat daarvoor geen belangstelling was. Misschien is het een beter idee om het in TTK te proberen?quote:Op donderdag 5 mei 2011 00:33 schreef porsche1 het volgende:
Geen idee waar ik dit moet plaatsen. Maar het heeft met school te maken.
Wat betekend de volgende zin precies:
The Earth is mean so I plot mad schemes
Gr.


Dankje.quote:Op donderdag 5 mei 2011 00:56 schreef lyolyrc het volgende:
[..]
Het alfa-huiswerktopic is gesloten, omdat daarvoor geen belangstelling was. Misschien is het een beter idee om het in TTK te proberen?
Op maandag 20 januari 2014 14:20 schreef BozeHaas het volgende:
Ik ken porsche1 alleen als een doorwinterde Braddie-basher eigenlijks.
Ik ken porsche1 alleen als een doorwinterde Braddie-basher eigenlijks.


ik heb ook een vraagje:
bij de zuur-base constanten (Kz en Kb) staat de ene keer de linker kant van de reactievergelijking bovenaan, en de andere keer staat de rechterkant van de reactievergelijking bovenaan (wat normaal is imo) wat bepaalt wat noemer en wat teller is?
bij de zuur-base constanten (Kz en Kb) staat de ene keer de linker kant van de reactievergelijking bovenaan, en de andere keer staat de rechterkant van de reactievergelijking bovenaan (wat normaal is imo) wat bepaalt wat noemer en wat teller is?


Mocht een dergelijk isotoop in de vraag staan, dan zal in de tekst wel duidelijk zijn om welk verval het gaat. Een enkel atoom kan in ieder geval niet tegelijk beta en alfa vervallen, dus er zijn twee verschillende verval reacties (1 voor alfa verval en 1 voor beta verval) en niet een of andere reactie met de twee gecombineerd.quote:Op woensdag 4 mei 2011 18:53 schreef Mark94 het volgende:
[..]
Ja maar wat nou als je een isotoop krijgt, bijvoorbeeld Po-216. Die vervalt via alfa- en bètastraling. Die hebben allebei massa en lading, dus hoe zit het dan?
Stel dat gevraagd wordt geef de vervalreactie(s) van Po-216 dan krijg je dus:
216/84 Po -> 212/82 Pb + 4/2 He voor alfa verval en 216/84 Po -> 216/85 At + 0/-1 e voor beta verval
Ga ze niet tegelijk gebruiken door zoiets te doen: 216/84 Po -> 4/2 He + 0/-1 e + 212/83 Bi


Ik snap je vraag niet helemaal, maar als je bedoelt wat ik denk..... De concentraties van H3O+ of OH- staan altijd bovenaan (teller) vermenigvuldigd met de concentratie(s) van wat nog meer aan die kant van de evenwichtsreactie staat.quote:Op donderdag 5 mei 2011 22:36 schreef kevintjuhh2 het volgende:
ik heb ook een vraagje:
bij de zuur-base constanten (Kz en Kb) staat de ene keer de linker kant van de reactievergelijking bovenaan, en de andere keer staat de rechterkant van de reactievergelijking bovenaan (wat normaal is imo) wat bepaalt wat noemer en wat teller is?
Bijvoorbeeld als je de Ph wil berekenen van een oplossing van 1 mol HCN in een liter water
De evenwichtsreactie: HCN + H2O <--> CN- + H3O+
Het gaat om een zuur dus zoek de Kz op : Kz=6,1 * 10^-10
Oftewel: [H3O+] x [CN-] / [HCN] = 6,1 * 10^-10
Je begint met 1 M HCN, maar een gedeelte x zal overgaan tot H3O+ + CN -, je hebt nu dus [H3O+]=x, [CN-]=x en [HCN]= 1-x (de 1 komt van de 1 M).
De vergelijking wordt dus: x^2/(1-x) = 6,1 * 10^-10, als je ziet dat x heel klein wordt mag je de -x weglaten en krijg je dus x^2= 6,1 * 10^-10 -> x = 2,5 * 10^-5 = [H3O+] --> pH = -log[x]
Volgens mij geldt in het algemeen dat wat rechts van de evenwichtsreactie staat is de teller en links de noemer


Bedankt! Dan doe ik dat tenminste niet fout.quote:Op zondag 8 mei 2011 02:24 schreef bert_van_dirkjan het volgende:
[..]
Mocht een dergelijk isotoop in de vraag staan, dan zal in de tekst wel duidelijk zijn om welk verval het gaat. Een enkel atoom kan in ieder geval niet tegelijk beta en alfa vervallen, dus er zijn twee verschillende verval reacties (1 voor alfa verval en 1 voor beta verval) en niet een of andere reactie met de twee gecombineerd.
Stel dat gevraagd wordt geef de vervalreactie(s) van Po-216 dan krijg je dus:
216/84 Po -> 212/82 Pb + 4/2 He voor alfa verval en 216/84 Po -> 216/85 At + 0/-1 e voor beta verval
Ga ze niet tegelijk gebruiken door zoiets te doen: 216/84 Po -> 4/2 He + 0/-1 e + 212/83 Bi


jah ik ben laatst een paar keer tegengekomen dat rechts onder en links boven stond, dat snapte ik niet ( en nog steeds niet) maar zullen wel fouten in antwoordmodellen zijn ofzo:Squote:Op zondag 8 mei 2011 03:00 schreef bert_van_dirkjan het volgende:
[..]
Ik snap je vraag niet helemaal, maar als je bedoelt wat ik denk..... De concentraties van H3O+ of OH- staan altijd bovenaan (teller) vermenigvuldigd met de concentratie(s) van wat nog meer aan die kant van de evenwichtsreactie staat.
Bijvoorbeeld als je de Ph wil berekenen van een oplossing van 1 mol HCN in een liter water
De evenwichtsreactie: HCN + H2O <--> CN- + H3O+
Het gaat om een zuur dus zoek de Kz op : Kz=6,1 * 10^-10
Oftewel: [H3O+] x [CN-] / [HCN] = 6,1 * 10^-10
Je begint met 1 M HCN, maar een gedeelte x zal overgaan tot H3O+ + CN -, je hebt nu dus [H3O+]=x, [CN-]=x en [HCN]= 1-x (de 1 komt van de 1 M).
De vergelijking wordt dus: x^2/(1-x) = 6,1 * 10^-10, als je ziet dat x heel klein wordt mag je de -x weglaten en krijg je dus x^2= 6,1 * 10^-10 -> x = 2,5 * 10^-5 = [H3O+] --> pH = -log[x]
Volgens mij geldt in het algemeen dat wat rechts van de evenwichtsreactie staat is de teller en links de noemer


Fouten kunnen natuurlijk altijd voorkomen. Hou er wel rekening mee dat teller en noemer op basis van rekenregels verwisseld kunnen worden wanneer je bezig bent met de uitdrukking voor pKz.quote:Op zondag 8 mei 2011 21:46 schreef kevintjuhh2 het volgende:
[..]
jah ik ben laatst een paar keer tegengekomen dat rechts onder en links boven stond, dat snapte ik niet ( en nog steeds niet) maar zullen wel fouten in antwoordmodellen zijn ofzo:S
Om even door te gaan op het voorbeeld van bert_van_dirkjan:
HCN +H2O <-> CN- + H3O+
Kz = [CN-][H3O+]/[HCN]
pKz = -log(Kz) = -log([CN-][H3O+]/[HCN]) = -log([H3O+]) - log([CN-]/[HCN]) = pH - log([CN-]/[HCN]) = pH + log([HCN]/[CN-])
In de laatste uitdrukking zijn teller en noemer verwisseld ten opzichte van de uitdrukking van Kz.


Kunstproductie en lijsten is dat een assortiment groep?
en klopt dit?
Assortiment groep Multimedia
Artikelgroep Foto s
Artikelsoort Canvas
Assortiment groep opname apparatuur
Artikelgroep Foto-apparatuur
Artikelsoort Digitale compact camera s
en klopt dit?
Assortiment groep Multimedia
Artikelgroep Foto s
Artikelsoort Canvas
Assortiment groep opname apparatuur
Artikelgroep Foto-apparatuur
Artikelsoort Digitale compact camera s


Hey, ik heb een klein vraagje over een zuur-base titratie die ik binnenkort moet doen.
Ik moet de stof NaHCO3 (0,3M) titreren. Dan krijg je volgens mij:
HCO3 + H3O <-> CO3 + 2H2O
[HCO3] X [H3O]
_____________ = Kb
[CO3]
Volgens acibbaselabs zou ik nu erg veel moeten titreren, dus wil ik het verdunnen naar 0,1M.
Dan heb je ongeveer 25ml nodig. Nu moet ik het dus 3 keer verdunnen, maar ik ben eigenlijk helemaal vergeten hoe je moet verdunnen. Als ik 6ml water neem en hier 3ml NaHCO3 bijvoeg heb ik dan drie keer verdunt?
Ik moet de stof NaHCO3 (0,3M) titreren. Dan krijg je volgens mij:
HCO3 + H3O <-> CO3 + 2H2O
[HCO3] X [H3O]
_____________ = Kb
[CO3]
Volgens acibbaselabs zou ik nu erg veel moeten titreren, dus wil ik het verdunnen naar 0,1M.
Dan heb je ongeveer 25ml nodig. Nu moet ik het dus 3 keer verdunnen, maar ik ben eigenlijk helemaal vergeten hoe je moet verdunnen. Als ik 6ml water neem en hier 3ml NaHCO3 bijvoeg heb ik dan drie keer verdunt?
Neem het leven niet te serieus, je overleeft het toch niet.


De reactievergelijking die je hebt opgesteld klopt niet, want HCO3, H3O en CO3 bestaan niet. Vermeld altijd ladingen als daarvan sprake is!
De juiste reactievergelijking luidt:
HCO3- + H3O+ <-> H2CO3 + H2O -> 2 H2O + CO2
Bicarbonaat (HCO3-) en het hydroniumion (H3O+) zijn dus in evenwicht met koolzuur (H2CO3) en het reactiewater (H2O). Koolzuur op zijn beurt kan splitsen in water en koolstofdioxide. Deze laatste reactie loopt af, omdat koolstofdioxide wegbubbelt uit het reactiemengsel.
Het heeft hier niet echt zin om een evenwichtsvoorwaarde op te gaan stellen, want je doet er hier verder niets mee.
De verdunning klopt en dat kun je ook narekenen:
3 ml 0,3 M NaHCO3-oplossing bevat:
0,3 M * 3,0 ml = 0,9 mmol NaHCO3
Na verdunnen met 6,0 ml water is de concentratie:
0,9 mmol/9,0 ml = 0,1 M NaHCO3.
De juiste reactievergelijking luidt:
HCO3- + H3O+ <-> H2CO3 + H2O -> 2 H2O + CO2
Bicarbonaat (HCO3-) en het hydroniumion (H3O+) zijn dus in evenwicht met koolzuur (H2CO3) en het reactiewater (H2O). Koolzuur op zijn beurt kan splitsen in water en koolstofdioxide. Deze laatste reactie loopt af, omdat koolstofdioxide wegbubbelt uit het reactiemengsel.
Het heeft hier niet echt zin om een evenwichtsvoorwaarde op te gaan stellen, want je doet er hier verder niets mee.
De verdunning klopt en dat kun je ook narekenen:
3 ml 0,3 M NaHCO3-oplossing bevat:
0,3 M * 3,0 ml = 0,9 mmol NaHCO3
Na verdunnen met 6,0 ml water is de concentratie:
0,9 mmol/9,0 ml = 0,1 M NaHCO3.


Ok bedankt, de evenwichtsvoorwaarde heb ik later wel nodig, want ik moet ook de pH uitrekenen. Nog bedankt voor het corrigeren daarvanquote:Op woensdag 18 mei 2011 19:30 schreef lyolyrc het volgende:
De reactievergelijking die je hebt opgesteld klopt niet, want HCO3, H3O en CO3 bestaan niet. Vermeld altijd ladingen als daarvan sprake is!
De juiste reactievergelijking luidt:
HCO3- + H3O+ <-> H2CO3 + H2O -> 2 H2O + CO2
Bicarbonaat (HCO3-) en het hydroniumion (H3O+) zijn dus in evenwicht met koolzuur (H2CO3) en het reactiewater (H2O). Koolzuur op zijn beurt kan splitsen in water en koolstofdioxide. Deze laatste reactie loopt af, omdat koolstofdioxide wegbubbelt uit het reactiemengsel.
Het heeft hier niet echt zin om een evenwichtsvoorwaarde op te gaan stellen, want je doet er hier verder niets mee.
De verdunning klopt en dat kun je ook narekenen:
3 ml 0,3 M NaHCO3-oplossing bevat:
0,3 M * 3,0 ml = 0,9 mmol NaHCO3
Na verdunnen met 6,0 ml water is de concentratie:
0,9 mmol/9,0 ml = 0,1 M NaHCO3.
Neem het leven niet te serieus, je overleeft het toch niet.


Vraag: Je hebt een zure met een waarde van pH 4.
Je verdunt deze zure 10 keer, welke pH waarde krijg je dan?
Kan iemand de berekening erbij geven? Heb het dringend nodig
Je verdunt deze zure 10 keer, welke pH waarde krijg je dan?
Kan iemand de berekening erbij geven? Heb het dringend nodig
Op zondag 25 september 2011 16:29 schreef Dimens het volgende:
Je bent een voorbeeld voor de meeste onder ons.
Op dinsdag 4 oktober 2011 01:23 schreef Zenato het volgende:
Jij bent 1 van de FOK!kers die aanbeden moet worden
Je bent een voorbeeld voor de meeste onder ons.
Op dinsdag 4 oktober 2011 01:23 schreef Zenato het volgende:
Jij bent 1 van de FOK!kers die aanbeden moet worden


pH=-log([h3O+]), pH=4 komt dus overeen met [H3O+]=10-4. Tien keer verdunnen betekent (neem ik aan) dat de concentratie tien keer kleiner wordt, dus [H3O+] wordt 10-5, dit invullen in de formule van pH levert op pH=5.quote:Op donderdag 19 mei 2011 18:09 schreef FreakyStyley het volgende:
Vraag: Je hebt een zure met een waarde van pH 4.
Je verdunt deze zure 10 keer, welke pH waarde krijg je dan?
Kan iemand de berekening erbij geven? Heb het dringend nodig
Dat is trouwens niet toevallig, dat 10x verdunnen een stap van 1 geeft op de pH-schaal, iedere verandering met een factor tien zal de pH één stap verhogen danwel verlagen.
The biggest argument against democracy is a five minute discussion with the average voter.


Gisteren had ik een gesprek met een medicus. Ik heb met scheikunde altijd geleerd dat water PH-neutraal is, dus 7. Aangezien de zure H+ de base OH- elkaar precies neutraliseren.
De arts beweerde echter dat H2O een PH van minder dan 3 heeft. Dat is bijna net zo zuur als cola. Hij heeft er allicht meer verstand van dan ik, maar ik kan het moeilijk geloven. Wie heeft er gelijk?
(Hij was niet aan het trollen trouwens, de voorafgaande reden was een flesje met (pure) H2O en ernaast een flesje met PH 7, toen vroeg ik welke vloeistof dat was omdat ik dacht dat H2O ook PH 7 is.)
De arts beweerde echter dat H2O een PH van minder dan 3 heeft. Dat is bijna net zo zuur als cola. Hij heeft er allicht meer verstand van dan ik, maar ik kan het moeilijk geloven. Wie heeft er gelijk?
(Hij was niet aan het trollen trouwens, de voorafgaande reden was een flesje met (pure) H2O en ernaast een flesje met PH 7, toen vroeg ik welke vloeistof dat was omdat ik dacht dat H2O ook PH 7 is.)


Voor zover ik weet is de pH van water onder standaardsomstandigheden gewoon gelijk aan 7. Bij gedeutereerd water (D2O) is de pH (of eigenlijk pD) hoger, namelijk 7,4.quote:Op vrijdag 20 mei 2011 22:35 schreef 08gnoT. het volgende:
Gisteren had ik een gesprek met een medicus. Ik heb met scheikunde altijd geleerd dat water PH-neutraal is, dus 7. Aangezien de zure H+ de base OH- elkaar precies neutraliseren.
De arts beweerde echter dat H2O een PH van minder dan 3 heeft. Dat is bijna net zo zuur als cola. Hij heeft er allicht meer verstand van dan ik, maar ik kan het moeilijk geloven. Wie heeft er gelijk?
(Hij was niet aan het trollen trouwens, de voorafgaande reden was een flesje met (pure) H2O en ernaast een flesje met PH 7, toen vroeg ik welke vloeistof dat was omdat ik dacht dat H2O ook PH 7 is.)


Ik geloof dat jij toch echt gelijk hebt, dat is ook de strekking van deze wikipedia-pagina.quote:Op vrijdag 20 mei 2011 22:35 schreef 08gnoT. het volgende:
Gisteren had ik een gesprek met een medicus. Ik heb met scheikunde altijd geleerd dat water PH-neutraal is, dus 7. Aangezien de zure H+ de base OH- elkaar precies neutraliseren.
De arts beweerde echter dat H2O een PH van minder dan 3 heeft. Dat is bijna net zo zuur als cola. Hij heeft er allicht meer verstand van dan ik, maar ik kan het moeilijk geloven. Wie heeft er gelijk?
(Hij was niet aan het trollen trouwens, de voorafgaande reden was een flesje met (pure) H2O en ernaast een flesje met PH 7, toen vroeg ik welke vloeistof dat was omdat ik dacht dat H2O ook PH 7 is.)
The biggest argument against democracy is a five minute discussion with the average voter.


Ja daarom, en hier staat het ook:
http://en.wikipedia.org/wiki/PH
Pure water is said to be neutral, with a pH close to 7.0 at 25 °C
Nou ja raar, hij bracht me wel aan het twijfelen. Dan hoop ik maar dat zijn onderzoeken goed gaan
Edit: Ik herinner me net dat ik een paar PH-strips binnenkrijg volgende week, dan kan ik het mooi zelf testen
http://en.wikipedia.org/wiki/PH
Pure water is said to be neutral, with a pH close to 7.0 at 25 °C
Nou ja raar, hij bracht me wel aan het twijfelen. Dan hoop ik maar dat zijn onderzoeken goed gaan
Edit: Ik herinner me net dat ik een paar PH-strips binnenkrijg volgende week, dan kan ik het mooi zelf testen


Misschien had hij het over spa rood of zo. Frisdrank met prik is behoorlijk zuur en daardoor erg slecht voor je tanden, aldus mijn tandarts.quote:Op zaterdag 21 mei 2011 01:08 schreef 08gnoT. het volgende:
Ja daarom, en hier staat het ook:
http://en.wikipedia.org/wiki/PH
Pure water is said to be neutral, with a pH close to 7.0 at 25 °C
Nou ja raar, hij bracht me wel aan het twijfelen. Dan hoop ik maar dat zijn onderzoeken goed gaan
Edit: Ik herinner me net dat ik een paar PH-strips binnenkrijg volgende week, dan kan ik het mooi zelf testen


Medici hebben doorgaans niet zo veel verstand van scheikunde. Het is inderdaad gewoon 7.quote:Op vrijdag 20 mei 2011 22:35 schreef 08gnoT. het volgende:
Gisteren had ik een gesprek met een medicus. Ik heb met scheikunde altijd geleerd dat water PH-neutraal is, dus 7. Aangezien de zure H+ de base OH- elkaar precies neutraliseren.
De arts beweerde echter dat H2O een PH van minder dan 3 heeft. Dat is bijna net zo zuur als cola. Hij heeft er allicht meer verstand van dan ik, maar ik kan het moeilijk geloven. Wie heeft er gelijk?
(Hij was niet aan het trollen trouwens, de voorafgaande reden was een flesje met (pure) H2O en ernaast een flesje met PH 7, toen vroeg ik welke vloeistof dat was omdat ik dacht dat H2O ook PH 7 is.)


Iemand enig idee hoe je het aantal watts berekent wat je in een staalborstel moet stoppen.
De borstel moet ongeveer 1000 toeren draaien.
is 50-40 kilo zwaar en heeft de radius van ongveer 175mm en is ongveer 800 mm lang
De borstel moet ongeveer 1000 toeren draaien.
is 50-40 kilo zwaar en heeft de radius van ongveer 175mm en is ongveer 800 mm lang
Als ook van de sarcastische opmerkingen


Even een vraagje.
Als je een spijker in het vuur houdt, gaat hij niet branden, hij gaat gloeien, en later smelt hij. (als de temperatuur hoog genoeg is.)
Maar waarom gaat ijzerpoeder dan vonken (verbrandt) als je het bij een vlam houdt?
En nog één: Zou ijzer geschikt zijn om warmte op te wekken? waarom (niet) ?
Graag antwoord!
Als je een spijker in het vuur houdt, gaat hij niet branden, hij gaat gloeien, en later smelt hij. (als de temperatuur hoog genoeg is.)
Maar waarom gaat ijzerpoeder dan vonken (verbrandt) als je het bij een vlam houdt?
En nog één: Zou ijzer geschikt zijn om warmte op te wekken? waarom (niet) ?
Graag antwoord!
Op zondag 25 september 2011 16:29 schreef Dimens het volgende:
Je bent een voorbeeld voor de meeste onder ons.
Op dinsdag 4 oktober 2011 01:23 schreef Zenato het volgende:
Jij bent 1 van de FOK!kers die aanbeden moet worden
Je bent een voorbeeld voor de meeste onder ons.
Op dinsdag 4 oktober 2011 01:23 schreef Zenato het volgende:
Jij bent 1 van de FOK!kers die aanbeden moet worden


Ik heb weer een vraag. Zo'n vraag als deze kwam ik een lange tijd geleden tegen op een toets:
Stel je hebt een beker 1 gevuld met water van 10 graden Celsius die 10 gram weegt en je hebt een beker 2 gevuld met water van -10 graden Celsius die 20 gram weegt. En je moet dan de eindtemperatuur berekenen, hoe ga je dan te werk?
Ik ging toen eerst de formule Q = c x m x ΔT hanteren bij beide bekers. Je krijgt dan Q(beker1) = 4,18 x 10^3 x 0,01 x 10 = 418 Joule. Q(beker2) = 4,18 x 10^3 x 0,02 x -10 = -836 Joule. Dan zou ik dit doen: Qtotaal = Q(beker2) - Q(beker1) = -836 - 418 = -1254 Joule. Dan Q = c x m x ΔT ombouwen tot ΔT = Q / c x m. Dan zou ik ΔT = -1254 / ((2 x 4,18 x 10^3) x 0,03) = -5 graden Celsius krijgen. Klopt dit?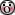
Snel antwoord graag!
[ Bericht 4% gewijzigd door #ANONIEM op 25-05-2011 14:04:42 ]
Stel je hebt een beker 1 gevuld met water van 10 graden Celsius die 10 gram weegt en je hebt een beker 2 gevuld met water van -10 graden Celsius die 20 gram weegt. En je moet dan de eindtemperatuur berekenen, hoe ga je dan te werk?
Ik ging toen eerst de formule Q = c x m x ΔT hanteren bij beide bekers. Je krijgt dan Q(beker1) = 4,18 x 10^3 x 0,01 x 10 = 418 Joule. Q(beker2) = 4,18 x 10^3 x 0,02 x -10 = -836 Joule. Dan zou ik dit doen: Qtotaal = Q(beker2) - Q(beker1) = -836 - 418 = -1254 Joule. Dan Q = c x m x ΔT ombouwen tot ΔT = Q / c x m. Dan zou ik ΔT = -1254 / ((2 x 4,18 x 10^3) x 0,03) = -5 graden Celsius krijgen. Klopt dit?
Snel antwoord graag!
[ Bericht 4% gewijzigd door #ANONIEM op 25-05-2011 14:04:42 ]


Nee, het antwoord klopt niet.quote:Op woensdag 25 mei 2011 13:46 schreef Mark94 het volgende:
Ik heb weer een vraag. Zo'n vraag als deze kwam ik een lange tijd geleden tegen op een toets:
Stel je hebt een beker 1 gevuld met water van 10 graden Celsius die 10 gram weegt en je hebt een beker 2 gevuld met water van -10 graden Celsius die 20 gram weegt. En je moet dan de eindtemperatuur berekenen, hoe ga je dan te werk?
Ik ging toen eerst de formule Q = c x m x ΔT hanteren bij beide bekers. Je krijgt dan Q(beker1) = 4,18 x 10^3 x 0,01 x 10 = 418 Joule. Q(beker2) = 4,18 x 10^3 x 0,02 x -10 = -836 Joule. Dan zou ik dit doen: Qtotaal = Q(beker2) - Q(beker1) = -836 - 418 = -1254 Joule. Dan Q = c x m x ΔT ombouwen tot ΔT = Q / c x m. Dan zou ik ΔT = -1254 / ((2 x 4,18 x 10^3) x 0,03) = -5 graden Celsius krijgen. Klopt dit?
Snel antwoord graag!
Er geldt: Q1 + Q2 = 0
Dus: c*m1*ΔT1 + c*m2*ΔT2 = 0
c*(m1*ΔT1 + m2*ΔT2) = 0
c*(m1*(T1e - T1b) + m2*(T2e - T2b)) = 0
m1*(T1e - T1b) + m2*(T2e - T2b) = 0
T1e = T2e = Te
m1*(Te - T1b) + m2*(Te - T2b) = 0
Te = (m1* T1b + m2*T2b)/(m1+m2)
Invullen geeft Te = -3,33 °C


Aha. Ziet er wel een stuk ingewikkelder uit.quote:Op woensdag 25 mei 2011 14:27 schreef lyolyrc het volgende:
[..]
Nee, het antwoord klopt niet.
Er geldt: Q1 + Q2 = 0
Dus: c*m1*ΔT1 + c*m2*ΔT2 = 0
c*(m1*ΔT1 + m2*ΔT2) = 0
c*(m1*(T1e - T1b) + m2*(T2e - T2b)) = 0
m1*(T1e - T1b) + m2*(T2e - T2b) = 0
T1e = T2e = Te
m1*(Te - T1b) + m2*(Te - T2b) = 0
Te = (m1* T1b + m2*T2b)/(m1+m2)
Invullen geeft Te = -3,33 °C
[ Bericht 1% gewijzigd door #ANONIEM op 25-05-2011 15:13:34 ]


Geldt dat Q1 + Q2 = 0 alleen omdat ze allebei dezelfde soortelijke warmte hebben en gelijke tegengestelde temperaturen? Want de gewichten zijn wel verschillend.
[ Bericht 4% gewijzigd door #ANONIEM op 25-05-2011 15:15:54 ]
[ Bericht 4% gewijzigd door #ANONIEM op 25-05-2011 15:15:54 ]


Wet van behoud van energie.quote:Op woensdag 25 mei 2011 15:15 schreef Mark94 het volgende:
Geldt dat Q1 + Q2 = 0 alleen omdat ze allebei dezelfde soortelijke warmte hebben en gelijke tegengestelde temperaturen? Want de gewichten zijn wel verschillend.


Door te stellen Q1 + Q2 = 0 veronderstel je feitelijk dat er geen warmte verloren gaat. De energie van het warme water komt alleen ten goede van het koude water. Dat heet dan 'behoud van energie'.
De temperaturen zijn overigens niet tegengesteld. Celsius heeft ooit gekozen om het nulpunt van zijn temperatuurschaal te leggen bij het vriespunt van water. Er bestaat echter ook de temperatuurschaal van Kelvin die geen negatieve waardes kent.
De temperaturen zijn overigens niet tegengesteld. Celsius heeft ooit gekozen om het nulpunt van zijn temperatuurschaal te leggen bij het vriespunt van water. Er bestaat echter ook de temperatuurschaal van Kelvin die geen negatieve waardes kent.


Oja, want 0 graden Celsius is gelijk aan 273 Kelvin. Dus -10 graden Celsius zou dan gelijk aan 263 Kelvin zijn, en is inderdaad niet tegengesteld.quote:Op woensdag 25 mei 2011 19:17 schreef lyolyrc het volgende:
Door te stellen Q1 + Q2 = 0 veronderstel je feitelijk dat er geen warmte verloren gaat. De energie van het warme water komt alleen ten goede van het koude water. Dat heet dan 'behoud van energie'.
De temperaturen zijn overigens niet tegengesteld. Celsius heeft ooit gekozen om het nulpunt van zijn temperatuurschaal te leggen bij het vriespunt van water. Er bestaat echter ook de temperatuurschaal van Kelvin die geen negatieve waardes kent.
[ Bericht 1% gewijzigd door #ANONIEM op 25-05-2011 23:05:25 ]


Inderdaad!quote:Op woensdag 25 mei 2011 22:50 schreef Mark94 het volgende:
[..]
Oja, want 0 graden Celsius is 273 Kelvin. Dus -10 graden Celsius zou dan 263 Kelvin zijn, en is inderdaad niet tegengesteld.


iemand dit weet en uitleg erbij kan geven:
Een temperatuurmeting heeft een meetgebied van 0 tot 100 graden Celsius. Hoeveel bits moet een A/D omzetter minimaal hebben om een resolutie van 0.1 graden Celsius (±0.05 graden Celsius) te krijgen?
Een temperatuurmeting heeft een meetgebied van 0 tot 100 graden Celsius. Hoeveel bits moet een A/D omzetter minimaal hebben om een resolutie van 0.1 graden Celsius (±0.05 graden Celsius) te krijgen?


Je hebt (100 - 0)/0.1 + 1 = 1001 verschillende waardenquote:Op donderdag 26 mei 2011 13:41 schreef vault_tec het volgende:
iemand dit weet en uitleg erbij kan geven:
Een temperatuurmeting heeft een meetgebied van 0 tot 100 graden Celsius. Hoeveel bits moet een A/D omzetter minimaal hebben om een resolutie van 0.1 graden Celsius (±0.05 graden Celsius) te krijgen?
Dus heb je een 2 log (1001) = 9.967
[ Bericht 6% gewijzigd door Nelis89 op 27-05-2011 19:55:59 ]
[img]http://i.minus.com/ibnbBZVlYCvsZI.gif[/img]


Finance vraagje,
Portfolio P bestaat uit diverse stocks + een risk free Treasury bill.
De risk free rate (Tbill rate) is 2%
Nu wil ik de expected return van Portfolio P berekenen. Voor de diverse stocks is een expected return + weight op gegeven. Maar voor de Tressuray bill is alleen de weight opgegeven.
Kun je nu voor deze treasury bill de risk free rate pakken om de expected return van de portfolio te berekenen?
Dus: weight * risk free rate + ........
Portfolio P bestaat uit diverse stocks + een risk free Treasury bill.
De risk free rate (Tbill rate) is 2%
Nu wil ik de expected return van Portfolio P berekenen. Voor de diverse stocks is een expected return + weight op gegeven. Maar voor de Tressuray bill is alleen de weight opgegeven.
Kun je nu voor deze treasury bill de risk free rate pakken om de expected return van de portfolio te berekenen?
Dus: weight * risk free rate + ........
BlaBlaBla


Lijkt mij wel.
Bij het berekenen van de standaarddeviatie van portfolio P hoef je pas moeilijk te doen aangezien er meestal een correlatie tussen de verschillende stocks is.
Bij het berekenen van de standaarddeviatie van portfolio P hoef je pas moeilijk te doen aangezien er meestal een correlatie tussen de verschillende stocks is.


is die +1 voor de waarde tussen 0 en de eerste ''stap''?quote:Op vrijdag 27 mei 2011 19:49 schreef Nelis89 het volgende:
[..]
Je hebt (100 - 0)/0.1 + 1 = 1001 verschillende waarden
Dus heb je een 2 log (1001) = 9.967 [ afbeelding ]10 bits A/D converter nodig


Tel je alle waarden die de temperatuur in jouw situatie aan kan nemen, dan kom je op 1001 waarden.quote:Op donderdag 2 juni 2011 19:25 schreef jabbahabba het volgende:
[..]
is die +1 voor de waarde tussen 0 en de eerste ''stap''?
Simpeler voorbeeldje: stel dat de temperatuur in hele graden gemeten zou worden en zou kunnen variëren tussen 0 en 10 °C. Dan heb je 11 verschillende meetwaarden in plaats van 10, namelijk 0, 1, 2, 3, 4, 5, 6, 7, 8, 9 en 10 °C. <- Tel ze maar na, het zijn er 11.


verkeerde topic 
Op dinsdag 9 augustus 2011 23:01 schreef SuperrrTuxxx het volgende:
Ik hou zoveel van jou, ik doe alles voor je! O+
Ik hou zoveel van jou, ik doe alles voor je! O+


Voor natuurkunde heb ik nu een paar hoofdstukken over licht en lenzen. Wat mij verwart is dat een virtueel beeld niet geprojecteerd kan worden maar een spiegel geeft een virtueel beeld.
Na wat googlen ben ik er nog steeds niet uit. Dus als iemand mij kan helpen, graag!
Na wat googlen ben ik er nog steeds niet uit. Dus als iemand mij kan helpen, graag!


Wat is precies je vraag? Hoe het komt dat je het beeld van een spiegel, terwijl dat beeld virtueel is, toch scherp kan zien? Dat ligt aan de positieve lens in je oog, die zorgt ervoor dat de lichtstralen weer convergeren.quote:Op zondag 12 juni 2011 16:06 schreef vault_tec het volgende:
Voor natuurkunde heb ik nu een paar hoofdstukken over licht en lenzen. Wat mij verwart is dat een virtueel beeld niet geprojecteerd kan worden maar een spiegel geeft een virtueel beeld.
Na wat googlen ben ik er nog steeds niet uit. Dus als iemand mij kan helpen, graag!
Als je iets anders bedoelt moet je het maar zeggen
The biggest argument against democracy is a five minute discussion with the average voter.


Ik snap het verschil niet tussen een virtueel en een reeel beeld. Want je kan een virtueel beeld niet projecteren (?) maar een spiegel kan je duidelijk zien en is een virtueel beeld. Dus wanneer is dan iets virtueel en wanneer is iets reeel?quote:Op zondag 12 juni 2011 16:06 schreef vault_tec het volgende:
Voor natuurkunde heb ik nu een paar hoofdstukken over licht en lenzen. Wat mij verwart is dat een virtueel beeld niet geprojecteerd kan worden maar een spiegel geeft een virtueel beeld.
Na wat googlen ben ik er nog steeds niet uit. Dus als iemand mij kan helpen, graag!


Bij een reëel beeld komen de stralen die van het object af komen, ook allemaal in één punt samen. In het plaatje hieronder is dat heel duidelijk te zien:quote:Op maandag 13 juni 2011 11:49 schreef vault_tec het volgende:
[..]
Ik snap het verschil niet tussen een virtueel en een reeel beeld. Want je kan een virtueel beeld niet projecteren (?) maar een spiegel kan je duidelijk zien en is een virtueel beeld. Dus wanneer is dan iets virtueel en wanneer is iets reeel?
Er is duidelijk een punt aan te wijzen waar de stralen bij elkaar komen, daar is dus een echt beeld te zien. Verder is ook duidelijk te zien dat de stralen na de spiegel/lens convergeren.
Bij een virtueel beeld komen de stralen niet samen in één punt, maar lijken ze allemaal uit één punt te komen. Dat is duidelijk te zien op het volgende plaatje:
De stippellijnen zijn de lijnen die je krijgt wanneer je de gespiegelde/gebroken lichtstralen 'terugtekent'. Deze lijnen komen ook in één punt samen, maar als je in dit punt gaat kijken zie je niks. Dat is het makkelijkst te begrijpen bij de spiegel, als je aan de andere kant van de spiegel gaat kijken zie je niets, al lijkt het wel alsof het beeld wat je ziet (als je voor de spiegel staat) daar vandaan komt.
De reden dat je een virtueel beeld wel kan zien, hoewel je het niet kan projecteren, heeft te maken met de positieve lens in je oog. Een virtueel beeld kan je niet projecteren, omdat de stralen divergeren. Deze divergerende stralen kunnen echter met de lens in je oog weer convergerend gemaakt worden, waarna ze in op je oog geprojecteerd worden.
Ik hoop dat het een beetje duidelijker geworden is
The biggest argument against democracy is a five minute discussion with the average voter.


Hoi, ik heb hier een vraag waar ik niet uitkom.
Mevrouw Kraker blijkt een laag kaliumgehalte te hebben. Dit zal per infuus worden aangevuld. Aanwezig is een 8% KCl oplossing in infuuszakken met NaCl 0,7% (750 ml). De arts schrijft 900 mg KCl per infuuszak voor.
Hoeveel ml KCl oplossing moet aan de infuuszak worden toegevoegd?
Rond (zo nodig) af op 1 decimaal.
Als je hem weet, ben je echt een held!
Mevrouw Kraker blijkt een laag kaliumgehalte te hebben. Dit zal per infuus worden aangevuld. Aanwezig is een 8% KCl oplossing in infuuszakken met NaCl 0,7% (750 ml). De arts schrijft 900 mg KCl per infuuszak voor.
Hoeveel ml KCl oplossing moet aan de infuuszak worden toegevoegd?
Rond (zo nodig) af op 1 decimaal.
Als je hem weet, ben je echt een held!


Ik ga het proberen uit te leggen, maar het is al een jaartje geleden dat ik iets aan scheikunde heb gedaan. Er zijn al infuuszakken van 750 mL aanwezig met 8% KCl. Hoeveel mL KCl bevat een infuuszak? (Ik ga er even vanuit dat het hier om volumeprocenten gaat, en dat KCl niet reageren, wat ik niet zeker weet)quote:Op dinsdag 14 juni 2011 01:05 schreef glaba het volgende:
Hoi, ik heb hier een vraag waar ik niet uitkom.
Mevrouw Kraker blijkt een laag kaliumgehalte te hebben. Dit zal per infuus worden aangevuld. Aanwezig is een 8% KCl oplossing in infuuszakken met NaCl 0,7% (750 ml). De arts schrijft 900 mg KCl per infuuszak voor.
Hoeveel ml KCl oplossing moet aan de infuuszak worden toegevoegd?
Rond (zo nodig) af op 1 decimaal.
Als je hem weet, ben je echt een held!
Dit volume kan je met behulp van de dichtheid omrekenen naar het aantal milligram (de dichtheid van kaliumchloride is 1,987 g/cm³, dus het aantal milligram kan je berekenen door het aantal milliliter keer dit getal te doen, want één milliliter = één cm3)
Omdat je dit getal moet aanvullen tot 900 mg, moet je 900 min dit getal doen, en dat is je antwoord.
(Ik was nooit goed in scheikunde, maar ik hoop dat ik dit goed heb gedaan... Ik ben er nog steeds niet uit of KCl en NaCl zouden moeten reageren, als ze dat wel doen heb je niks aan deze post
Finally, someone let me out of my cage


Bedankt voor je uitleg op dit late tijdstip! 
Ik kom dan uit op 780,8 helaas zegt hij dat het niet klopt. Klopt het wel dat één mililiter = één cm3 is?
Dit is overigens de site waar ik de opgave vandaan heb gehaald en je het antwoord kan invullen.
http://wiskunde.stmichael(...)_medisch_rekenen.htm
Ik kom dan uit op 780,8 helaas zegt hij dat het niet klopt. Klopt het wel dat één mililiter = één cm3 is?
Dit is overigens de site waar ik de opgave vandaan heb gehaald en je het antwoord kan invullen.
http://wiskunde.stmichael(...)_medisch_rekenen.htm


Het antwoord klopt niet, omdat de uitleg niet klopt.
8% KCl-oplossing betekent dat er 8 g KCl opgelost is per 100 ml oplossing. Percentages van zulk soort oplossingen luiden, tenzij anders vermeld, altijd in massa per volume-eenheid. De vraag die je dus moet oplossen is: hoeveel milliliter oplossing heb je nodig als je weet dat er 8 g KCl in 100 ml oplossing zit?
Antwoord: 0,9/8 * 100 = 11,3 ml.
8% KCl-oplossing betekent dat er 8 g KCl opgelost is per 100 ml oplossing. Percentages van zulk soort oplossingen luiden, tenzij anders vermeld, altijd in massa per volume-eenheid. De vraag die je dus moet oplossen is: hoeveel milliliter oplossing heb je nodig als je weet dat er 8 g KCl in 100 ml oplossing zit?
Antwoord: 0,9/8 * 100 = 11,3 ml.


ik, nee.quote:Op dinsdag 14 juni 2011 17:47 schreef Ouail222 het volgende:
Wie is goed in Engels en wil mijn vijf opdrachten voor mij nakijken?
tevens: [ bèta overig] huiswerk- en vragentopic.
26"
Fading slowly.
Fading slowly.


Excuses in dat geval, in mijn herinnering ging het altijd om massapercentages of volumepercentages. Heb ik ook weer wat geleerdquote:Op dinsdag 14 juni 2011 10:14 schreef lyolyrc het volgende:
Het antwoord klopt niet, omdat de uitleg niet klopt.
8% KCl-oplossing betekent dat er 8 g KCl opgelost is per 100 ml oplossing. Percentages van zulk soort oplossingen luiden, tenzij anders vermeld, altijd in massa per volume-eenheid. De vraag die je dus moet oplossen is: hoeveel milliliter oplossing heb je nodig als je weet dat er 8 g KCl in 100 ml oplossing zit?
Antwoord: 0,9/8 * 100 = 11,3 ml.
Ik zie nu ook dat ik de vraag verkeerd gelezen heb, ik bakte er eigenlijk niks van
nog even naar kijken dan...
[ Bericht 5% gewijzigd door minibeer op 14-06-2011 20:26:47 ]
Finally, someone let me out of my cage


Er zijn nogal wat verschillende manieren om een concentratie uit te drukken. Het is dus ook een kwestie van bekend zijn met de gebruikelijke manier voor dit soort vraagstukken.quote:Op dinsdag 14 juni 2011 20:12 schreef minibeer het volgende:
[..]
Excuses in dat geval, in mijn herinnering ging het altijd om massapercentages of volumepercentages. Heb ik ook weer wat geleerd
Ik zie nu ook dat ik de vraag verkeerd gelezen heb, ik bakte er eigenlijk niks van
nog even naar kijken dan...
In jouw antwoord ging je werken met dichtheid, maar dat had hier geen zin. KCl valt bij oplossen in water namelijk uiteen in de ionen K+ en Cl-. Die ionen hoeven opgelost in water niet per se hetzelfde volume in te nemen als dat ze doen als vaste stof.
Het was jammer dat je antwoord niet klopte, maar het was natuurlijk wel goed dat je probeerde te helpen!


Kan iemand kijken of de volgende opdracht goed gemaakt is?
Niveau: Atheneum 3.
Opdracht 1)
Pieter makt een foto van de toren van Pisa (55 meter hoog).
De lenssterkte van zijn fotolens is +21dpt.
Als Pieter de foto maakt staat hij 63 meter van de toren af.
Bereken hoe groot de afbeelding van de toren is.
Mijn antwoord:
LL' = 55 Meter
V = 63 Meter
S = 21 dpt
f = 0,0476 Meter
b = 0,0476 Meter
N = 4,56*10^-4
BB' = 4,16 CM
Berekening:
LL' : Gegeven
v : Gegeven
s : Gegeven
f : s=1/f 21=1/f 1*1/21 = 0,0476 Meter
b :1/f =1/b+1/v, 1/f-1/v=1/b, 1/0,0467-1/63=b= 0,0476 Meter
N : b/v = 0,0476/63= 7,56*10^-4
BB' : N= BB'/LL' 7,56*10^-4 = BB'/55 meter BB' = 4,16 CM.
Zeg asjeblieft dat dit juist is.
Niveau: Atheneum 3.
Opdracht 1)
Pieter makt een foto van de toren van Pisa (55 meter hoog).
De lenssterkte van zijn fotolens is +21dpt.
Als Pieter de foto maakt staat hij 63 meter van de toren af.
Bereken hoe groot de afbeelding van de toren is.
Mijn antwoord:
LL' = 55 Meter
V = 63 Meter
S = 21 dpt
f = 0,0476 Meter
b = 0,0476 Meter
N = 4,56*10^-4
BB' = 4,16 CM
Berekening:
LL' : Gegeven
v : Gegeven
s : Gegeven
f : s=1/f 21=1/f 1*1/21 = 0,0476 Meter
b :1/f =1/b+1/v, 1/f-1/v=1/b, 1/0,0467-1/63=b= 0,0476 Meter
N : b/v = 0,0476/63= 7,56*10^-4
BB' : N= BB'/LL' 7,56*10^-4 = BB'/55 meter BB' = 4,16 CM.
Zeg asjeblieft dat dit juist is.


Hij klopt bijna, je hebt alleen een foutje gemaakt bij de berekening van de beeldafstand. Deze afstand haal je uit 1/f=1/b+1/v, maar bij jou zijn f en b aan elkaar gelijk. Dat zou alleen kunnen als 1/v nul is, en dat is hier niet het geval. Probeer de formule zo om te schrijven dat je alleen nog maar f en b in hoeft te vullen, en dat b er dan zo uitrolt (dus van de vorm b = ...). De rest klopt zo te zien wel  .
.
The biggest argument against democracy is a five minute discussion with the average voter.


Wat ik doe is dit:
1/f = 1/b + 1/v
1/f - 1/v = 1/b
1/0,0476 - 1/63 = 1/b
21 - 0,016 = 1/b
21 = 1/b
b = 0,0476
Wat doe ik fout dan:( ?
1/f = 1/b + 1/v
1/f - 1/v = 1/b
1/0,0476 - 1/63 = 1/b
21 - 0,016 = 1/b
21 = 1/b
b = 0,0476
Wat doe ik fout dan:( ?


Sorry, je hebt helemaal gelijk! Omdat die voorwerpsafstand relatief erg groot is, mag je 1/v wel nul stellen (je kan beter gewoon, zoals je ook deed, alles netjes uitwerken, dan krijg je ook niet zulke vergissingen  ).
).
The biggest argument against democracy is a five minute discussion with the average voter.


Kan iemand mij de formule van de evenwichtsconstante misschien uitleggen?
pA+qB rC+sD
Kan iemand uitleggen waarom die formule er zo uitziet en bijvoorbeeld niet zo:
pA+qB rC+sD
K= (r[C]+s[D])/(p[A]+q[B])
sorry als dit een domme vraag is.
pA+qB rC+sD
Kan iemand uitleggen waarom die formule er zo uitziet en bijvoorbeeld niet zo:
pA+qB rC+sD
K= (r[C]+s[D])/(p[A]+q[B])
sorry als dit een domme vraag is.


Iemand die toevallig de werking van een MRP [Material requirements planning] snapt?
Ps. Weet niet zeker of het in dit topic thuishoort?
Ps. Weet niet zeker of het in dit topic thuishoort?


Ik heb een vraag over een opgave over een Double-Slit experiment.
Twee monochromatische lichtstralen gaan via een slit en komen elkaar weer tegen op een scherm. De lichtstralen komen elkaar tegen bij n=8. Het weglengte verschil is 4,57 x 10^-6m. Wat is λ?
d sin θ = n x λ
Hoe kom ik nu aan λ?
d is volgens mij die 4,57x10^-6 m. Maar hoe bereken in nu die hoek?
Twee monochromatische lichtstralen gaan via een slit en komen elkaar weer tegen op een scherm. De lichtstralen komen elkaar tegen bij n=8. Het weglengte verschil is 4,57 x 10^-6m. Wat is λ?
d sin θ = n x λ
Hoe kom ik nu aan λ?
d is volgens mij die 4,57x10^-6 m. Maar hoe bereken in nu die hoek?
AJAX AMSTERDAM!


Wie kan deze vraag oplossen, en uitleggen hoe je dit doet want ik weet niet waar ik beginnen moet.
Vraag
Bereken de molariteit van een geconcentreerde azijnzuuroplossing.
Gegeven: dichtheid geconc. azijnzuur = 1.044 g/cm3 concentratie ch3cooh 100 m/m %
Vraag
Bereken de molariteit van een geconcentreerde azijnzuuroplossing.
Gegeven: dichtheid geconc. azijnzuur = 1.044 g/cm3 concentratie ch3cooh 100 m/m %


571 nmquote:Op woensdag 31 augustus 2011 15:41 schreef bloodysunday het volgende:
Ik heb een vraag over een opgave over een Double-Slit experiment.
Twee monochromatische lichtstralen gaan via een slit en komen elkaar weer tegen op een scherm. De lichtstralen komen elkaar tegen bij n=8. Het weglengte verschil is 4,57 x 10^-6m. Wat is λ?
d sin θ = n x λ
Hoe kom ik nu aan λ?
d is volgens mij die 4,57x10^-6 m. Maar hoe bereken in nu die hoek?
Als de afstand tussen de twee spleten (d) veel kleiner is dan de afstand tot het scherm (L), m.a.w. d << L, dan kun je zeggen dat het weglengteverschil r1 - r2 = d sinθ.
De hoek tussen x (afstand tussen n=0 en in dit geval n=8) en L is dan weer θ
Het weglengteverschil is gegeven, dus r1 - r2 = d sinθ = 4,57E-6 m en daaruit volgt dat λ = 4,57E-6 / 8 = 571,25 nm.


Ligt het nou aan mij of klopt de eenheid hier niet of is het wel erg kort door de bocht geschreven? Meer dan meter/meter mol/mol kan ik er niet van makenquote:Op donderdag 1 september 2011 15:58 schreef jouwkeuze het volgende:
Wie kan deze vraag oplossen, en uitleggen hoe je dit doet want ik weet niet waar ik beginnen moet.
Vraag
Bereken de molariteit van een geconcentreerde azijnzuuroplossing.
Gegeven: dichtheid geconc. azijnzuur = 1.044 g/cm3 concentratie ch3cooh 100 m/m %


Kan zijn dat 'ie mol per milliliter bedoelde - percentageteken is dan nog wel een beetje vreemd.quote:Op donderdag 1 september 2011 16:35 schreef zoem het volgende:
[..]
Ligt het nou aan mij of klopt de eenheid hier niet of is het wel erg kort door de bocht geschreven? Meer dan meter/meter mol/mol kan ik er niet van maken


Ik heb het letterlijk zo uit mijn werkboek overgetypt en dacht dus dat ik dom was omdat ik het niet snapte maar er blijkt dus niets van te kloppen, wat ik dus al vermoedde. Zal het morgen even aan de leraar vragen


Klopt wel, is massapercentage;
De massafractie wordt vaak als percentage weergegeven, en dan massa-percentage genoemd. De grootheid wordt aangeduid met %(m/m).
Je weet hoeveel gram er in 1 cm³ zit, dus kan je bepalen hoeveel er in 1 dm³/1 liter zit.
Dan met de molmassa en het aantal gram azijnzuur het aantal mol azijnzuur uitrekenen hoeveel er dus in 1 liter zit en dat is de molariteit.
De massafractie wordt vaak als percentage weergegeven, en dan massa-percentage genoemd. De grootheid wordt aangeduid met %(m/m).
Je weet hoeveel gram er in 1 cm³ zit, dus kan je bepalen hoeveel er in 1 dm³/1 liter zit.
Dan met de molmassa en het aantal gram azijnzuur het aantal mol azijnzuur uitrekenen hoeveel er dus in 1 liter zit en dat is de molariteit.


Je kunt altijd het beste beginnen met het opschrijven wat je al weet. Je hebt de gegevens uit de vraag (1) en je hebt een stuk theorie gekregen (2) met formules. Wat heb je en waar moet je naartoe? Zoek de juiste formule(s) op en begin gewoon met opschrijven en rekenen. Een puzzle maak je tenslotte ook niet door alle stukjes afzonderlijk te bekijken. Je zult ze onderling moeten vergelijken en proberenquote:Op donderdag 1 september 2011 15:58 schreef jouwkeuze het volgende:
Wie kan deze vraag oplossen, en uitleggen hoe je dit doet want ik weet niet waar ik beginnen moet.
Vraag
Bereken de molariteit van een geconcentreerde azijnzuuroplossing.
Gegeven: dichtheid geconc. azijnzuur = 1.044 g/cm3 concentratie ch3cooh 100 m/m %
Bij een vraag als dit wéét je gewoon dat je de molmassa nodig hebt. De dichtheid zul je om moeten rekenen, want dat is nodig om de molariteit te berekenen (je moet dus wel je definities en bijbehorende eenheden kennen!).
Voor mij is dit weer al ruim 6 jaar geleden, dus fouten voorbehouden
De molmassa van azijnzuur:
Dichtheid omrekenen:
We weten dat:
Dus:
[ Bericht 12% gewijzigd door zoem op 02-09-2011 00:16:41 ]


ah thx, ik zat met de verkeerde weglengte. Zo is het duidelijk!quote:Op donderdag 1 september 2011 16:23 schreef zoem het volgende:
[..]
571 nm
Als de afstand tussen de twee spleten (d) veel kleiner is dan de afstand tot het scherm (L), m.a.w. d << L, dan kun je zeggen dat het weglengteverschil r1 - r2 = d sinθ.
[ afbeelding ]
De hoek tussen x (afstand tussen n=0 en in dit geval n=8) en L is dan weer θ
Het weglengteverschil is gegeven, dus r1 - r2 = d sinθ = 4,57E-6 m en daaruit volgt dat λ = 4,57E-6 / 8 = 571,25 nm.
AJAX AMSTERDAM!


Hoi,
Ik ben bezig met een marktonderzoek en ik heb een deelvraag 'Wie zijn de jongeren van 18 tot 24 jaar?'
En dit zijn mijn sub vragen
• Wat zijn de maandelijkse inkomsten en uitgaven?
• Hoeveel tijd besteden ze aan sport en welke sport?
Volgens mijn docent moeten mijn sub vragen uitgebreider zijn, maar mijn vraag is: hoe moeten ze uitgebreider zijn geformuleerd? Kan iemand me dat vertellen door mijn sub vragen uitgebreider te formuleren? Alvast bedankt voor uw antwoord!!
Mvg,
superky
Ik ben bezig met een marktonderzoek en ik heb een deelvraag 'Wie zijn de jongeren van 18 tot 24 jaar?'
En dit zijn mijn sub vragen
• Wat zijn de maandelijkse inkomsten en uitgaven?
• Hoeveel tijd besteden ze aan sport en welke sport?
Volgens mijn docent moeten mijn sub vragen uitgebreider zijn, maar mijn vraag is: hoe moeten ze uitgebreider zijn geformuleerd? Kan iemand me dat vertellen door mijn sub vragen uitgebreider te formuleren? Alvast bedankt voor uw antwoord!!
Mvg,
superky


Bedoelt je docent niet dat je méér subvragen moet formuleren? Het lijkt me namelijk vrij relevant om bijvoorbeeld geslacht, leeftijd en opleiding van de ondervraagde groep te kennen.quote:Op zaterdag 17 september 2011 21:28 schreef superky het volgende:
Hoi,
Ik ben bezig met een marktonderzoek en ik heb een deelvraag 'Wie zijn de jongeren van 18 tot 24 jaar?'
En dit zijn mijn sub vragen
• Wat zijn de maandelijkse inkomsten en uitgaven?
• Hoeveel tijd besteden ze aan sport en welke sport?
Volgens mijn docent moeten mijn sub vragen uitgebreider zijn, maar mijn vraag is: hoe moeten ze uitgebreider zijn geformuleerd? Kan iemand me dat vertellen door mijn sub vragen uitgebreider te formuleren? Alvast bedankt voor uw antwoord!!
Mvg,
superky


Nee dat bedoelt ze niet. En die subvragen die je had genoemd gaat iemand anders doen in mijn groepje. Het gaat echt om mijn sub vragen hier, wat ik totaal niet snap. Ik bedoel je hoe ik mijn sub vragen kan uitbreiden :S??quote:Op zaterdag 17 september 2011 23:29 schreef lyolyrc het volgende:
[..]
Bedoelt je docent niet dat je méér subvragen moet formuleren? Het lijkt me namelijk vrij relevant om bijvoorbeeld geslacht, leeftijd en opleiding van de ondervraagde groep te kennen.


Denk dat je docent dit bedoelt:quote:Op zaterdag 17 september 2011 21:28 schreef superky het volgende:
Hoi,
Ik ben bezig met een marktonderzoek en ik heb een deelvraag 'Wie zijn de jongeren van 18 tot 24 jaar?'
En dit zijn mijn sub vragen
• Wat zijn de maandelijkse inkomsten en uitgaven?
• Hoeveel tijd besteden ze aan sport en welke sport?
Volgens mijn docent moeten mijn sub vragen uitgebreider zijn, maar mijn vraag is: hoe moeten ze uitgebreider zijn geformuleerd? Kan iemand me dat vertellen door mijn sub vragen uitgebreider te formuleren? Alvast bedankt voor uw antwoord!!
Mvg,
superky
- Waaruit halen de jongeren hun maandelijkse inkomsten en hoe groot zijn deze?
- Waaraan besteden de jongeren hun maandelijkse inkomsten en hoe groot zijn deze?
- Hoeveel tijd besteden jongeren per week/maand aan sport (en andere vrije tijdsbesteding)?
[img]http://i.minus.com/ibnbBZVlYCvsZI.gif[/img]


Moeten woorden als hogescholen en universiteiten met hoofdletter?
Het gaat hier bijvoorbeeld niet over een naam zoals Avans Hogeschool, maar gewoon over een willekeurige hogeschool/uni
Het gaat hier bijvoorbeeld niet over een naam zoals Avans Hogeschool, maar gewoon over een willekeurige hogeschool/uni
Cuz I'm Mr. Brightside


Als los woord hoef je geen hoofdletter te gebruiken. Dat is alleen als je het over de naam van de school hebt zoals Avans Hogeschool, Technische Universiteit Delft, etc


Thanksquote:Op maandag 19 september 2011 20:35 schreef zoem het volgende:
Als los woord hoef je geen hoofdletter te gebruiken. Dat is alleen als je het over de naam van de school hebt zoals Avans Hogeschool, Technische Universiteit Delft, etc
Cuz I'm Mr. Brightside


Ik heb een relatief simpele vraag (denk ik) over het maken van een oplossing.
Er staat "maak een oplossing van 50ml van 50mg/ml citroenzuur (houdt rekening met de aanwezigheid van een watermolecuul in het kristal)."
Als ik een oplossing van 50ml moet hebben, en ik moet een concentratie aanhouden van 50mg per milliliter, dan kan ik toch niet anders dan 50*50 doen? Dan snap ik de relevantie van dat watermolecuul niet. Maar ik zal vast ergens een denkfout maken. Of is het een foutje in de tekst, en vragen ze gewoon 50mg/ml citroenzuuroplossing, zonder een totale hoeveelheid aan te geven?
Nee ik heb geen chemie gehad op de middelbare idd
Edit: ok ik ben nu zo ver dat de berekening idd gewoon zo simpel is, maar ik snap nog steeds niet wat ik aan dat verhaal over het watermolecuul heb. Iemand zei me zojuist via facebook dat dat iets uitmaakt voor als je molwaarden gaat berekenen ofzo, maar waarom dan?
[ Bericht 15% gewijzigd door lateralize op 20-09-2011 15:05:59 ]
Er staat "maak een oplossing van 50ml van 50mg/ml citroenzuur (houdt rekening met de aanwezigheid van een watermolecuul in het kristal)."
Als ik een oplossing van 50ml moet hebben, en ik moet een concentratie aanhouden van 50mg per milliliter, dan kan ik toch niet anders dan 50*50 doen? Dan snap ik de relevantie van dat watermolecuul niet. Maar ik zal vast ergens een denkfout maken. Of is het een foutje in de tekst, en vragen ze gewoon 50mg/ml citroenzuuroplossing, zonder een totale hoeveelheid aan te geven?
Nee ik heb geen chemie gehad op de middelbare idd
Edit: ok ik ben nu zo ver dat de berekening idd gewoon zo simpel is, maar ik snap nog steeds niet wat ik aan dat verhaal over het watermolecuul heb. Iemand zei me zojuist via facebook dat dat iets uitmaakt voor als je molwaarden gaat berekenen ofzo, maar waarom dan?
[ Bericht 15% gewijzigd door lateralize op 20-09-2011 15:05:59 ]


Bedank voor jouw antwoord! Maar ik heb nog een vraagje over: 'Waaraan besteden de jongeren van 18 tot 24 jaar hun maandelijkse inkomsten en hoe groot zijn deze?''quote:Op zondag 18 september 2011 22:05 schreef Nelis89 het volgende:
[..]
Denk dat je docent dit bedoelt:
- Waaruit halen de jongeren hun maandelijkse inkomsten en hoe groot zijn deze?
- Waaraan besteden de jongeren hun maandelijkse inkomsten en hoe groot zijn deze?
- Hoeveel tijd besteden jongeren per week/maand aan sport (en andere vrije tijdsbesteding)?
Ik had al gezocht naar het antwoord op het internet, maar ik kon er nog niks over vinden. Ik had al op google, cbs en op lexis nexus newsportal gekeken. Maar nog steeds niks
Alvast bedankt voor uw antwoord!


Iemand nog?? De rest van mijn sub vragen had ik al bronnen gevonden. Behalve van deze sub vraag 1.3 Waaraan besteden de jongeren van 18 tot 24 jaar hun maandelijkse inkomsten en hoe groot zijn deze?
Alvast bedankt voor uw antwoord!
Groet,
superky
Alvast bedankt voor uw antwoord!
Groet,
superky


[beta] huiswerk- en vragentopicquote:Op donderdag 22 september 2011 16:19 schreef superky het volgende:
Iemand nog?? De rest van mijn sub vragen had ik al bronnen gevonden. Behalve van deze sub vraag 1.3 Waaraan besteden de jongeren van 18 tot 24 jaar hun maandelijkse inkomsten en hoe groot zijn deze?
Alvast bedankt voor uw antwoord!
Groet,
superky


Ik moet vergelijkingen oplossen, ik weet het heel makkelijk alleen weet ik niet hoe hun het andtwoordt op die manier geschreven krijgen
Vraag:
0.33x^2 - 0.125 = 0.25
mijn antwoord was (Wortel)1.25
maar hun hebben 0.5(wortel)5
(sorry dat ik het zo typ maar ik kon die tekens niet vinden)
Vraag:
0.33x^2 - 0.125 = 0.25
mijn antwoord was (Wortel)1.25
maar hun hebben 0.5(wortel)5
(sorry dat ik het zo typ maar ik kon die tekens niet vinden)


Je kan je antwoord op de volgende manier omschrijven:quote:Op vrijdag 23 september 2011 19:33 schreef jouwkeuze het volgende:
Ik moet vergelijkingen oplossen, ik weet het heel makkelijk alleen weet ik niet hoe hun het andtwoordt op die manier geschreven krijgen
Vraag:
0.33x^2 - 0.125 = 0.25
mijn antwoord was (Wortel)1.25
maar hun hebben 0.5(wortel)5
(sorry dat ik het zo typ maar ik kon die tekens niet vinden)
Het antwoord is echter niet goed, er komt uit
The biggest argument against democracy is a five minute discussion with the average voter.


Hoi,
Ik heb een vraagje
Wat bedoelen ze eigenlijk met: in viervoud inleveren?
Bedoelen ze misschien in 4 kopietjes inleveren? Alvast bedankt voor je antwoord
groet,
Ik heb een vraagje
Wat bedoelen ze eigenlijk met: in viervoud inleveren?
Bedoelen ze misschien in 4 kopietjes inleveren? Alvast bedankt voor je antwoord
groet,


Je mag niet meer radenquote:Op maandag 26 september 2011 18:01 schreef superky het volgende:
Hoi,
Ik heb een vraagje
Wat bedoelen ze eigenlijk met: in viervoud inleveren?
Bedoelen ze misschien in 4 kopietjes inleveren? Alvast bedankt voor je antwoord
groet,
Viervoud betekent niets anders dan 4 (identieke) exemplaren van een document.


Ik heb een vraag over een titratie die ik moet doen. Ik moet het mierenzuurgehalte bepalen in wc-
eend.
Nu is de vraag:
Leid zelf een berekenigsformule af voor het berekenen van het mierenzuurgehalte% (m/m) in Wc-eend. Bereken hoeveel gram wc-eend moet worden afgewogen voor een natronloogverbruik van ca. 30 ml. (concentratie NaOH = ca. 0,1 mol/l).
reactievergelijking: HCOOH + OH ------> Hcoo + H2O
Ik snap de hele vraag niet, en heb geen idee wat ik moet doen. Wie kan me op weg helpen?
Alvast bedankt
eend.
Nu is de vraag:
Leid zelf een berekenigsformule af voor het berekenen van het mierenzuurgehalte% (m/m) in Wc-eend. Bereken hoeveel gram wc-eend moet worden afgewogen voor een natronloogverbruik van ca. 30 ml. (concentratie NaOH = ca. 0,1 mol/l).
reactievergelijking: HCOOH + OH ------> Hcoo + H2O
Ik snap de hele vraag niet, en heb geen idee wat ik moet doen. Wie kan me op weg helpen?
Alvast bedankt


De bedoeling van een titratie is dat je de concentratie van een stof gaat bepalen met een oplossing van een andere stof waarvan je de concentratie precies kent.(Het klopt daarom ook niet dat de concentratie van natronloog zo onnauwkeurig wordt gegeven!) Doordat je die concentratie van die andere stof precies kent en je ook nauwkeurig bepaalt hoeveel je ervan toevoegt, kun je berekenen hoeveel er van de ene stof aanwezig was.quote:Op maandag 26 september 2011 21:43 schreef daantje1044 het volgende:
Ik heb een vraag over een titratie die ik moet doen. Ik moet het mierenzuurgehalte bepalen in wc-
eend.
Nu is de vraag:
Leid zelf een berekenigsformule af voor het berekenen van het mierenzuurgehalte% (m/m) in Wc-eend. Bereken hoeveel gram wc-eend moet worden afgewogen voor een natronloogverbruik van ca. 30 ml. (concentratie NaOH = ca. 0,1 mol/l).
reactievergelijking: HCOOH + OH ------> Hcoo + H2O
Ik snap de hele vraag niet, en heb geen idee wat ik moet doen. Wie kan me op weg helpen?
Alvast bedankt
In dit geval ga je dus mierezuur met natronloog titreren. Dat geeft de reactievergelijking:
HCOOH + OH- ------> HCOO- + H2O
Je had zelf niet de ladingen van het hydroxy- en methanoaat-ion opgeschreven. Let daarop, want die moeten er wel staan!
De formule voor het gehalte mierezuur in WC-eend kun je afleiden:
• Tijdens de titratie meet je het aantal ml natronloog dat je toevoegt: Vnatronloog
• Als je dit vermenigvuldigt met de concentratie van natronloog [OH-], krijg je het aantal mol OH- dat je hebt toegevoegd.
• Natronloog reageert 1:1 met mierezuur, dus er reageert evenveel mol mierezuur weg als je mol OH- toevoegt.
• Vermenigvuldigen van het aantal mol mierezuur met de molmassa van mierezuur MWHCOOH geeft de massa van het mierezuur in gram.
• Delen van de massa van mierezuur door de massa van WC-eend mWC-eend (in gram!) dat je titreert geeft de massaverhouding van mierezuur en WC-eend.
• Vermenigvuldigen met 100% geeft deze verhouding weer als percentage.
Probeer hier eens een formule van te maken (antwoord in de spoiler).
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Kan iemand me uitleggen, hoe je een goede VLS maakt?
Ik weet wel hoe het gaat, maar ik vergeet er steeds een paar, of de richting van de krachten staan verkeerd.
Ik weet wel hoe het gaat, maar ik vergeet er steeds een paar, of de richting van de krachten staan verkeerd.


Heb je een voorbeeld voor mij, liefst eentje die je zelf niet zo goed begrijpt? Dan wil ik het best voor je uitleggenquote:Op vrijdag 7 oktober 2011 13:36 schreef snellehenk het volgende:
Kan iemand me uitleggen, hoe je een goede VLS maakt?
Ik weet wel hoe het gaat, maar ik vergeet er steeds een paar, of de richting van de krachten staan verkeerd.


Hoi,
Ik heb een vraagje, ik wil graag weten: Hoeveel uur per week uitwonend studerende mannen in Amsterdam van 18 t/m 21 jaar (die het hoger onderwijs volgen) besteden aan internet en het lezen van een tijdschrift.
Verder had ik al gezocht op os amsterdam, maar ik kon nog niks vinden. Kan iemand me misschien helpen ? Alvast bedankt voor jouw hulp!
? Alvast bedankt voor jouw hulp!
Groet,
superky
Ik heb een vraagje, ik wil graag weten: Hoeveel uur per week uitwonend studerende mannen in Amsterdam van 18 t/m 21 jaar (die het hoger onderwijs volgen) besteden aan internet en het lezen van een tijdschrift.
Verder had ik al gezocht op os amsterdam, maar ik kon nog niks vinden. Kan iemand me misschien helpen
Groet,
superky


quote:Op vrijdag 7 oktober 2011 13:40 schreef zoem het volgende:
[..]
Heb je een voorbeeld voor mij, liefst eentje die je zelf niet zo goed begrijpt? Dan wil ik het best voor je uitleggen
sorry voor mijn late reactie, maar ik had wat problemen met mijn computer,
zou je er alsnog voor mij naar willen kijken?


Ja hoorquote:Op maandag 10 oktober 2011 14:16 schreef snellehenk het volgende:
[..]
[ afbeelding ]
sorry voor mijn late reactie, maar ik had wat problemen met mijn computer,
zou je er alsnog voor mij naar willen kijken?
Ik heb het uitgewerkt op papier en ingescand:
subscript h staat voor horizontale component en v voor verticale component
Uitleg
Als je naar de opdracht kijkt dan moeten al een paar dingen je opvallen:
- punt A is een scharnierpunt en kent dus geen moment
- punt C is eigenlijk ook een soort scharnierpunt en ook hier geen moment
- tussen B en C is een touw gespannen en kent dus alleen een trekkracht
De methode die ik nu gebruik werkt aan de hand van de krachtenevenwichten in elk punt (node). Je trekt de constructie uit elkaar, zodat je elk punt of lijnsegment afzonderlijk kunt gaan analyseren.
Het is het gemakkelijkst om te beginnen met punt C. Hier weet je dat er een touw aan trekt met kracht FBC. Omdat het touw alleen trekkracht kent, weet je dat in het touwsegment de richting van de kracht "naar buiten toe" is. Dus de kracht die op punt C werkt is dan precies het tegenovergestelde zoals je in de tekening ziet (er wordt als het ware getrokken aan punt C). Punt C zit vast aan de muur die weerstand biedt in horizontale en verticale richting. Aangezien FBC naar rechts en naar beneden werkt, zullen de krachten in de muur naar links en naar boven moeten zijn om een evenwicht te creëren in horizontale en verticale richting (FBC kun je namelijk ook weer opdelen in een hor+vert component).
Vervolgens ga je naar punt B. Ook daar trekt het touw aan en net zoals bij punt C krijg je een kracht FBC die een tegenovergestelde richting heeft van het touw. Daarnaast werkt er een (gegeven) kracht F2 op punt B. Punt B zit ook nog eens vast aan staaf ABD en zal er een kracht bestaan tussen B en D: FBD. Kracht FBC wijst naar links+boven en kracht F2 naar beneden. Een staaf kent alleen trek- of compressiekrachten in de lengterichting, dus om een evenwicht te krijgen zal FBD wel naar rechtsboven moeten wijzen. De andere optie was linksonder, maar dan heb je geen evenwicht!
Punt D kent de tegenovergestelde kracht die vanuit B op D werkt. FBD wijst de tegenovergestelde kant op in D. Er is een gegeven verticale kracht F1 in D en er werkt een kracht tussen A en D: FAD. Wederom horizontale+verticale krachtenevenwichten in het punt: FBD en F1 wijzen naar beneden, dus dan blijft voor FAD alleen de richting rechtsboven over.
Punt A kent de tegenovergestelde kracht die vanuit D op A werkt (zelfde verhaal als in punt D). Punt A zit vast aan de muur en zal een kracht naar boven en een kracht naar rechts moeten hebben om een evenwicht te creëren met FAD.
Uiteindelijk zie je dat in het bovenste plaatje de krachten zowel horizontaal als verticaal in evenwicht zijn. De kracht in FBD kun je het makkelijkst uitrekenen door een moment om punt A te doen en het touw te vervangen door de kracht FBD. Opdelen van deze kracht in een horizontale+verticale component maakt het uitrekenen makkelijker.
Uitleg werd langer dan gedacht. Het kan maar duidelijk zijn


Speciale relativiteitstheorie:
Een neutron beweegt met snelheid v = 0.3c van een melkwegstelsel af. Als het neutron zich op 1 lichtjaar afstand van het centrum bevindt, zendt hij een elektron met snelheid u = 0.5c t.o.v. het neutron de andere kant op (naar het centrum).
Hoe lang duurt het voordat het elektron het centrum bereikt, gemeten door een waarnemer in het melkwegstesell?
Ik heb de relatieve snelheid van het elektron t.o.v. het melkwegstelsel berekend: w = -0.24 c.
Mag ik nu zeggen, omdat het melkwegstelsel in rust is, t melkweg = lichtjaar/ 0,24c = 4.17 jaar, of moet ik met lorentztransformaties werken?
Een neutron beweegt met snelheid v = 0.3c van een melkwegstelsel af. Als het neutron zich op 1 lichtjaar afstand van het centrum bevindt, zendt hij een elektron met snelheid u = 0.5c t.o.v. het neutron de andere kant op (naar het centrum).
Hoe lang duurt het voordat het elektron het centrum bereikt, gemeten door een waarnemer in het melkwegstesell?
Ik heb de relatieve snelheid van het elektron t.o.v. het melkwegstelsel berekend: w = -0.24 c.
Mag ik nu zeggen, omdat het melkwegstelsel in rust is, t melkweg = lichtjaar/ 0,24c = 4.17 jaar, of moet ik met lorentztransformaties werken?


Kan hier iemand wat vinden over oud premier Dries van Agt ik heb alleen iets op Wiki gevonden. Maar dat is ook niet veel..


Niet echt bèta eigenlijk. Maar wat zoek je precies? Dit is nogal algemeen...quote:Op maandag 10 oktober 2011 20:32 schreef bjanaan het volgende:
Kan hier iemand wat vinden over oud premier Dries van Agt ik heb alleen iets op Wiki gevonden. Maar dat is ook niet veel..


Biografie.quote:Op maandag 10 oktober 2011 20:36 schreef zoem het volgende:
[..]
Niet echt bèta eigenlijk. Maar wat zoek je precies? Dit is nogal algemeen...


ff een vraag ter controle of ik het nu goed doe met die berekeningsformule.
sorry voor de opmaak: link in de op werkt niet
De vraag is: leid zelf een berekeningsformule af voor het berekenen van de massa die er aan calciumcarbonaat moet worden ingewogen voor een natronloogverbruik van 25 ml ( concentratie NaOH = 0,1 mol/l)
nu heb ik dus als berekenings formule: Vnatronloog * [OH-] * MWCaCO3.
Is deze formule juist?
sorry voor de opmaak: link in de op werkt niet
De vraag is: leid zelf een berekeningsformule af voor het berekenen van de massa die er aan calciumcarbonaat moet worden ingewogen voor een natronloogverbruik van 25 ml ( concentratie NaOH = 0,1 mol/l)
nu heb ik dus als berekenings formule: Vnatronloog * [OH-] * MWCaCO3.
Is deze formule juist?


Het is sowieso van belang om eerst uit te schrijven welke reactie er gaat plaatsvinden. Het is mij niet duidelijk wat calciumcarbonaat met natronloog moet gaan doen. Volgens mij reageren die twee namelijk niet met elkaar. Weet je zeker dat je stofnamen correct hebt overgenomen?quote:Op donderdag 13 oktober 2011 13:29 schreef daantje1044 het volgende:
ff een vraag ter controle of ik het nu goed doe met die berekeningsformule.
sorry voor de opmaak: link in de op werkt niet
De vraag is: leid zelf een berekeningsformule af voor het berekenen van de massa die er aan calciumcarbonaat moet worden ingewogen voor een natronloogverbruik van 25 ml ( concentratie NaOH = 0,1 mol/l)
nu heb ik dus als berekenings formule: Vnatronloog * [OH-] * MWCaCO3.
Is deze formule juist?
Je formule is correct voor een reactie met molverhouding 1:1, maar geeft de massa van CaCO3 in mg. Wil je dit in grammen hebben, dan moet je nog delen door 1000.


het gaat om een terugtritatie met natronloog sorry. CaCo3 wordt eerst opgelost in een overmaat zuur :
CaCo3 + 2H+ -------> Ca + H2CO3
H2CO3 ---------> H2O + CO2
daarna wordt het CO2 uitgekookt. Omdat er meer zuur wordt toegevoegd dan nodig is, kan het restant H+ teruggetriteerd worden met een natriumhydroxide- oplossing.
CaCo3 + 2H+ -------> Ca + H2CO3
H2CO3 ---------> H2O + CO2
daarna wordt het CO2 uitgekookt. Omdat er meer zuur wordt toegevoegd dan nodig is, kan het restant H+ teruggetriteerd worden met een natriumhydroxide- oplossing.


Dat verklaart een hoop! Dit betekent dat ook bekend moet zijn hoeveel zuur je toevoegt, anders kun je niet bepalen hoeveel CaCO3 je moet toevoegen.quote:Op donderdag 13 oktober 2011 14:26 schreef daantje1044 het volgende:
het gaat om een terugtritatie met natronloog sorry. CaCo3 wordt eerst opgelost in een overmaat zuur :
CaCo3 + 2H+ -------> Ca + H2CO3
H2CO3 ---------> H2O + CO2
daarna wordt het CO2 uitgekookt. Omdat er meer zuur wordt toegevoegd dan nodig is, kan het restant H+ teruggetriteerd worden met een natriumhydroxide- oplossing.
Uit de eerste formule (CaCO3 + 2H+ -------> Ca2+ + H2CO3) blijkt dat het calciumcarbonaat en zuur in een verhouding 1:2 reageren. Natronloog en zuur reageren in een verhouding 1:1.
Je moet dan de volgende stappen zetten om de formule te krijgen:
• bepaal hoeveel mol zuur wordt toegevoegd aan de hand van het toegevoegde volume zuur en de concentratie van het zuur
• daar trek je het aantal mol zuur vanaf dat wegreageert met natronloog; berekenen aan de hand van het toegevoegde volume natronloog en de concentratie ervan
• dat geeft het aantal mol zuur dat reageert met calciumcarbonaat
• vermenigvuldigen met 0,5 (of delen door 2) geeft het aantal mol CaCO3 dat heeft gereageerd
• vermenigvuldigd met de molmassa geeft de massa van het weggereageerde CaCO3
SPOILER: antwoord in deze spoilerOm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


ok dank je wel! weer wat wijzer geworden!
Nog 1 vraag uit nieuwsgierigheid. Waarom kook je de CO2 uit? Gaat de titratie anders niet werken?
Nog 1 vraag uit nieuwsgierigheid. Waarom kook je de CO2 uit? Gaat de titratie anders niet werken?


CO2 kan reageren met OH-, dat geeft HCO3-. Zonder uitkoken zou de titratie daarom niet meer kloppen.quote:Op donderdag 13 oktober 2011 17:32 schreef daantje1044 het volgende:
ok dank je wel! weer wat wijzer geworden!
Nog 1 vraag uit nieuwsgierigheid. Waarom kook je de CO2 uit? Gaat de titratie anders niet werken?


Sorry, alweer een vraag, begrijp het gewoon echt niet:
Moet een practicum voorbereiden voor het opnemen van titratiecurven, berekenen van de equivalentiepunten en het bepalen van de omslaggebieden van een aantal zuur-base indicatoren.
Het practicum voer ik uit met natriumhydroxide oplossing en de volgende stoffen: zoutzuur, azijnzuur en fosforzuur.
Nu moet ik berekenen hoeveel ml NaOH (aq) er theoretisch nodig is om de eindpunten te bereiken. Ik heb dus geen idee hoe ik dat moet berekenen.
De gegevens die ik heb. ( ik ga uit van de reactie met zoutzuur):
Ik moet 25 ml zoutzuuroplossing gebruiken. concentratie NaOH is 0,1 mol/l.
En de pH meter wordt gekalibreerd met buffer pH= 7,00 en pH = 4,00.
reactievergelijking:
NaOH + HCL -----> NaCl + H2O
Kan iemand me uitleggen hoe ik het aantal ml NaOH moet berekenen? Zit er al uren naar te staren, maar kom er echt niet uit.
Moet een practicum voorbereiden voor het opnemen van titratiecurven, berekenen van de equivalentiepunten en het bepalen van de omslaggebieden van een aantal zuur-base indicatoren.
Het practicum voer ik uit met natriumhydroxide oplossing en de volgende stoffen: zoutzuur, azijnzuur en fosforzuur.
Nu moet ik berekenen hoeveel ml NaOH (aq) er theoretisch nodig is om de eindpunten te bereiken. Ik heb dus geen idee hoe ik dat moet berekenen.
De gegevens die ik heb. ( ik ga uit van de reactie met zoutzuur):
Ik moet 25 ml zoutzuuroplossing gebruiken. concentratie NaOH is 0,1 mol/l.
En de pH meter wordt gekalibreerd met buffer pH= 7,00 en pH = 4,00.
reactievergelijking:
NaOH + HCL -----> NaCl + H2O
Kan iemand me uitleggen hoe ik het aantal ml NaOH moet berekenen? Zit er al uren naar te staren, maar kom er echt niet uit.


Weet je niet (ongeveer) de concentratie van de zoutzuuroplossing? Je moet namelijk weten hoeveel mol zoutzuur er is, waaruit je kunt beredeneren hoeveel mol NaOH er nodig is om HCl totaal te neutraliseren.quote:Op maandag 17 oktober 2011 15:33 schreef daantje1044 het volgende:
Sorry, alweer een vraag, begrijp het gewoon echt niet:
Moet een practicum voorbereiden voor het opnemen van titratiecurven, berekenen van de equivalentiepunten en het bepalen van de omslaggebieden van een aantal zuur-base indicatoren.
Het practicum voer ik uit met natriumhydroxide oplossing en de volgende stoffen: zoutzuur, azijnzuur en fosforzuur.
Nu moet ik berekenen hoeveel ml NaOH (aq) er theoretisch nodig is om de eindpunten te bereiken. Ik heb dus geen idee hoe ik dat moet berekenen.
De gegevens die ik heb. ( ik ga uit van de reactie met zoutzuur):
Ik moet 25 ml zoutzuuroplossing gebruiken. concentratie NaOH is 0,1 mol/l.
En de pH meter wordt gekalibreerd met buffer pH= 7,00 en pH = 4,00.
reactievergelijking:
NaOH + HCL -----> NaCl + H2O
Kan iemand me uitleggen hoe ik het aantal ml NaOH moet berekenen? Zit er al uren naar te staren, maar kom er echt niet uit.


Als je dan 25 ml van die oplossing pakt, hoeveel mol HCl heb je dan?quote:Op maandag 17 oktober 2011 23:51 schreef daantje1044 het volgende:
concentratie zoutzuur is 0,1 mol/l
SPOILER: antwoordOm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.En als je weet dat HCl volledig dissocieert in water, dat wil zeggen het splitst zich in H+ en Cl-, hoeveel mol H+ heb je dan in oplossing?SPOILER: antwoordOm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Hoeveel mol OH- heb je dan nodig om het zuur te neutraliseren?SPOILER: antwoordOm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.En hoeveel ml 0,1 M natronloog heb je dan nodig?SPOILER: antwoordOm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.
 Hoi,
Hoi,
Ik heb een vraag over een portfolio. Nou is het zo dat ik er nog nooit één gemaakt had. Maar mijn moeder maakt wel een portfolio tijdens haar inburgingscursus voor school.
Bij haar portfolio zie ik een blz. met persoonlijke gegevens. Dus naam, adres, woonplaats, hobby's en etc. In mijn ogen lijkt die blz. op een C.V.
Nu maak ik een portfolio van een vak voor school. De opdrachten die ik heb gemaakt zitten in mijn portfolio, maar er wordt niet gevraagd dat ik zo'n blz. maak met persoonlijke gegevens als een soort van C.V.
Mijn vraag is: Moet ik die persoonlijke gegevens na de inhoudsopgave er niet in zetten, omdat het niet wordt gevraagd.
Of moet ik mijn persoonlijke gegevens er wel in zetten zelfs als dat niet wordt gevraagd, omdat het standaard in een portfolio hoort. Alvast bedankt voor uw antwoord!
Groet,
superky
 wie kan deze vraag oplossen, en uitleggen?
wie kan deze vraag oplossen, en uitleggen?
Aspirin (acetylsalicylic acid, C9H8O4 ) is a weak monoprotic acid. To determine its acid-dissociation constant, a student dissolved 2.00 of aspirin in 0.600 L of water and measured thePH . What was the Ka value calculated by the student if the PH of the solution was 2.61?
bij voorbaat dank.
 'Voor de jaren na 2007 verwacht de regering van dit land een verbetering van het saldo van de kapitaalrekening.'
'Voor de jaren na 2007 verwacht de regering van dit land een verbetering van het saldo van de kapitaalrekening.'
De kapitaalrekening had een overschot van 18.4 miljard.
'Zal in de toekomst het saldo van de inkomensrekening van dit land daardoor positief of negatief worden beinvloed? Verklaar het antwoord.'
Het antwoord is: Negatief. De toevloed van kapitaal via de kapitaalrekening leidt in de toekomst tot rentebetalingen en dividendafdrachten aan het buitenland.
Maar dit klopt toch niet? Een verbetering van het saldo van de kapitaalrekening betekent toch juist dat deze overheid haar overschot op de kapitaalrekening van 18.4 miljard juist nog hoger wil maken? Waardoor er nog meer geld naar het buitenland gaat, waar WIJ juist winst en rente over ontvangen?
 Je moet altijd eerst beginnen met het opstellen van de reactievergelijking:quote:
Je moet altijd eerst beginnen met het opstellen van de reactievergelijking:quote:Op zaterdag 22 oktober 2011 18:16 schreef jouwkeuze het volgende:
wie kan deze vraag oplossen, en uitleggen?
Aspirin (acetylsalicylic acid, C9H8O4 ) is a weak monoprotic acid. To determine its acid-dissociation constant, a student dissolved 2.00 of aspirin in 0.600 L of water and measured thePH . What was the Ka value calculated by the student if the PH of the solution was 2.61?
bij voorbaat dank.
HA + H2O <=> H3O+ + A-
Hierin is aspirine weergegeven als HA en zijn geconjugeerde base als A-.
Vervolgens stel je de bijbehorende evenwichtsvoorwaarde op:
Ka = [H3O+][A-]/[HA]
Om Ka te kunnen berekenen, moet je alle concentraties die genoemd worden in de evenwichtsvoorwaarde kennen.
De pH is bepaald op 2,61, waaruit we kunnen afleiden dat [H3O+] = 10pH = 10-2,61 = 0,00245 mol/l
[A-] = [H3O+] = 0,00245 mol/l, want beide ionen worden in een 1:1-verhouding gevormd.
Dan hoeven we alleen nog de concentratie van het ongedissocieerde zuur te bepalen: [HA].
Dat kun je doen door eerst te bepalen hoeveel mol aspirine er is opgelost en die te verminderen met [A-].
De opgave geeft geen eenheid van de opgeloste massa aspirine, maar ik ga even uit van 2,00 g. 2,00 g aspirine komt overeen met 2,00/180,16 = 0,0111 mol. Dat is opgelost in 0,600 l water, wat betekent dat de initiële concentratie van aspirine gelijk was aan 0,0111/0,600 = 0,0185 mol/l. Verminder deze met [A-], dat geeft 0,0185 - 0,00245 = 0,01605 mol/l
Invullen van de concentraties in de evenwichtsvoorwaarde geeft Ka = (0,00245)2/0,01605 = 3,75 * 10-4 mol/l
 @ supersky: vraag het eens na bij je leraar. Die waardeert het waarschijnlijk dat je het zo graag goed wil doen, dus wellicht vertelt hij het wel.
@ supersky: vraag het eens na bij je leraar. Die waardeert het waarschijnlijk dat je het zo graag goed wil doen, dus wellicht vertelt hij het wel.
Als hij het niet verklapt zou ik het er wel bij doen maar niet te uitgebreid.
 Heren , une question, gelieve mij te helpen, ik kom er zelf niet uit (al veel geprobeerd).
Heren , une question, gelieve mij te helpen, ik kom er zelf niet uit (al veel geprobeerd).
De opdracht met vragen:
Mijn poging op vraag 1 (weet niet of het klopt) (en heb v niet kunnen uitrekenen) (p.s. niets met integralen a.u.b. ):
Mijn poging op vraag 2:

 voor jouw eerste opdracht heb je T = m*g (20*9.8), dit is alleen waar als blok b stil zou staan(als de kabel massaloos is), en dat is niet zoquote:
voor jouw eerste opdracht heb je T = m*g (20*9.8), dit is alleen waar als blok b stil zou staan(als de kabel massaloos is), en dat is niet zoquote:Op zondag 30 oktober 2011 20:08 schreef alicarpali het volgende:
Heren , une question, gelieve mij te helpen, ik kom er zelf niet uit (al veel geprobeerd).
De opdracht met vragen:
[ afbeelding ]
Mijn poging op vraag 1 (weet niet of het klopt) (en heb v niet kunnen uitrekenen) (p.s. niets met integralen a.u.b. ):
[ afbeelding ]
Mijn poging op vraag 2:
[ afbeelding ]
denk ik

 http://i.imgur.com/GveY7.jpg zo moet ie denk ikquote:
http://i.imgur.com/GveY7.jpg zo moet ie denk ikquote:Op zondag 30 oktober 2011 20:08 schreef alicarpali het volgende:
Heren , une question, gelieve mij te helpen, ik kom er zelf niet uit (al veel geprobeerd).
De opdracht met vragen:
[ afbeelding ]
Mijn poging op vraag 1 (weet niet of het klopt) (en heb v niet kunnen uitrekenen) (p.s. niets met integralen a.u.b. ):
[ afbeelding ]
Mijn poging op vraag 2:
[ afbeelding ]
 Hallo,
Hallo,
Zou iemand mij nadere uitleg wilen geven over de volgende functie's bij kansberekening?
De NCR funtctie
Fakkeltijd
BIj wat voor soort vraag moet ik welke functie gebruiken, ik haal het telkens door elkaar heen en in het boek staat het niet precies beschreven.''Ja die meneer heeft kaal haar.''
 Het is faculteit; fakkeltijd is heel wat andersquote:
Het is faculteit; fakkeltijd is heel wat andersquote:Op zondag 6 november 2011 12:28 schreef Mierenneuker. het volgende:
Hallo,
Zou iemand mij nadere uitleg wilen geven over de volgende functie's bij kansberekening?
De NCR funtctie
Fakkeltijd
BIj wat voor soort vraag moet ik welke functie gebruiken, ik haal het telkens door elkaar heen en in het boek staat het niet precies beschreven.
De nCr-functie gebruik je voor het berekenen van combinaties (volgorde níet van belang).
Stel dat je uit een groep van 5 mensen er 2 mag kiezen; hoeveel verschillende keuzes (combinaties) kun je maken? Het maakt hier niet uit of je eerst A en dan B kiest, uiteindelijk kies je beide personen. Je maakt hier gebruik van nCr (combinaties). De oplossing is hier 5 nCr 2 oftewel 10 keuzes.
De nPr-functie gebruik je voor permutaties (volgorde wél van belang).
Stel dat je uit een groep van 5 mensen een voorzitter en een notulist moet kiezen; hoeveel verschillende keuzes (permutaties) kun je maken? De volgorde is van belang, want als je A als voorzitter kiest dan is hij geen notulist (want dat is B). Je maakt hier gebruik van nPr (permutaties). De oplossing is hier 5 nPr 2 oftewel 20 mogelijkheden.
Faculteit gebruik je voor het berekenen ervan:
waarin k het aantal elementen uit de verzamling n is.
 Bedankt voor je reactie, nu ga ik al met een aardig beter gevoel mijn tentamen wisk. tegemoet.quote:
Bedankt voor je reactie, nu ga ik al met een aardig beter gevoel mijn tentamen wisk. tegemoet.quote:Op zondag 6 november 2011 13:25 schreef zoem het volgende:
[..]
Het is faculteit; fakkeltijd is heel wat anders
De nCr-functie gebruik je voor het berekenen van combinaties (volgorde níet van belang).
Stel dat je uit een groep van 5 mensen er 2 mag kiezen; hoeveel verschillende keuzes (combinaties) kun je maken? Het maakt hier niet uit of je eerst A en dan B kiest, uiteindelijk kies je beide personen. Je maakt hier gebruik van nCr (combinaties). De oplossing is hier 5 nCr 2 oftewel 10 keuzes.
De nPr-functie gebruik je voor permutaties (volgorde wél van belang).
Stel dat je uit een groep van 5 mensen een voorzitter en een notulist moet kiezen; hoeveel verschillende keuzes (permutaties) kun je maken? De volgorde is van belang, want als je A als voorzitter kiest dan is hij geen notulist (want dat is B). Je maakt hier gebruik van nPr (permutaties). De oplossing is hier 5 nPr 2 oftewel 20 mogelijkheden.
Faculteit gebruik je voor het berekenen ervan:
waarin k het aantal elementen uit de verzamling n is.''Ja die meneer heeft kaal haar.''
 Ik moet voor natuurkunde een formule invullen waarin de dichtheid van lucht voorkomt. Hoe moet ik deze dichtheid weten?
Ik moet voor natuurkunde een formule invullen waarin de dichtheid van lucht voorkomt. Hoe moet ik deze dichtheid weten?
Het antwoord is trouwens 1,293 kgm^-3 maar hoe kom je hieraan? :S
[ Bericht 24% gewijzigd door #ANONIEM op 07-11-2011 16:55:54 ]
 Als de dichtheid van lucht niet gegeven is dan kun je uitgaan van ISA condities (International Standard Atmosphere). Dan is de luchtdichtheid:quote:
Als de dichtheid van lucht niet gegeven is dan kun je uitgaan van ISA condities (International Standard Atmosphere). Dan is de luchtdichtheid:quote:Op maandag 7 november 2011 16:54 schreef magneetstrip het volgende:
Ik moet voor natuurkunde een formule invullen waarin de dichtheid van lucht voorkomt. Hoe moet ik deze dichtheid weten?
Het antwoord is trouwens 1,293 kgm^-3 maar hoe kom je hieraan? :S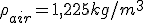

 Dit is bij 0 graden Celsius. Is dit niet makkelijk te vinden in een BINAS?quote:
Dit is bij 0 graden Celsius. Is dit niet makkelijk te vinden in een BINAS?quote:Op maandag 7 november 2011 16:54 schreef magneetstrip het volgende:
Ik moet voor natuurkunde een formule invullen waarin de dichtheid van lucht voorkomt. Hoe moet ik deze dichtheid weten?
Het antwoord is trouwens 1,293 kgm^-3 maar hoe kom je hieraan? :S
 Jongens, als er wordt gevraagd hoeveel gram koolstofatomen er zitten in 100 gram C6H12O6 (glucose)
Jongens, als er wordt gevraagd hoeveel gram koolstofatomen er zitten in 100 gram C6H12O6 (glucose)
Hoe pak ik dat aan? Ik ben bekend met molverhoudingen en omrekenen naar gram in reactievergelijkingen.
Is het goed als ik:
- Eerst de molmassa glucose uitreken
- 100 gram deel door de molmassa = aantal mol
- aantal mol delen door (6+12+6) en daarna vermenigvuldig met 6? (want je hebt 6 koolstofatomen)?
- Ten slotte aantal mol vermenigvuldig met de molmassa van koolstof?
Zo'n vraag zat in de sk toets maar dan een stuk ingewikkelder. Het deel wat ik niet begreep was dit hierboven. Ik denk dat punt 3 niet goed is.
[ Bericht 12% gewijzigd door BeyondTheGreen op 10-11-2011 14:32:16 ]Unbowed, Unbent, Unbroken.
 C = 12g/mol
C = 12g/mol
H = 1g/mol
O = 16g/mol
molmassa C6H12O6 = 6*12+12*1+6*16 = 180 g/mol
Je hebt 100 gram C6H12O6, dus 100/180 = 0.555 mol.
Er is 6*12 = 72g/mol aan koolstofatomen aanwezig.
Dus 0.555 mol * 72 g/mol = 40g.
Lijkt me vrij rechttoe rechtaan

 Danku.quote:
Danku.quote:Op donderdag 10 november 2011 14:43 schreef zoem het volgende:
C = 12g/mol
H = 1g/mol
O = 16g/mol
molmassa C6H12O6 = 6*12+12*1+6*16 = 180 g/mol
Je hebt 100 gram C6H12O6, dus 100/180 = 0.555 mol.
Er is 6*12 = 72g/mol aan koolstofatomen aanwezig.
Dus 0.555 mol * 72 g/mol = 40g.
Lijkt me vrij rechttoe rechtaan
Het is ook niet zo moeilijk, maar als je Sprinthavo doet en nooit eerder scheikunde hebt gehad gaat het wel allemaal erg snel.Unbowed, Unbent, Unbroken.
 OPGELOST
OPGELOST
Een halve glazen bol is bedekt met een spiegelende zilverlaag aan de gekromde kant van het
oppervlak. Binnenin de bol, op de centrale as, bevindt zich een kleine luchtbel op 50.0 mm afstand
van het platte oppervlak. De kromtestraal R van de halve bol is gelijk aan 75.0 mm en het glas van
de bol heeft een brekingsindex n = 1.60. (zie figuur). We kijken langs de as in het vlakke oppervlak
en we zien twee afbeeldingen van de luchtbel.
http://imageshack.us/photo/my-images/141/optica.png/ (copy/paste deze link)
a) Verklaar hoe de twee afbeeldingen van de luchtbel tot stand komen
OPGELOST
[ Bericht 11% gewijzigd door Anoonumos op 12-11-2011 23:26:46 ]
 Hoi,
Hoi,
Mijn vorige vragen zijn al beantwoord en opgelost, dus nogmaals bedankt. Maar ik heb nog een vraagje:
Op welke tijden kijken kinderen van 9 t/m 12 jaar naar de televisie?
Ik had al op CBS Statline en SKO gekeken, maar dan kon ik niks vinden. Alvast bedankt voor uw antwoord!
Groet,
superky
 Ik ben eigenlijk wel benieuwd naar het antwoord. Nav jouw vraag heb ik het proberen op te lossen, maar ik kwam er ook niet uit. Optica is één van de weinige natuurkunde-onderdelen die ik niet in mijn opleiding gehad heb.quote:
Ik ben eigenlijk wel benieuwd naar het antwoord. Nav jouw vraag heb ik het proberen op te lossen, maar ik kwam er ook niet uit. Optica is één van de weinige natuurkunde-onderdelen die ik niet in mijn opleiding gehad heb.quote:
 Uitwerking komt komende week online, dus die zal ik hier wel posten. Het idee was dat het voorwerp dichterbij lijkt dan hij daadwerkelijk is, net zoals een zwembad minder diep lijkt als je van boven kijkt. Het andere beeld ontstaat door de spiegel.
Uitwerking komt komende week online, dus die zal ik hier wel posten. Het idee was dat het voorwerp dichterbij lijkt dan hij daadwerkelijk is, net zoals een zwembad minder diep lijkt als je van boven kijkt. Het andere beeld ontstaat door de spiegel.
 Ik was wel al zo ver dat ik de beeldafstand had uitgerekend, en die lag inderdaad net iets vóór het voorwerp zelf. Ik kwam uit op 16.67mm voor het object, of 41.67mm vanaf de lens/bol. Maar ja dat is met middelbare-schooloptica
Ik was wel al zo ver dat ik de beeldafstand had uitgerekend, en die lag inderdaad net iets vóór het voorwerp zelf. Ik kwam uit op 16.67mm voor het object, of 41.67mm vanaf de lens/bol. Maar ja dat is met middelbare-schooloptica
Forum Opties Forumhop: Hop naar:



 rC+sD
rC+sD