SES School, Studie en Onderwijs
Wiskunde in de brugklas, Frans voor het examen of een studie Personeel en Arbeid? Moeilijke formulieren van DUO? Iets weten over studiefinanciering of studentenverenigingen? Dit is het forum voor leerkrachten, scholieren en studenten, van brugklas tot uni



Vorige deel: [Bèta overig] 'Huiswerk- en vragentopic'.
Post hier weer al je vragen, passies, trauma's en andere dingen die je uit je slaap houden met betrekking tot de vakken:
• Natuurkunde
• Informatica
• Scheikunde
• Biologie
• Algemene Natuurwetenschappen
• ... en alles wat verder in de richting komt.
Van MBO tot WO, hier is het topic waar je een antwoord kunt krijgen op je vragen.
Opmaak: met de [tex]-tag kun je Latexcode in je post opnemen om formules er mooier uit te laten zien (uitleg).
[ Bericht 11% gewijzigd door GlowMouse op 02-06-2012 11:21:02 ]
Post hier weer al je vragen, passies, trauma's en andere dingen die je uit je slaap houden met betrekking tot de vakken:
• Natuurkunde
• Informatica
• Scheikunde
• Biologie
• Algemene Natuurwetenschappen
• ... en alles wat verder in de richting komt.
Van MBO tot WO, hier is het topic waar je een antwoord kunt krijgen op je vragen.
Opmaak: met de [tex]-tag kun je Latexcode in je post opnemen om formules er mooier uit te laten zien (uitleg).
[ Bericht 11% gewijzigd door GlowMouse op 02-06-2012 11:21:02 ]


Tja, Ofresca, als je dit kunt bedenken dan had je de opgave niet hoeven posten. En trouwens, aangezien A en A1 niet bekend zijn, is de opgave dan nog steeds niet op te lossen. De opgave deugt gewoon niet.


Ik heb de antwoorden, wil niet zeggen dat ik ze ook zelf kan bedenken.quote:Op woensdag 30 mei 2012 17:33 schreef Riparius het volgende:
Tja, Ofresca, als je dit kunt bedenken dan had je de opgave niet hoeven posten. En trouwens, aangezien A en A1 niet bekend zijn, is de opgave dan nog steeds niet op te lossen. De opgave deugt gewoon niet.
A_1 kun je uitdrukken in termen van A, Waarna je door A kunt delen en beide termen dus wegvallen. Ik miste waarom je phi_M,in aan phi_M,uit gelijk mocht stellen. En dát begrijp ik nu. Het antwoord had ik al.


Goed, maar hoe druk je A1 uit in A als je hier niets over weet? Dat is niet uit de opgave af te leiden, of je houdt iets achter.quote:Op woensdag 30 mei 2012 17:37 schreef Ofresca het volgende:
[..]
Ik heb de antwoorden, wil niet zeggen dat ik ze ook zelf kan bedenken.
A_1 kun je uitdrukken in termen van A, Waarna je door A kunt delen en beide termen dus wegvallen. Ik miste waarom je phi_M,in aan phi_M,uit gelijk mocht stellen. En dát begrijp ik nu. Het antwoord had ik al.


Omdat je weet dat op t = t_1, h = 0 geldt, dus moet je formule voor hoogte (met afvoer open, kraan dicht) daar 0 zijn. Dat is het geval wanneer A_1 = (2 * H^(1/2) * A) / (sqrt(29) * t_1). Waarmee je A_1 dus in (onder andere) A hebt uitgedrukt.quote:Op woensdag 30 mei 2012 17:41 schreef Riparius het volgende:
[..]
Goed, maar hoe druk je A1 uit in A als je hier niets over weet? Dat is niet uit de opgave af te leiden, of je houdt iets achter.


Goed, maar je hebt in je formules de waarden van t_0 en t_1 omgewisseld, want met de formules die je geeft kom ik niet op 32 cm uit, als ik t_0 en t_1 echter met elkaar verwissel wel, kijk maar.quote:Op woensdag 30 mei 2012 17:49 schreef Ofresca het volgende:
[..]
Omdat je weet dat op t = t_1, h = 0 geldt, dus moet je formule voor hoogte (met afvoer open, kraan dicht) daar 0 zijn. Dat is het geval wanneer A_1 = (2 * H^(1/2) * A) / (sqrt(29) * t_1). Waarmee je A_1 dus in (onder andere) A hebt uitgedrukt.


Oh, ja klopt. Ik zie het.quote:Op woensdag 30 mei 2012 18:43 schreef Riparius het volgende:
[..]
Goed, maar je hebt in je formules de waarden van t_0 en t_1 omgewisseld, want met de formules die je geeft kom ik niet op 32 cm uit, als ik t_0 en t_1 echter met elkaar verwissel wel, kijk maar.


Als je ionen moet benoemen he, en je hebt bijvoorbeeld Au³+, heet het dan gewoon goud-ion?
En klopt het ook dat Mn²+ het mangaan(II)-ion is?
Weet ook iemand wat de naam is van K2S, FeN en SnI4?
En klopt het ook dat Mn²+ het mangaan(II)-ion is?
Weet ook iemand wat de naam is van K2S, FeN en SnI4?


Ja dat mag je ionen noemen. Je mag eventueel de lading tussen haakjes zetten.quote:Op woensdag 30 mei 2012 19:42 schreef Wicky15 het volgende:
Als je ionen moet benoemen he, en je hebt bijvoorbeeld Au³+, heet het dan gewoon goud-ion?
En klopt het ook dat Mn²+ het mangaan(II)-ion is?
quote:Weet ook iemand wat de naam is van K2S, FeN en SnI4?
quote:Op woensdag 30 mei 2012 19:13 schreef zoem het volgende:
[..]
Kaliumsulfide, ijzer(III)nitride en tin(tetra/IV)jodide?


Nogmaals bedankt, alleen waarom is het ||| bij ijzernitride? Dat snap ik dus niet goed.quote:Op woensdag 30 mei 2012 19:51 schreef zoem het volgende:
[..]
Ja dat mag je ionen noemen. Je mag eventueel de lading tussen haakjes zetten.
[..]
[..]


Het ijzerion kan zowel 2+ of 3+ zijn. Aangezien het stikstofion een lading van -3 heeft zal het ijzerion een lading van 3+ krijgen en dus schrijf je (III).quote:Op woensdag 30 mei 2012 19:55 schreef Wicky15 het volgende:
[..]
Nogmaals bedankt, alleen waarom is het ||| bij ijzernitride? Dat snap ik dus niet goed.
Zie hier voor een overzicht.


Kan iemand mij even helpen met mijn natuurkunde vraag?
De vraag:
Een vloeistof bevat 24Na; 1cm3 ervan heeft een activiteit van 950 Bq en wordt ingespoten in het bloed van een patient. Als 29,6 uur later wordt gemeten blijkt de activiteit van 1 cm3 bloed 24 deeltjes per 10 min te zijn.
Welke activiteit zou in 1 cm3 bloed direct na het inspuiten gemeten zijn?
-----
Wat ik dus dacht:
Halveringstijd van 24Na is 14,8 u, dus na 29,6 uur is dit (.5)2 en is er nog 25% van de activiteit over. 24 * .25 = 6 deeltjes per 10 minuten = 0.6 deeltjes per minuut = 0.01 deeltjes per seconde, wat dus 0.01 Bq is.
Alleen het antwoordmodel zegt dit:
Je zou dan dus 22·24 deeltjes in 10 min gemeten hebben, dus 0,16 Bq
En ik snap niet waar ze die 22 vandaan halen.
De vraag:
Een vloeistof bevat 24Na; 1cm3 ervan heeft een activiteit van 950 Bq en wordt ingespoten in het bloed van een patient. Als 29,6 uur later wordt gemeten blijkt de activiteit van 1 cm3 bloed 24 deeltjes per 10 min te zijn.
Welke activiteit zou in 1 cm3 bloed direct na het inspuiten gemeten zijn?
-----
Wat ik dus dacht:
Halveringstijd van 24Na is 14,8 u, dus na 29,6 uur is dit (.5)2 en is er nog 25% van de activiteit over. 24 * .25 = 6 deeltjes per 10 minuten = 0.6 deeltjes per minuut = 0.01 deeltjes per seconde, wat dus 0.01 Bq is.
Alleen het antwoordmodel zegt dit:
Je zou dan dus 22·24 deeltjes in 10 min gemeten hebben, dus 0,16 Bq
En ik snap niet waar ze die 22 vandaan halen.


Je doet het achterstevoren, je moet juist terugrekenen. Lees nog maar eens goed wat er gevraagd wordt en wat jij feitelijk uitrekent.quote:Op donderdag 31 mei 2012 21:46 schreef Miraculously het volgende:
Kan iemand mij even helpen met mijn natuurkunde vraag?
De vraag:
Een vloeistof bevat 24Na; 1cm3 ervan heeft een activiteit van 950 Bq en wordt ingespoten in het bloed van een patient. Als 29,6 uur later wordt gemeten blijkt de activiteit van 1 cm3 bloed 24 deeltjes per 10 min te zijn.
Welke activiteit zou in 1 cm3 bloed direct na het inspuiten gemeten zijn?
-----
Wat ik dus dacht:
Halveringstijd van 24Na is 14,8 u, dus na 29,6 uur is dit (.5)2 en is er nog 25% van de activiteit over. 24 * .25 = 6 deeltjes per 10 minuten = 0.6 deeltjes per minuut = 0.01 deeltjes per seconde, wat dus 0.01 Bq is.
Alleen het antwoordmodel zegt dit:
Je zou dan dus 22·24 deeltjes in 10 min gemeten hebben, dus 0,16 Bq
En ik snap niet waar ze die 22 vandaan halen.


Een verticaal geplaatste veer is vastgezet op de grond. Een blokje van 0.400 kg wordt op de bovenkant van de veer geplaatst. De veer begint te trillen. De veerconstante is 112N/m Het blokje zit niet vast op de veer.
a) Bepaal de frequentie.
b) bepaal de amplitude waarbij het blokje geen contact meer maakt met de veer.
de frequentie heb ik al bepaald dat is 2,66 Hz. Maar hoe beantwoord ik nu vraag b?
a) Bepaal de frequentie.
b) bepaal de amplitude waarbij het blokje geen contact meer maakt met de veer.
de frequentie heb ik al bepaald dat is 2,66 Hz. Maar hoe beantwoord ik nu vraag b?
AJAX AMSTERDAM!


Bereken de amplitude waarbij de krachten niet meer gelijk zijn, dwz dat de kracht omhoog ten gevolge van een uitstrekkende veer groter wordt dan m*g.quote:Op zondag 10 juni 2012 16:05 schreef bloodysunday het volgende:
Een verticaal geplaatste veer is vastgezet op de grond. Een blokje van 0.400 kg wordt op de bovenkant van de veer geplaatst. De veer begint te trillen. De veerconstante is 112N/m Het blokje zit niet vast op de veer.
a) Bepaal de frequentie.
b) bepaal de amplitude waarbij het blokje geen contact meer maakt met de veer.
de frequentie heb ik al bepaald dat is 2,66 Hz. Maar hoe beantwoord ik nu vraag b?
M'n gutfeeling zegt dat je dit het beste met de wet van behoud van energie op kunt lossen.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Bij een gegeven amplitude kun je ook de versnelling als functie van de tijd bepalen, dat is immers de tweede afgeleide van de positie naar de tijd. Het blokje komt 'los' als de maximale versnelling groter wordt dan de valversnelling van de zwaartekracht.quote:Op zondag 10 juni 2012 16:05 schreef bloodysunday het volgende:
Een verticaal geplaatste veer is vastgezet op de grond. Een blokje van 0.400 kg wordt op de bovenkant van de veer geplaatst. De veer begint te trillen. De veerconstante is 112N/m Het blokje zit niet vast op de veer.
a) Bepaal de frequentie.
b) bepaal de amplitude waarbij het blokje geen contact meer maakt met de veer.
de frequentie heb ik al bepaald dat is 2,66 Hz. Maar hoe beantwoord ik nu vraag b?


Ik heb (wederom) een vraagje over meetkunde:
De volgende koordenvierhoek is gegeven (tegen de klok in met punt A - D). De bogen BC, CD en DA zijn in de verhoudingen 1:3:5. De lijn ligt op het middelpunt van de cirkel en bevat dus punt M.
Nu is het de bedoeling dat ik de hoeken uitrekenen van de koordenvierhoek. Maar ik kom niet verder aangezien ik niet weet waar ik moet beginnen/ik heb geen referentie.
De volgende koordenvierhoek is gegeven (tegen de klok in met punt A - D). De bogen BC, CD en DA zijn in de verhoudingen 1:3:5. De lijn ligt op het middelpunt van de cirkel en bevat dus punt M.
Nu is het de bedoeling dat ik de hoeken uitrekenen van de koordenvierhoek. Maar ik kom niet verder aangezien ik niet weet waar ik moet beginnen/ik heb geen referentie.


Dit is niet het wiskundetopic, dus post het even daar. En je moet wel nauwkeurig formuleren, je bedoelt kennelijk dat zijde AB van je koordenvierhoek een middellijn is van de cirkel.quote:Op zondag 10 juni 2012 16:33 schreef Aardappel2610 het volgende:
Ik heb (wederom) een vraagje over meetkunde:
De volgende koordenvierhoek is gegeven (tegen de klok in met punt A - D). De bogen BC, CD en DA zijn in de verhoudingen 1:3:5. De lijn ligt op het middelpunt van de cirkel en bevat dus punt M.
[ afbeelding ]
Nu is het de bedoeling dat ik de hoeken uitrekenen van de koordenvierhoek. Maar ik kom niet verder aangezien ik niet weet waar ik moet beginnen/ik heb geen referentie.


3.12. Een massa van 2 kg wordt in een verticaal vlak met een constante hoeksnelheid rondgeslingerd aan het eind van een koord. De straal van de cirkel is 0,5 m en de massa maakt 1 omwenteling per seconde.
De maximale spankracht in het koord bedraagt ongeveer:
a. 80 N
b. 60 N
c. 40 N
d. 20 N
e. 10 N
Ik heb de omtrek berekend die is ongeveer 1,6 m. De snelheid is dus 1,6 m/s aangezien hij 1 omwenteling per seconde maakt. Maar hoe bereken ik nu die spankracht?
Er is zwaartekracht dus iets met de formule F=mg en omdat het een draaibeweging is dacht ik Fmpz = mv^2/r maar ik kom dan niet op het juiste antwoord. Wie kan me helpen?
De maximale spankracht in het koord bedraagt ongeveer:
a. 80 N
b. 60 N
c. 40 N
d. 20 N
e. 10 N
Ik heb de omtrek berekend die is ongeveer 1,6 m. De snelheid is dus 1,6 m/s aangezien hij 1 omwenteling per seconde maakt. Maar hoe bereken ik nu die spankracht?
Er is zwaartekracht dus iets met de formule F=mg en omdat het een draaibeweging is dacht ik Fmpz = mv^2/r maar ik kom dan niet op het juiste antwoord. Wie kan me helpen?
AJAX AMSTERDAM!


Heb je het tweede deel van de opgave van gisteren wel begrepen? Je zou moeten kunnen afleiden dat voor de maximale amplitude A waarbij het blokje nog net niet los komt van de veer geldt:quote:Op maandag 11 juni 2012 17:07 schreef bloodysunday het volgende:
3.12. Een massa van 2 kg wordt in een verticaal vlak met een constante hoeksnelheid rondgeslingerd aan het eind van een koord. De straal van de cirkel is 0,5 m en de massa maakt 1 omwenteling per seconde.
De maximale spankracht in het koord bedraagt ongeveer:
a. 80 N
b. 60 N
c. 40 N
d. 20 N
e. 10 N
Ik heb de omtrek berekend die is ongeveer 1,6 m. De snelheid is dus 1,6 m/s aangezien hij 1 omwenteling per seconde maakt. Maar hoe bereken ik nu die spankracht?
Er is zwaartekracht dus iets met de formule F=mg en omdat het een draaibeweging is dacht ik Fmpz = mv^2/r maar ik kom dan niet op het juiste antwoord. Wie kan me helpen?
A = mg/k,
waarbij m de massa is van het blokje, k de veerconstante en g de zwaartekrachtversnelling.
Voor deze opgave vergis je je al bij het berekenen van de omtrek van de cirkel.


Nee, daarom refereer ik aan de opgave van gisteren. Wel goed lezen.quote:Op maandag 11 juni 2012 19:52 schreef bloodysunday het volgende:
Het gaat bij deze opgave toch helemaal niet over een veer?


Kan iemand mij de betalingsbalans van economie uitleggen? Ik snap echt niet waar ik de lopende rekening moet zetten? Wat is dat in godsnaam?
Ik heb echt te veel geslapen bij economie
Ik heb echt te veel geslapen bij economie
#TeamMiley


Ik heb weer eens een vraag.
De opgave is: 17.34 g Kaliumhydroxide wordt opgelost in een maatkolf van 200 ml (oplossing I). oplossing II wordt verkregen door 10.00 ml van oplossing I met water aan te vullen tot 150.0 ml. Tot slot wordt 25.00 ml van oplossing II tot neutraal getitreerd met een 0.138 M HCL-oplossing in water.
De eerste vraag was: Wat is de KOH-concentratie in mol/l in oplossing I?
Die heb ik als volgt uitgerekend:
n= m/M dus n= 17,34 g/ (39.10 + 16.00 + 1.0079) = 0.309 mol
c= n/V dus c= 0.309 mol/ 0.200L = 1.55 mol/L
De volgende vraag kom ik niet uit
Wat is de KOH concentratie in oplossing II?
Zou iemand me daarmee op weg kunnen helpen?
Alvast bedankt.
De opgave is: 17.34 g Kaliumhydroxide wordt opgelost in een maatkolf van 200 ml (oplossing I). oplossing II wordt verkregen door 10.00 ml van oplossing I met water aan te vullen tot 150.0 ml. Tot slot wordt 25.00 ml van oplossing II tot neutraal getitreerd met een 0.138 M HCL-oplossing in water.
De eerste vraag was: Wat is de KOH-concentratie in mol/l in oplossing I?
Die heb ik als volgt uitgerekend:
n= m/M dus n= 17,34 g/ (39.10 + 16.00 + 1.0079) = 0.309 mol
c= n/V dus c= 0.309 mol/ 0.200L = 1.55 mol/L
De volgende vraag kom ik niet uit
Wat is de KOH concentratie in oplossing II?
Zou iemand me daarmee op weg kunnen helpen?
Alvast bedankt.


Je antwoord voor de concentratie van oplossing I is goed.quote:Op woensdag 13 juni 2012 12:44 schreef daantje1044 het volgende:
Ik heb weer eens een vraag.
De opgave is: 17.34 g Kaliumhydroxide wordt opgelost in een maatkolf van 200 ml (oplossing I). oplossing II wordt verkregen door 10.00 ml van oplossing I met water aan te vullen tot 150.0 ml. Tot slot wordt 25.00 ml van oplossing II tot neutraal getitreerd met een 0.138 M HCL-oplossing in water.
De eerste vraag was: Wat is de KOH-concentratie in mol/l in oplossing I?
Die heb ik als volgt uitgerekend:
n= m/M dus n= 17,34 g/ (39.10 + 16.00 + 1.0079) = 0.309 mol
c= n/V dus c= 0.309 mol/ 0.200L = 1.55 mol/L
De volgende vraag kom ik niet uit
Wat is de KOH concentratie in oplossing II?
Zou iemand me daarmee op weg kunnen helpen?
Alvast bedankt.
Om de concentratie van oplossing II te bepalen kun je 2 methoden gebruiken.
1) De simpelste methode is berekenen hoeveel keer er wordt verdund om oplossing II te verkrijgen. Delen van de concentratie van I door de verdunningsgraad geeft het antwoord.
2) Een wat omslachtigere wijze is eerst berekenen hoeveel mol KOH er aanwezig is in 10 ml oplossing van I en dan berekenen wat de concentratie is als dat aantal mol wordt opgelost in 150 ml.
SPOILER: oplossing volgens methode 1Om spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.SPOILER: oplossing volgens methode 2Om spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Bedankt weer! zat al te denken aan oplossing 1, maar dacht dat dat te makkelijk gedacht was van me. Niet zo moeilijk denken dus.
Heb nog een vraag.
Gegeven: oplossing I: 100ml, 0.5 M Pb(NO3)2 (aq) en oplossing II: 75 ml 0.4 M K2SO4.
nu is de vraag hoeveel gram neerslag kan er maximaal ontstaan?
Ik heb al uitgerekend dat oplossing I 100 ml * 0.5 M = 50 mmol Pb(NO3)2 bevat.
Oplossing II bevat 75ml * 0.4 M = 30 mmol K2SO4.
de netto reactie is:
Pb2+ + SO42- ---> PbSO4
de beperkende reactant is SO42-.
Als ik nu 30 mmol * de molaire massa van PbSO4 doe, bereken ik dan hoeveel gram neerslag er kan ontstaan? Ik dacht dat het zo moest, maar kom daarmee niet op het goede antwoord uit.
Heb nog een vraag.
Gegeven: oplossing I: 100ml, 0.5 M Pb(NO3)2 (aq) en oplossing II: 75 ml 0.4 M K2SO4.
nu is de vraag hoeveel gram neerslag kan er maximaal ontstaan?
Ik heb al uitgerekend dat oplossing I 100 ml * 0.5 M = 50 mmol Pb(NO3)2 bevat.
Oplossing II bevat 75ml * 0.4 M = 30 mmol K2SO4.
de netto reactie is:
Pb2+ + SO42- ---> PbSO4
de beperkende reactant is SO42-.
Als ik nu 30 mmol * de molaire massa van PbSO4 doe, bereken ik dan hoeveel gram neerslag er kan ontstaan? Ik dacht dat het zo moest, maar kom daarmee niet op het goede antwoord uit.


In principe zou je hiermee op het juiste antwoord moeten komen, maar ik zou het iets anders opschrijven.quote:Op woensdag 13 juni 2012 13:41 schreef daantje1044 het volgende:
Bedankt weer! zat al te denken aan oplossing 1, maar dacht dat dat te makkelijk gedacht was van me. Niet zo moeilijk denken dus.
Heb nog een vraag.
Gegeven: oplossing I: 100ml, 0.5 M Pb(NO3)2 (aq) en oplossing II: 75 ml 0.4 M K2SO4.
nu is de vraag hoeveel gram neerslag kan er maximaal ontstaan?
Ik heb al uitgerekend dat oplossing I 100 ml * 0.5 M = 50 mmol Pb(NO3)2 bevat.
Oplossing II bevat 75ml * 0.4 M = 30 mmol K2SO4.
de netto reactie is:
Pb2+ + SO42- ---> PbSO4
de beperkende reactant is SO42-.
Als ik nu 30 mmol * de molaire massa van PbSO4 doe, bereken ik dan hoeveel gram neerslag er kan ontstaan? Ik dacht dat het zo moest, maar kom daarmee niet op het goede antwoord uit.
Je berekening dat er 50 mmol Pb(NO3)2 is opgelost klopt, maar je moet er nog wel bijschrijven dat 50 mmol Pb(NO3)2 ook 50 mmol Pb2+ bevat. Idem voor kaliumsulfaat: 30 mmol opgelost K2SO4 bevat 30 mmol SO42-.
Omdat het lood- en sulfaation reageren in de verhouding die jij ook opschrijft (1 mol lood reageert met 1 mol sulfaat en geeft 1 mol loodsulfaat), kan er niet meer loodsulfaat ontstaan dan er van de beperkende reactant aanwezig is: inderdaad 50 mmol lood, en slechts 30 mmol sulfaat, dus maximaal 30 mmol loodsulfaat.
30 mmol * de molmassa van loodsulfaat zou het antwoord moeten geven: 0,030* 303,3 = 9,1 g PbSO4


Ok dank je wel, zal het duidelijker uitschrijven dan, zou zonde zijn als ik daar dan punten op laat liggen, maar dan had ik het toch goed gedaan, op mijn antwoordblad kwamen ze op 11,2 g PbSO4 uit.quote:Op woensdag 13 juni 2012 14:15 schreef lyolyrc het volgende:
[..]
In principe zou je hiermee op het juiste antwoord moeten komen, maar ik zou het iets anders opschrijven.
Je berekening dat er 50 mmol Pb(NO3)2 is opgelost klopt, maar je moet er nog wel bijschrijven dat 50 mmol Pb(NO3)2 ook 50 mmol Pb2+ bevat. Idem voor kaliumsulfaat: 30 mmol opgelost K2SO4 bevat 30 mmol SO42-.
Omdat het lood- en sulfaation reageren in de verhouding die jij ook opschrijft (1 mol lood reageert met 1 mol sulfaat en geeft 1 mol loodsulfaat), kan er niet meer loodsulfaat ontstaan dan er van de beperkende reactant aanwezig is: inderdaad 50 mmol lood, en slechts 30 mmol sulfaat, dus maximaal 30 mmol loodsulfaat.
30 mmol * de molmassa van loodsulfaat zou het antwoord moeten geven: 0,030* 303,3 = 9,1 g PbSO4
Vandaar dat ik ook niet snapte wat ik nu fout deed. Ik kwam zelf namelijk ook op 9,1 g uit.
Bedankt!


Bij de meeste toetsen wordt ook gekeken naar hoe je tot het antwoord komt, vandaar dat zorgvuldig uitwerken van belang is. En het zou inderdaad zonde zijn als je dan punten daarop laat liggen, terwijl je wel snapt hoe je tot het juiste antwoord moet komen.quote:Op woensdag 13 juni 2012 14:26 schreef daantje1044 het volgende:
[..]
Ok dank je wel, zal het duidelijker uitschrijven dan, zou zonde zijn als ik daar dan punten op laat liggen, maar dan had ik het toch goed gedaan, op mijn antwoordblad kwamen ze op 11,2 g PbSO4 uit.
Vandaar dat ik ook niet snapte wat ik nu fout deed. Ik kwam zelf namelijk ook op 9,1 g uit.
Bedankt!
Antwoordbladen bevatten wel vaker fouten. Ik denk wel eens dat ze expres fouten erin zetten om studenten nog wat extra te laten zweten.


Denk het ook ja, ik maar denken wat doe ik toch fout? drie keer die molaire massa nagerekend, maar bleef maar op 9,1 uit komen hahaha.quote:Op woensdag 13 juni 2012 14:38 schreef lyolyrc het volgende:
[..]
Bij de meeste toetsen wordt ook gekeken naar hoe je tot het antwoord komt, vandaar dat zorgvuldig uitwerken van belang is. En het zou inderdaad zonde zijn als je dan punten daarop laat liggen, terwijl je wel snapt hoe je tot het juiste antwoord moet komen.
Antwoordbladen bevatten wel vaker fouten. Ik denk wel eens dat ze expres fouten erin zetten om studenten nog wat extra te laten zweten.


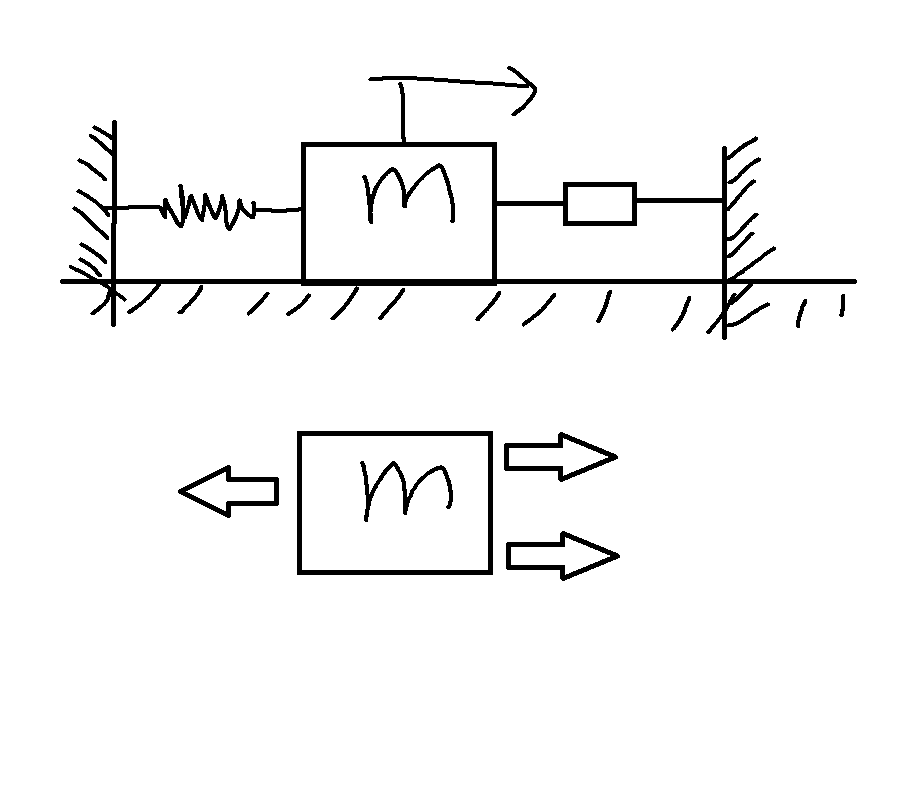
Ik heb weer iets heel simpels waar ik weer over na ga denken totdat ik mezelf niet meer snap:
Hier een simpel veer demper systeem. Als je daar een VLS van tekent hoe komen de krachten dan?
Die van de veer wijst naar links dat weet ik zeker maar van de demper gaat die ook naar links of toch naar rechts. Pijl boven op het blok is gewoon een externe kracht bijv.
Hier een simpel veer demper systeem. Als je daar een VLS van tekent hoe komen de krachten dan?
Die van de veer wijst naar links dat weet ik zeker maar van de demper gaat die ook naar links of toch naar rechts. Pijl boven op het blok is gewoon een externe kracht bijv.
Blues ain't nothing but a good man feeling bad...


Dat is zeker iets waarover je niet moet gaan nadenken tot je hoofdpijn hebt.quote:Op donderdag 14 juni 2012 16:34 schreef GoodGawd het volgende:
Ik heb weer iets heel simpels waar ik weer over na ga denken totdat ik mezelf niet meer snap:
[ afbeelding ]
Hier een simpel veer demper systeem. Als je daar een VLS van tekent hoe komen de krachten dan?
Die van de veer wijst naar links dat weet ik zeker maar van de demper gaat die ook naar links of toch naar rechts. Pijl boven op het blok is gewoon een externe kracht bijv.
Het antwoord is heel simpel: kies wat je handig lijkt, maar teken wel de reactiekrachten juist (lees: tegengesteld) in.


Nog maar even een paint en uitleg om duidelijk te maken waarom het niets uitmaakt:
Als we x naar rechts als positief kiezen, dan geldt voor A:
-Fs + Fd = mx" (1)
Fs = k(x-0) = kx (2)
Fd = d(0-x') = -dx' (3)
Substitueren van de (2) en (3) in (1) geeft
-kx - dx' = mx"
We kiezen wederom x naar rechts als positief en dan vinden we voor B:
Fs - Fd = mx" (4)
Fs = k(0-x) = -kx (5)
Fd = d(x'-0) = dx' (6)
Substitueren van (5) en (6) in (4) geeft
-kx - dx' = mx"
Zoals je ziet, krijg je voor A en B dezelfde bewegingsvergelijking.
Als we x naar rechts als positief kiezen, dan geldt voor A:
-Fs + Fd = mx" (1)
Fs = k(x-0) = kx (2)
Fd = d(0-x') = -dx' (3)
Substitueren van de (2) en (3) in (1) geeft
-kx - dx' = mx"
We kiezen wederom x naar rechts als positief en dan vinden we voor B:
Fs - Fd = mx" (4)
Fs = k(0-x) = -kx (5)
Fd = d(x'-0) = dx' (6)
Substitueren van (5) en (6) in (4) geeft
-kx - dx' = mx"
Zoals je ziet, krijg je voor A en B dezelfde bewegingsvergelijking.


Hey,
Zou iemand me kunnen helpen met deze fysica vraag...
Een uniform verdeelde lading (lineaire ladingsdichtheid 9 nC/m) is geplaatst tussen x=0 en x=3 langsheen de x-as. Bereken de grootte van het elektrisch veld in x = 4.
ik begrijp dat ik de volgende formule moet gebruiken : Ke * ʃ 1/r^2 dq
Ke is een constante namelijk 8,99 *10^9 en dq mag voor het integraal teken gezet worden.
Dus Ke * q *ʃ 1/r^2
dan moet ʃ 1/r^2 omgezet worden naar de primitieve vorm.. ik kom dan uit op ʃ r^-1 /-1 en vervolgens ʃ - 1 / r ... Het is een bepaalde integraal met begin waarde 0 en eindwaarde 3.
Ik weet echter totaal niet hoe ik nu verder moet, ik snap dat ik met bovenstaande formule het electrisch veld moet berekenen tot x=3 en dan x=4 als puntlading moet beschouwen... maar het lukt me niet. Het zou fijn zijn als iemand me hiermee kan helpen !
Zou iemand me kunnen helpen met deze fysica vraag...
Een uniform verdeelde lading (lineaire ladingsdichtheid 9 nC/m) is geplaatst tussen x=0 en x=3 langsheen de x-as. Bereken de grootte van het elektrisch veld in x = 4.
ik begrijp dat ik de volgende formule moet gebruiken : Ke * ʃ 1/r^2 dq
Ke is een constante namelijk 8,99 *10^9 en dq mag voor het integraal teken gezet worden.
Dus Ke * q *ʃ 1/r^2
dan moet ʃ 1/r^2 omgezet worden naar de primitieve vorm.. ik kom dan uit op ʃ r^-1 /-1 en vervolgens ʃ - 1 / r ... Het is een bepaalde integraal met begin waarde 0 en eindwaarde 3.
Ik weet echter totaal niet hoe ik nu verder moet, ik snap dat ik met bovenstaande formule het electrisch veld moet berekenen tot x=3 en dan x=4 als puntlading moet beschouwen... maar het lukt me niet. Het zou fijn zijn als iemand me hiermee kan helpen !


Nee, dat mag niet. Als je docent of boek dat beweert is dat flauwekul. Bedenk eerst eens wat dq/dr is.quote:Op zondag 17 juni 2012 18:29 schreef Vostokk het volgende:
Hey,
Zou iemand me kunnen helpen met deze fysica vraag...
Een uniform verdeelde lading (lineaire ladingsdichtheid 9 nC/m) is geplaatst tussen x=0 en x=3 langsheen de x-as. Bereken de grootte van het elektrisch veld in x = 4.
ik begrijp dat ik de volgende formule moet gebruiken : Ke * ʃ 1/r^2 dq
Ke is een constante namelijk 8,99 *10^9 en dq mag voor het integraal teken gezet worden.


hmm, ja ik dacht dat het integraal teken het differentiaalteken opheft en dat ik daarom q voor het integraalteken kan zetten. Maar om terug te komen op je vraag, dq/dr is volgens mij een heel klein deel van q gedeeld door een heel klein deel van r ..


Wat je in feite moet doen is de bijdrage aan het elektrisch veld van alle 'infinitesimale' ladingen dq verspreid over het lijnstuk langs de x-as van x = 0 tot x = 3 bij elkaar optellen. De bijdrage die één zo'n elementje levert is omgekeerd evenredig met het kwadraat van de afstand r tot het punt x = 4, en die afstand r loopt dus van r = 4 (voor x = 0) tot r = 1 (voor x = 3). Dan weet je dus al dat je moet integreren met r (niet q) als variabele en over het interval [1,4]. Weer de vraag: wat is dq/dr hier? Nu mag je het weer even zelf proberen.quote:Op zondag 17 juni 2012 18:46 schreef Vostokk het volgende:
hmm, ja ik dacht dat het integraal teken het differentiaalteken opheft en dat ik daarom q voor het integraalteken kan zetten. Maar om terug te komen op je vraag, dq/dr is volgens mij een heel klein deel van q gedeeld door een heel klein deel van r ..


Het 1e deel van je uitleg snap ik wel, ik weet alleen niet precies wat dq/dr is... ik weet dat df/dx de 1e afgeleide is van de functie f. Ik denk dan dat dq/dr wil zeggen dat je q afleidt naar r ?? Dit deel snap ik niet echt, ik heb het proberen op te zoeken maar ik word er niet veel wijzer van..
Als ik er echter vanuit ga dat ik bij de formule: Ke * ʃ 1/r^2 dq.
dq niet voor het integraalteken mag zetten kom ik op t volgende uit: Ke * ʃ -q/r
als ik dan het interval [1,4] toepas kom ik uit op 60,75 en dat is het juiste antwoord. Maar wat dq/dr nou precies is en wat die dq inhoudt begrijp ik ook niet echt...
Als ik er echter vanuit ga dat ik bij de formule: Ke * ʃ 1/r^2 dq.
dq niet voor het integraalteken mag zetten kom ik op t volgende uit: Ke * ʃ -q/r
als ik dan het interval [1,4] toepas kom ik uit op 60,75 en dat is het juiste antwoord. Maar wat dq/dr nou precies is en wat die dq inhoudt begrijp ik ook niet echt...


Het is echt heel eenvoudig, want in de opgave staat dat de lading uniform is verdeeld over het lijnstuk en dat de lineaire ladingsdichtheid 9 nC/m bedraagt. Dus hebben we dq/dr = 9 nC/m = 9∙10-9 C/m.quote:Op maandag 18 juni 2012 16:37 schreef Vostokk het volgende:
Het 1e deel van je uitleg snap ik wel, ik weet alleen niet precies wat dq/dr is... ik weet dat df/dx de 1e afgeleide is van de functie f. Ik denk dan dat dq/dr wil zeggen dat je q afleidt naar r ?? Dit deel snap ik niet echt, ik heb het proberen op te zoeken maar ik word er niet veel wijzer van..
Zoals gezegd integreer je met r als variabele, en dus moet je ook een integraal krijgen met dr, niet met dq.quote:Als ik er echter vanuit ga dat ik bij de formule: Ke * ʃ 1/r^2 dq.
dq niet voor het integraalteken mag zetten kom ik op t volgende uit: Ke * ʃ -q/r
als ik dan het interval [1,4] toepas kom ik uit op 60,75 en dat is het juiste antwoord. Maar wat dq/dr nou precies is en wat die dq inhoudt begrijp ik ook niet echt...
Welnu, voor de bijdrage dE aan het electrisch veld van een 'infinitesimale' lading dq op een stukje dr van het lijnstuk op een afstand r van het punt x = 4 hebben we:
dE = Ke∙r-2∙dq
Maar nu weten we ook dat dq/dr = 9∙10-9 C/m en dus dq = 9∙10-9∙dr (Coulomb, aangezien r in meter wordt uitgedrukt). Dus krijgen we:
dE = Ke∙r-2∙9∙10-9∙dr = 9∙10-9∙Ke∙r-2∙dr
De veldsterkte E in het punt x = 4 door de lading op het lijnstuk L wordt nu:
E = ʃL dE = 9∙10-9∙Ke∙ʃ14 r-2∙dr = 9∙10-9∙Ke∙[-r-1]14 = 9∙10-9∙Ke∙((-1/4) - (-1)) = 9∙10-9∙Ke∙(3/4) ≈ 60,75 N/C.
[ Bericht 2% gewijzigd door Riparius op 21-06-2012 13:15:58 ]


haha ja ik zie nu wat je bedoelt met dq/dr, en ik begrijp je werkwijze. Maar we komen op t zelfde antwoord uit, en ik gebruik deze formule Ke * ʃ -q/r. Volgens mij klopt deze formule dan ook of zie ik hier toch weer iets over t hoofd ?
Heel erg bedankt voor je uitleg, het is een stuk duidelijker nu !
Heel erg bedankt voor je uitleg, het is een stuk duidelijker nu !


Nee, je formule klopt niet. Om te beginnen is -r-1 een primitieve van r-2, dus moet je dan niet meer dat integraalteken schrijven. Hierboven deed je dat ook al, en dat is gewoon fout. Correct is bijvoorbeeld wel:quote:Op maandag 18 juni 2012 19:58 schreef Vostokk het volgende:
Haha ja ik zie nu wat je bedoelt met dq/dr, en ik begrijp je werkwijze. Maar we komen op 't zelfde antwoord uit, en ik gebruik deze formule Ke * ʃ -q/r. Volgens mij klopt deze formule dan ook of zie ik hier toch weer iets over 't hoofd ?
∫14 r-2dr = [-r-1]14 = (-1/4) -(-1) = 3/4.
Je hebt wel gelijk dat d en ∫ inverse bewerkingen symboliseren, zodat bijvoorbeeld E = ∫ dE, en zo heb je ook q = ∫ dq, maar je moest de veldsterkte E berekenen in het punt x = 4, en niet de lading q van het gehele lijnstuk. Dus moet je eerst een uitdrukking voor dE afleiden, zoals ik hierboven heb gedaan.
quote:Heel erg bedankt voor je uitleg, het is een stuk duidelijker nu !


Help! Morgen een tentamen moleculaire biologie maar er is een techniek die ik echt niet snap. 
Het gaat om het gebruiken van homologe recombinatie om knock outs te maken (in bv. muisjes).
Als iemand me dit wat duidelijker kan uitleggen of een goed filmpje weet waarin de techniek wordt besproken zou ik dat erg op prijs stellen.
Het gaat om het gebruiken van homologe recombinatie om knock outs te maken (in bv. muisjes).
Als iemand me dit wat duidelijker kan uitleggen of een goed filmpje weet waarin de techniek wordt besproken zou ik dat erg op prijs stellen.


Wat snap je niet precies?quote:Op woensdag 20 juni 2012 21:54 schreef VGA4xZoom het volgende:
Help! Morgen een tentamen moleculaire biologie maar er is een techniek die ik echt niet snap.
Het gaat om het gebruiken van homologe recombinatie om knock outs te maken (in bv. muisjes).
Als iemand me dit wat duidelijker kan uitleggen of een goed filmpje weet waarin de techniek wordt besproken zou ik dat erg op prijs stellen.


Ik heb hier een vraag over de impulsbalans van een vak genaamd Fysische Transportverschijnselen. Het gaat om stroming van een vloeistof door een buis. De opdracht is geformuleerd als volgt:
De eerste 2 vragen kan op oplossen. a wordt opgelost door het opstellen van een massabalans, en b door het opstellen van een energiebalans. Ik weet dat vraag c wordt opgelost door het opstellen van een impulsbalans, maar ik begrijp het zelf niet echt. Ik heb hier een gedeelte van de uitwerking door de docent.
Dit is de algemene impulsbalans, dat is het makkelijke gedeelte:
Echter ik begrijp niet waarom deze kracht negatief is, en waarom niet cosinus of tangens.
Weet iemand hier het antwoord op?
De eerste 2 vragen kan op oplossen. a wordt opgelost door het opstellen van een massabalans, en b door het opstellen van een energiebalans. Ik weet dat vraag c wordt opgelost door het opstellen van een impulsbalans, maar ik begrijp het zelf niet echt. Ik heb hier een gedeelte van de uitwerking door de docent.
Dit is de algemene impulsbalans, dat is het makkelijke gedeelte:
Echter ik begrijp niet waarom deze kracht negatief is, en waarom niet cosinus of tangens.
Weet iemand hier het antwoord op?


In de onderste tekening is v3 ontbonden in een x- en y-component en daarbij wijst de y-component omlaag. Omdat die y-component omlaag wijst en y omhoog als positief is gedefinieerd, moet de y-component van v3 negatief zijn.quote:Op zaterdag 23 juni 2012 11:33 schreef Oswald_Montecristo het volgende:
Ik heb hier een vraag over de impulsbalans van een vak genaamd Fysische Transportverschijnselen. Het gaat om stroming van een vloeistof door een buis. De opdracht is geformuleerd als volgt:
[ afbeelding ]
De eerste 2 vragen kan op oplossen. a wordt opgelost door het opstellen van een massabalans, en b door het opstellen van een energiebalans. Ik weet dat vraag c wordt opgelost door het opstellen van een impulsbalans, maar ik begrijp het zelf niet echt. Ik heb hier een gedeelte van de uitwerking door de docent.
Dit is de algemene impulsbalans, dat is het makkelijke gedeelte:
[ afbeelding ]
Echter ik begrijp niet waarom deze kracht negatief is, en waarom niet cosinus of tangens.
[ afbeelding ]
[ afbeelding ]
Weet iemand hier het antwoord op?


Ik kom er maar niet uit hoe ik formules als om moet zetten naar bijvoorbeeld
Iemand die me dit uit kan leggen?
Iemand die me dit uit kan leggen?


Deel beide kanten door l, en doe dan beide kanten keer A. Wat komt daar dan uit?quote:Op zaterdag 23 juni 2012 14:55 schreef Miraculously het volgende:
Ik kom er maar niet uit hoe ik formules als [ afbeelding ] om moet zetten naar bijvoorbeeld [ afbeelding ]
Iemand die me dit uit kan leggen?


Dat lijkt me dan
Maar waarom dan eerst delen door l en dan pas keer A, want dat deed ik eerst andersom, en dan kwam ik uit op dit:
Maar waarom dan eerst delen door l en dan pas keer A, want dat deed ik eerst andersom, en dan kwam ik uit op dit:


Dat is hetzelfde.quote:Op zaterdag 23 juni 2012 15:28 schreef Miraculously het volgende:
Dat lijkt me dan [ afbeelding ]
Maar waarom dan eerst delen door l en dan pas keer A, want dat deed ik eerst andersom, en dan kwam ik uit op dit:
[ afbeelding ]


Zij T = (V, E) een optimale decodeerboom voor een prefixcode voor het
alfabet met tekens 1, 2, ..., n, waarbij n = 2^k en frequentieverdeling f1=<f2=<....=<fn.
Zij l de afstand in T van de wortel tot het blad van teken i. Ontwikkel een voorwaarde voor de frequenties zó dat T noodzakelijkerwijs de volle binaire boom van diepte (hoogte) k is. Beargumenteer uw oplossing.
de afstand in T van de wortel tot het blad van teken i. Ontwikkel een voorwaarde voor de frequenties zó dat T noodzakelijkerwijs de volle binaire boom van diepte (hoogte) k is. Beargumenteer uw oplossing.
-------------------------------
Nou heb je een vrij simpele voorwaarde, dat is als alle frequenties gelijk zijn. Alleen neem ik aan dat er hier een sterkere voorwaarde gezocht moet worden?
alfabet met tekens 1, 2, ..., n, waarbij n = 2^k en frequentieverdeling f1=<f2=<....=<fn.
Zij l
 de afstand in T van de wortel tot het blad van teken i. Ontwikkel een voorwaarde voor de frequenties zó dat T noodzakelijkerwijs de volle binaire boom van diepte (hoogte) k is. Beargumenteer uw oplossing.
de afstand in T van de wortel tot het blad van teken i. Ontwikkel een voorwaarde voor de frequenties zó dat T noodzakelijkerwijs de volle binaire boom van diepte (hoogte) k is. Beargumenteer uw oplossing.-------------------------------
Nou heb je een vrij simpele voorwaarde, dat is als alle frequenties gelijk zijn. Alleen neem ik aan dat er hier een sterkere voorwaarde gezocht moet worden?


Het gaat om het woord 'noodzakelijkerwijs'. Als alle frequenties gelijk zijn is de optimale decodeerboom niet noodzakelijkerwijs de volle binaire boom.


Je tweede afgeleide van θ(t) naar t is fout.quote:Op donderdag 28 juni 2012 17:17 schreef dynamiet het volgende:
Ik heb de volgende opgave:
[ afbeelding ]
Ik tot zover gekomen:
[ afbeelding ]
Zou iemand mij verder kunnen helpen? Ik kom er niet uit hoe ik de termen c1, c2 en c3 moet bepalen.
[ Bericht 7% gewijzigd door Riparius op 28-06-2012 18:37:00 ]


Nog een vraagje:
Volgens mij klopt het stukje met cos niet. Volgens mij moet dat alleen vermenigvuldigd worden met een lengte.
EDIT: na 2 dagen eigenlijk gevonden. Als je het opsplitst in een gewicht, snelheid en zwaartekracht matrix dan moet de gewicht matrix symmetrisch zijn.
Dat is hier niet het geval en daarom klopt er dus iets niet.
[ Bericht 15% gewijzigd door dynamiet op 01-07-2012 14:39:39 ]
Volgens mij klopt het stukje met cos niet. Volgens mij moet dat alleen vermenigvuldigd worden met een lengte.
EDIT: na 2 dagen eigenlijk gevonden. Als je het opsplitst in een gewicht, snelheid en zwaartekracht matrix dan moet de gewicht matrix symmetrisch zijn.
Dat is hier niet het geval en daarom klopt er dus iets niet.
[ Bericht 15% gewijzigd door dynamiet op 01-07-2012 14:39:39 ]


Een vraag met betrekking tot onderzoek.
Kan iemand vertellen wat de waarde van de Fisher's exact test moet zijn om significant te zijn? Is er een bepaald minimum/maximum waar de uitkomst aan zou moeten voldoen?
Dank alvast.
Kan iemand vertellen wat de waarde van de Fisher's exact test moet zijn om significant te zijn? Is er een bepaald minimum/maximum waar de uitkomst aan zou moeten voldoen?
Dank alvast.


heey ik heb een vraagje,
in de vakantie moest ik een extra opdracht voor scheikunde maken i.v.m een te laag cijfer.
maar nu ben ik bezig en ik ben ook bijna klaar, alleen ik kan niet uit deze vraag komen.
tekst:
in een vat van 500 ml word bij constante temperatuur de volgende reactie uitgevoerd:
CH3Cl + I- >>>> CH3I + Cl-
tijdens deze reactie wordt op verschillende tijdstippen gemeten hoeveel mol I- nog in het vat aanwezig is. Dat levert de volgende resultaten op.
tijd (min) --------------- hoeveelheid I-
0 ------------------------- 0,250
180 ---------------------- 0,225
360 ---------------------- 0,205
vraag:
bereken de gemiddelde reactie snelheid in het interval 0 - 180 minuten in mol L-1s-1
ik weet niet zeker wat ik hier moet doen, maar kan het kloppen dat ik eerst de 500ml naar L en dat ik de minuten naar seconde moet veranderen?
alvast bedankt
in de vakantie moest ik een extra opdracht voor scheikunde maken i.v.m een te laag cijfer.
maar nu ben ik bezig en ik ben ook bijna klaar, alleen ik kan niet uit deze vraag komen.
tekst:
in een vat van 500 ml word bij constante temperatuur de volgende reactie uitgevoerd:
CH3Cl + I- >>>> CH3I + Cl-
tijdens deze reactie wordt op verschillende tijdstippen gemeten hoeveel mol I- nog in het vat aanwezig is. Dat levert de volgende resultaten op.
tijd (min) --------------- hoeveelheid I-
0 ------------------------- 0,250
180 ---------------------- 0,225
360 ---------------------- 0,205
vraag:
bereken de gemiddelde reactie snelheid in het interval 0 - 180 minuten in mol L-1s-1
ik weet niet zeker wat ik hier moet doen, maar kan het kloppen dat ik eerst de 500ml naar L en dat ik de minuten naar seconde moet veranderen?
alvast bedankt


Klopt, je moet in ieder geval werken in liters en seconden, dus het is zeker slim om daar al je waarden naar over te zetten.quote:Op donderdag 30 augustus 2012 12:00 schreef orangesjuice het volgende:
in een vat van 500 ml word bij constante temperatuur de volgende reactie uitgevoerd:
CH3Cl + I- >>>> CH3I + Cl-
tijdens deze reactie wordt op verschillende tijdstippen gemeten hoeveel mol I- nog in het vat aanwezig is. Dat levert de volgende resultaten op.
tijd (min) --------------- hoeveelheid I-
0 ------------------------- 0,250
180 ---------------------- 0,225
360 ---------------------- 0,205
vraag:
bereken de gemiddelde reactie snelheid in het interval 0 - 180 minuten in mol L-1s-1
ik weet niet zeker wat ik hier moet doen, maar kan het kloppen dat ik eerst de 500ml naar L en dat ik de minuten naar seconde moet veranderen?
alvast bedankt
Ik neem aan dat de hoeveelheid aanwezige jodide in mol is gegeven?
www.4beta.nl
www.youtube.nl/jweckhardt
---
Als je het niet simpel kunt uitleggen, begrijp je het niet goed genoeg
www.youtube.nl/jweckhardt
---
Als je het niet simpel kunt uitleggen, begrijp je het niet goed genoeg


(edit: zie net dat ik in het verkeerde topic heb gepost)
Hey allemaal, heb een kansrekeningsvraag:
- Wat is de kans op een willekeurige straat bij het trekken van 5 kaarten uit een deck kaarten?
Ik kom hier niet uit, het berekenen van een specifieke straat (bijv. A t/m 5) is niet moeilijk, maar als je een willekeurige straat moet berekenen raak ik de draad kwijt.
Het maakt voor een straat niet uit wat de eerste kaart is, elke kaart is goed, maar de kans op een goede tweede kaart maakt wel uit van wat je als eerst getrokken hebt als kaart. Ik zie vast een makkelijkere redeneerwijze over het hoofd, maar kom er toch niet uit.
[ Bericht 5% gewijzigd door Hz op 31-08-2012 13:44:41 (fout topic) ]
Hey allemaal, heb een kansrekeningsvraag:
- Wat is de kans op een willekeurige straat bij het trekken van 5 kaarten uit een deck kaarten?
Ik kom hier niet uit, het berekenen van een specifieke straat (bijv. A t/m 5) is niet moeilijk, maar als je een willekeurige straat moet berekenen raak ik de draad kwijt.
Het maakt voor een straat niet uit wat de eerste kaart is, elke kaart is goed, maar de kans op een goede tweede kaart maakt wel uit van wat je als eerst getrokken hebt als kaart. Ik zie vast een makkelijkere redeneerwijze over het hoofd, maar kom er toch niet uit.
[ Bericht 5% gewijzigd door Hz op 31-08-2012 13:44:41 (fout topic) ]


t = 0quote:Op donderdag 30 augustus 2012 17:48 schreef 4Beta het volgende:
Ik neem aan dat de hoeveelheid aanwezige jodide in mol is gegeven?
Ow, je hebt het over de eenheden ... ik las te snel.


ja dat was in mol en ik ben eruit gekomen nu, maar nu heb ik nog wat anders.quote:Op donderdag 30 augustus 2012 17:48 schreef 4Beta het volgende:
[..]
Klopt, je moet in ieder geval werken in liters en seconden, dus het is zeker slim om daar al je waarden naar over te zetten.
Ik neem aan dat de hoeveelheid aanwezige jodide in mol is gegeven?
(in een reactie vat van 5,00L brengt men 1,00 mol H2(g) en 2,00 mol N2(g)
deze twee gassen reageren met elkaar onder vorming van ammoniakgas. na enige tijd steld zich een evenwicht in. er is dan 0,100 mol NH3 gevormd: 3H2(g) + N2 -> 2 NH3)
nu is de vraag bereken de concentratie van elk van de drie stoffen als het evenwicht bereikt is. maar uit het boek kan ik het niet ophalen, maar wat bedoelen ze hier bij "als het evenwicht bereikt is"?


Als het evenwicht bereikt is betekent dat de reactie 'gestopt' is. Dat wil zeggen, er gebeurd nog genoeg maar de reactie naar links werkt even snel als de reactie naar rechts en men spreekt dan ook van een evenwichtsituatie.quote:Op maandag 3 september 2012 14:30 schreef orangesjuice het volgende:
[..]
ja dat was in mol en ik ben eruit gekomen nu, maar nu heb ik nog wat anders.
(in een reactie vat van 5,00L brengt men 1,00 mol H2(g) en 2,00 mol N2(g)
deze twee gassen reageren met elkaar onder vorming van ammoniakgas. na enige tijd steld zich een evenwicht in. er is dan 0,100 mol NH3 gevormd: 3H2(g) + N2 -> 2 NH3)
nu is de vraag bereken de concentratie van elk van de drie stoffen als het evenwicht bereikt is. maar uit het boek kan ik het niet ophalen, maar wat bedoelen ze hier bij "als het evenwicht bereikt is"?


Hallo daar,
Wat betreft informatica,
Ben bezig met Aries Institute of Technology en loop een beetje vast bij de binaire getallen.
onder andere de vragen:
welke reeks decimale getallen wordt door deze binaire getallen weergegeven? 1,10,11,100,101.
welk decimale getal wordt door het binaire getal 10101111 weergegeven?
zijn deze op te lossen met een simpele rekensom of rekenmachine, of is dit nou iets wat je moet leren?
kon er verder geen duidelijke informatie over vinden. alvast bedankt:)
Wat betreft informatica,
Ben bezig met Aries Institute of Technology en loop een beetje vast bij de binaire getallen.
onder andere de vragen:
welke reeks decimale getallen wordt door deze binaire getallen weergegeven? 1,10,11,100,101.
welk decimale getal wordt door het binaire getal 10101111 weergegeven?
zijn deze op te lossen met een simpele rekensom of rekenmachine, of is dit nou iets wat je moet leren?
kon er verder geen duidelijke informatie over vinden. alvast bedankt:)
het is maar net wat je van je leven wilt maken.


Ik zal even binair van 0 tot 20 tellen. Zoek het systeem.
0
1
10
11
100
101
110
111
1000
1001
1010
1011
1100
1101
1110
1111
10000
10001
10010
10011
10100
0
1
10
11
100
101
110
111
1000
1001
1010
1011
1100
1101
1110
1111
10000
10001
10010
10011
10100


ik snap hem:) kwestie van logica en en een beetje rekenen dus, bedankt.
het is maar net wat je van je leven wilt maken.


Wat dacht je van de calculator van Windows? Die vertelt je meteen dat 10101111 binair gelijk is aan 175 decimaal. Of zet het even om naar hexadecimaal. Dan krijg je AF hex en zie je ook meteen dat dit gelijk is aan 10∙16 + 15 = 175.quote:Op donderdag 6 september 2012 20:46 schreef facile het volgende:
Hallo daar,
Wat betreft informatica,
Ben bezig met Aries Institute of Technology en loop een beetje vast bij de binaire getallen.
onder andere de vragen:
welke reeks decimale getallen wordt door deze binaire getallen weergegeven? 1,10,11,100,101.
welk decimale getal wordt door het binaire getal 10101111 weergegeven?
zijn deze op te lossen met een simpele rekensom of rekenmachine, of is dit nou iets wat je moet leren?
kon er verder geen duidelijke informatie over vinden. alvast bedankt:)


Brrr, okee, ik ben bezig met een cursus toegepaste rekenvaardigheden voor mn werk. The horror... Ik ben vroeger altijd meer een alfa student geweest en nu snap ik weer waarom  Heb me opgegeven om wat bedrevener te worden met rekensommen, maar ik vraag me af of ik het ooit ga leren
Heb me opgegeven om wat bedrevener te worden met rekensommen, maar ik vraag me af of ik het ooit ga leren 
Onderstaande opgave kom ik dus gewoon niet uit, weet niet eens waar ik moet beginnen... Kan iemand er wat licht op werpen? Het zal vast simpel zijn uiteindelijk, maar ik zie het niet...
Aantal motorfietsen totaal: 396.000. Deze zijn verdeeld over 90% bezitters met één motorfiets en 10% die drie motorfietsen bezitten.
Het aantal bezitters van één of meer motorfietsen is derhalve:
Onderstaande opgave kom ik dus gewoon niet uit, weet niet eens waar ik moet beginnen... Kan iemand er wat licht op werpen? Het zal vast simpel zijn uiteindelijk, maar ik zie het niet...
Aantal motorfietsen totaal: 396.000. Deze zijn verdeeld over 90% bezitters met één motorfiets en 10% die drie motorfietsen bezitten.
Het aantal bezitters van één of meer motorfietsen is derhalve:
Uitgelaten geeft het publiek een staande ovulatie.


Dit soort sommetjes kregen kinderen vroeger in de vijfde klas van de lagere school.quote:Op vrijdag 7 september 2012 09:24 schreef VaLkyRie het volgende:
Brrr, okee, ik ben bezig met een cursus toegepaste rekenvaardigheden voor mn werk. The horror... Ik ben vroeger altijd meer een alfa student geweest en nu snap ik weer waaromHeb me opgegeven om wat bedrevener te worden met rekensommen, maar ik vraag me af of ik het ooit ga leren

Onderstaande opgave kom ik dus gewoon niet uit, weet niet eens waar ik moet beginnen... Kan iemand er wat licht op werpen? Het zal vast simpel zijn uiteindelijk, maar ik zie het niet...
Aantal motorfietsen totaal: 396.000. Deze zijn verdeeld over 90% bezitters met één motorfiets en 10% die drie motorfietsen bezitten.
Het aantal bezitters van één of meer motorfietsen is derhalve:
Stel dat er x bezitters zijn van één of meer motorfietsen. Daarvan bezit 90% oftewel 0,9∙x personen één motorfiets en de resterende 10% oftewel 0,1∙x personen drie motorfietsen. Het totaal aantal motorfietsen is dus:
0,9∙x + 3∙0,1∙x = 1,2∙x
Maar nu is gegeven dat het totaal aantal motorfietsen 396.000 bedraagt. Dus hebben we:
1,2∙x = 396.000
Nu beide leden delen door 1,2 en we krijgen voor x oftewel het aantal bezitters:
x = 330.000


Ja erg hequote:Op vrijdag 7 september 2012 09:38 schreef Riparius het volgende:
[..]
Dit soort sommetjes kregen kinderen vroeger in de vijfde klas van de lagere school.
Stel dat er x bezitters zijn van één of meer motorfietsen. Daarvan bezit 90% oftewel 0,9∙x personen één motorfiets en de resterende 10% oftewel 0,1∙x personen drie motorfietsen. Het totaal aantal motorfietsen is dus:
0,9∙x + 3∙0,1∙x = 1,2∙x
Maar nu is gegeven dat het totaal aantal motorfietsen 396.000 bedraagt. Dus hebben we:
1,2∙x = 396.000
Nu beide leden delen door 1,2 en we krijgen voor x oftewel het aantal bezitters:
x = 330.000
Bedankt voor je hulp in ieder geval!
Uitgelaten geeft het publiek een staande ovulatie.


Dit leek me het beste topic om dit te vragen.
Wat is de wiskunde benaming van dat metalen ding, die 2 plus-tekens in elkaar?
Zoals een dobbelsteen een kubus is, hoe noem je dit?
Wat is de wiskunde benaming van dat metalen ding, die 2 plus-tekens in elkaar?
Zoals een dobbelsteen een kubus is, hoe noem je dit?
'To alcohol, the cause of and the solution to all of life's problems' - Homer J. Simpson


Kunnen jullie mij helpen met de volgende vraag:
Waarom zijn kunstof weegflesjes minder geschikt voor het wegen van een exact gepipetteerde vloeistof?
Waarom zijn kunstof weegflesjes minder geschikt voor het wegen van een exact gepipetteerde vloeistof?


Diffusie in het plastic. Weekmakers evt.quote:Op maandag 24 september 2012 23:12 schreef sorcovic het volgende:
Kunnen jullie mij helpen met de volgende vraag:
Waarom zijn kunstof weegflesjes minder geschikt voor het wegen van een exact gepipetteerde vloeistof?
De stof moet er ook weer uit. Massaverschil voor / na niet constant, grotere weegfout?


Even een vraagje over een formule 'ombouwen':
Als ik van hieruit de wortel weg wil werken moet ik toch al het andere kwadrateren, inclusief de T?
Zodat je dit krijgt:
Of de T niet?; want bij het nakijken kwadrateren ze de T niet. Maar als ik een grafiek plot op m'n GR kom ik op mijn antwoord uit.
Als ik van hieruit de wortel weg wil werken moet ik toch al het andere kwadrateren, inclusief de T?
Zodat je dit krijgt:
Of de T niet?; want bij het nakijken kwadrateren ze de T niet. Maar als ik een grafiek plot op m'n GR kom ik op mijn antwoord uit.


Als je aan een kant gaan kwadrateren gaat het alleen goed als toevallig beide kanten gelijk zijn aan 1 of 0. Want 1=1². Maar bijvoorbeeld niet 2=2². Met variabelen werkt het net zo.


Mijn broertje kwam vanavond naar me toe met een vraag in zijn natuurkundeboek over de Maagdenburgse bol: twee ijzeren halve bollen (met een gegeven straal r, in het boek was een concreet getal genoemd, maar het is denk ik net zo makkelijk om het algemene geval uit te rekenen) met zijn tegen elkaar 'geplakt', en de lucht is ertussenuit gepompt, zo, dat er (nagenoeg) een vacuum tussen hen is.
In de opdracht mag je ervan uitgaan dat er een vacuum is, en moet je de kracht berekenen die het kost om de bollen uit elkaar te trekken. Mijn broertje dacht dat je de oppervlakte van de bol moest nemen, maar kwam zelf al met de opmerking dat de luchtdruk richting de normaal naar binnen werkt, en dus niet elke richting 'even zwaar meetelt'.
Verder mocht je gebruiken dat de luchtdruk 1 bar = 100.000 Pa is, met 1 Pa = 1 N/m2.
De situatie:
In de opdracht mag je ervan uitgaan dat er een vacuum is, en moet je de kracht berekenen die het kost om de bollen uit elkaar te trekken. Mijn broertje dacht dat je de oppervlakte van de bol moest nemen, maar kwam zelf al met de opmerking dat de luchtdruk richting de normaal naar binnen werkt, en dus niet elke richting 'even zwaar meetelt'.
Verder mocht je gebruiken dat de luchtdruk 1 bar = 100.000 Pa is, met 1 Pa = 1 N/m2.
De situatie:
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Ik dacht zelf trouwens overigens dat je eigenlijk de integraal van de normaal (naar binnen gericht) moest nemen over de oppervlakte van een halve bol. Ik kon intuïtief ook wel inzien dat de kracht die nodig was om de bollen uit elkaar te trekken waarschijnlijk evenredig was met r2 (als je een papiertje tussen de bollen stopt, zie je dat de oppervlakte tussen hen gelijk is aan pi*r2, maar ik kon niet precies uitleggen waarom dit het goede antwoord was. Je kan het papiertje immers ook vouwen, zodat het een grotere oppervlakte heeft. Dan vallen er vast weer krachten tegen elkaar weg, maar de totale kracht blijft volgens mij niet per se even groot...)
Wie kan me hier wat inzicht over verschaffen? Ik weet nog dat ik de opgave destijds ook gemaakt heb, en dat ik hem toen ook niet helemaal snapte, maar mijn natuurkundeleraar wist me wel te overtuigen van de juistheid van de methode.


Stel dat je twee halve cylinders hebt, in plaats van halve bollen, maar met hetzelfde oppervlak waar de halve cylinders elkaar raken. Denk je dan dat de krachten anders zullen zijn dan bij halve bollen? Zo ja, waarom? Of dat je de "top" van de bollen afsnijdt met een snijbrander en daar dan pilonnen aan vastlast (van die wegwerkergevallen, maar dan van staal). Zal het iets uitmaken qua krachten? (De twee streepjes in onderstaande tekening geven aan dat de lengtes van deze lijnen even lang zijn).
Of bekijk het van de andere kant: houd de halve bollen even groot, maar las er twee verbindingsstukjes aan vast waardoor het oppervlak waarmee de twee halve bollen aan elkaar zitten, wordt verkleind. Een soort van vernauwing dus. Wat zal de invloed daarvan zijn op de krachten? Als je het antwoord niet weet, verklein het oppervlak van dat tussenstuk tot 1 mm2 en vraag je dan af of je die bollen nog uit elkaar kan trekken. Zelf, met je blote handen.
Geeft dit het inzicht waar je naar op zoek bent?
[ Bericht 0% gewijzigd door Lyrebird op 28-09-2012 06:21:08 ]
Of bekijk het van de andere kant: houd de halve bollen even groot, maar las er twee verbindingsstukjes aan vast waardoor het oppervlak waarmee de twee halve bollen aan elkaar zitten, wordt verkleind. Een soort van vernauwing dus. Wat zal de invloed daarvan zijn op de krachten? Als je het antwoord niet weet, verklein het oppervlak van dat tussenstuk tot 1 mm2 en vraag je dan af of je die bollen nog uit elkaar kan trekken. Zelf, met je blote handen.
Geeft dit het inzicht waar je naar op zoek bent?
[ Bericht 0% gewijzigd door Lyrebird op 28-09-2012 06:21:08 ]
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Zit een een statistiekvraagje. Hoop dat een van jullie mij kan helpen.
In het engels:
The Pediatrics unit at Carver Hospital has 24 beds. The number of patients needing a bed at any point is in time is N(19.2, 2.5). what is the probability that the number of patients needing a bed will exceed the pediatric units bed capacity.
antwoord is: P(Z-> 1,92) = 1-.9726 = .0274.
Kan er alleen niet uitkomen welke formule ik moet gebruiken. Ik gebruik zelf x-u/ o.
Ik weet alleen niet hoe ik hier de u en de o moet berekenen. wie kan me helpen?
In het engels:
The Pediatrics unit at Carver Hospital has 24 beds. The number of patients needing a bed at any point is in time is N(19.2, 2.5). what is the probability that the number of patients needing a bed will exceed the pediatric units bed capacity.
antwoord is: P(Z-> 1,92) = 1-.9726 = .0274.
Kan er alleen niet uitkomen welke formule ik moet gebruiken. Ik gebruik zelf x-u/ o.
Ik weet alleen niet hoe ik hier de u en de o moet berekenen. wie kan me helpen?


De formule die je wil gebruiken klopt (al moet je wel μ en σ schrijven in plaats van u en o).quote:Op vrijdag 28 september 2012 12:45 schreef ongelovelijk het volgende:
Zit een een statistiekvraagje. Hoop dat een van jullie mij kan helpen.
In het engels:
The Pediatrics unit at Carver Hospital has 24 beds. The number of patients needing a bed at any point is in time is N(19.2, 2.5). what is the probability that the number of patients needing a bed will exceed the pediatric units bed capacity.
antwoord is: P(Z-> 1,92) = 1-.9726 = .0274.
Kan er alleen niet uitkomen welke formule ik moet gebruiken. Ik gebruik zelf x-u/ o.
Ik weet alleen niet hoe ik hier de u en de o moet berekenen. wie kan me helpen?
Het is gebruikelijk om een normale verdeling op te geven in de vorm N(μ,σ2). Hier wordt opgegeven N(19.2, 2.5). Dat zou betekenen dat μ = 19,2 en σ2 = 2,5 en dus σ = √ 2,5.
Pas dan de formule toe die je zelf ook al had gevonden en vul μ en σ in zoals ik ze hier heb gegeven.
P(X>24) = P(Z>(24 - μ)/σ) = ... (doe de rest van de berekening zelf)
Mochten ze in deze opgave toch heel eigenwijs de normale verdeling hebben opgegeven in de vorm N(μ,σ), dan zou je moeten uitkomen op het antwoord dat is gegeven.


Het helpt zeker, bedankt!quote:Op vrijdag 28 september 2012 05:41 schreef Lyrebird het volgende:
Stel dat je twee halve cylinders hebt, in plaats van halve bollen, maar met hetzelfde oppervlak waar de halve cylinders elkaar raken. Denk je dan dat de krachten anders zullen zijn dan bij halve bollen? Zo ja, waarom? Of dat je de "top" van de bollen afsnijdt met een snijbrander en daar dan pilonnen aan vastlast (van die wegwerkergevallen, maar dan van staal). Zal het iets uitmaken qua krachten? (De twee streepjes in onderstaande tekening geven aan dat de lengtes van deze lijnen even lang zijn).
[ afbeelding ]
Of bekijk het van de andere kant: houd de halve bollen even groot, maar las er twee verbindingsstukjes aan vast waardoor het oppervlak waarmee de twee halve bollen aan elkaar zitten, wordt verkleind. Een soort van vernauwing dus. Wat zal de invloed daarvan zijn op de krachten? Als je het antwoord niet weet, verklein het oppervlak van dat tussenstuk tot 1 mm2 en vraag je dan af of je die bollen nog uit elkaar kan trekken. Zelf, met je blote handen.
[ afbeelding ]
Geeft dit het inzicht waar je naar op zoek bent?


dankje dat was hem, ik weet dat ik μ en σ moet schrijven in plaats van u en o.quote:Op vrijdag 28 september 2012 14:13 schreef lyolyrc het volgende:
[..]
De formule die je wil gebruiken klopt (al moet je wel μ en σ schrijven in plaats van u en o).
Het is gebruikelijk om een normale verdeling op te geven in de vorm N(μ,σ2). Hier wordt opgegeven N(19.2, 2.5). Dat zou betekenen dat μ = 19,2 en σ2 = 2,5 en dus σ = √ 2,5.
Pas dan de formule toe die je zelf ook al had gevonden en vul μ en σ in zoals ik ze hier heb gegeven.
P(X>24) = P(Z>(24 - μ)/σ) = ... (doe de rest van de berekening zelf)
Mochten ze in deze opgave toch heel eigenwijs de normale verdeling hebben opgegeven in de vorm N(μ,σ), dan zou je moeten uitkomen op het antwoord dat is gegeven.


Wat is de formele manier om hoeken tussen inwendig product te bepalen?
bijv:
bijv:
Blues ain't nothing but a good man feeling bad...


u.v = |u||v|cosθquote:Op vrijdag 28 september 2012 16:40 schreef GoodGawd het volgende:
Wat is de formele manier om hoeken tussen inwendig product te bepalen?
bijv:
[ afbeelding ]
Je kunt de hoek dus berekenen door het inproduct van de vectoren te bepalen en dan te delen door de lengtes van de vectoren. Van het resultaat neem je de arccos.


Nee precies, ik wist het niet meer zeker doordat ze het in het antwoordmodel niet deden. Dan staat daar dus een fout in. Bedankt.quote:Op donderdag 27 september 2012 22:53 schreef thenxero het volgende:
Als je aan een kant gaan kwadrateren gaat het alleen goed als toevallig beide kanten gelijk zijn aan 1 of 0. Want 1=1². Maar bijvoorbeeld niet 2=2². Met variabelen werkt het net zo.
Bedankt.quote:Op donderdag 27 september 2012 22:47 schreef Anoonumos het volgende:
Ja, de T moet ook. Je moet links en rechts van het = teken altijd hetzelfde doen.


quote:Op vrijdag 28 september 2012 01:40 schreef kutkloon7 het volgende:
Mijn broertje kwam vanavond naar me toe met een vraag in zijn natuurkundeboek over de Maagdenburgse bol: twee ijzeren halve bollen (met een gegeven straal r, in het boek was een concreet getal genoemd, maar het is denk ik net zo makkelijk om het algemene geval uit te rekenen) met zijn tegen elkaar 'geplakt', en de lucht is ertussenuit gepompt, zo, dat er (nagenoeg) een vacuum tussen hen is.
In de opdracht mag je ervan uitgaan dat er een vacuum is, en moet je de kracht berekenen die het kost om de bollen uit elkaar te trekken. Mijn broertje dacht dat je de oppervlakte van de bol moest nemen, maar kwam zelf al met de opmerking dat de luchtdruk richting de normaal naar binnen werkt, en dus niet elke richting 'even zwaar meetelt'.
Verder mocht je gebruiken dat de luchtdruk 1 bar = 100.000 Pa is, met 1 Pa = 1 N/m2.
De situatie:In de reactie van Lyrebird hierboven worden alleen maar vragen gesteld en geen antwoorden gegeven, dus ik kan me niet voorstellen dat je daar iets mee opschiet. Wat je uiteraard zoekt is een wiskundige verklaring waarom het volstaat om de oppervlakte van het grondvlak van de halve bol te vermenigvuldigen met de luchtdruk om de kracht te bepalen die op de halve bol wordt uitgeoefend.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Ik dacht zelf trouwens overigens dat je eigenlijk de integraal van de normaal (naar binnen gericht) moest nemen over de oppervlakte van een halve bol. Ik kon intuïtief ook wel inzien dat de kracht die nodig was om de bollen uit elkaar te trekken waarschijnlijk evenredig was met r2 (als je een papiertje tussen de bollen stopt, zie je dat de oppervlakte tussen hen gelijk is aan pi*r2, maar ik kon niet precies uitleggen waarom dit het goede antwoord was. Je kan het papiertje immers ook vouwen, zodat het een grotere oppervlakte heeft. Dan vallen er vast weer krachten tegen elkaar weg, maar de totale kracht blijft volgens mij niet per se even groot...)
Wie kan me hier wat inzicht over verschaffen? Ik weet nog dat ik de opgave destijds ook gemaakt heb, en dat ik hem toen ook niet helemaal snapte, maar mijn natuurkundeleraar wist me wel te overtuigen van de juistheid van de methode.
Bij het modelleren van fysische problemen is het vaak prettig om nog met infinitesimalen te werken, dus dat zal ik hier ook doen. Je idee dat je de kracht die op de halve bol wordt uitgeoefend uit kunt drukken als een integraal is correct. Beschouwen we een infinitesimaal oppervlakte elementje dS van de halve bol, dan is de kracht dFdie op dat elementje wordt uitgeoefend dF = p∙n∙dS waarbij p de luchtdruk is en n de naar binnen gerichte genormeerde normaalvector bij het elementje dS. De totale kracht die op de halve bol wordt uitgeoefend is dan de som van al deze infinitesimale bijdragen, dus F = ∫ dF = ∫ p∙n∙dS = p∙∫ n∙dS, waarbij we de integraal nemen over de oppervlakte van de halve bol. Het is evenwel niet nodig deze integraal ook echt uit te rekenen om F te bepalen.
Beschouwen we een infinitesimaal bolsegmentje met oppervlakte dA waarvan de snijvlakken evenwijdig lopen aan het grondvlak van de halve bol, dan kunnen we op grond van symmetrie overwegingen concluderen dat de resultante van de krachten op dit bolsegmentje loodrecht staat op het grondvlak van de halve bol. Immers, de componenten van de krachten evenwijdig aan het grondvlak van de bol die op elk tweetal diametraal tegenover elkaar gelegen elementjes dS van dit bolsegmentje werken zullen elkaar steeds opheffen.
De loodrechte projectie van het infinitesimale bolsegmentje op het grondvlak van de halve bol is een ring met straal ρ en dikte dρ, en dus een oppervlakte dO = 2πρ∙dρ. Zij φ de inclinatie van het bolsegmentje met het grondvlak (de 'breedtegraad'), dan geldt:
(1) dO = sin φ∙dA
De grootte van de kracht dF die op het bolsegmentje wordt uitgeoefend is gelijk aan het product van de luchtdruk p en de oppervlakte dA van het bolsegmentje, en dit weer vermenigvuldigd met cos(½π - φ) = sin φ, omdat de resultante loodrecht staat op het grondvlak en dus gelijk is aan de som van de loodrechte componenten van de krachten die op elk elementje dS van het bolsegmentje werken. Dus hebben we voor de grootte van de kracht uitgeoefend op het bolsegmentje:
(2) dF = sin φ∙p∙dA
Maar uit (1) en (2) volgt nu:
(3) dF = p∙dO
En dus:
(4) F = p∙O
aangezien ook F = 0 voor O = 0. Je ziet dus dat we de grootte van de kracht F die door de luchtdruk op de vacuum getrokken halve bol wordt uitgeoefend inderdaad kunnen berekenen door eenvoudig de luchtdruk p te vermenigvuldigen met de oppervlakte O = π∙r2 van het grondvlak van de halve bol.
Hebben we nu twee halve bollen met straal r tegen elkaar aan en is de ruimte binnenin luchtledig, dan oefent de luchtdruk op elk van de halve bollen een gelijke maar tegengesteld gerichte kracht uit, zodat de trekkracht die benodigd is om de halve bollen van elkaar te scheiden dan 2∙p∙π∙r2 bedraagt. De historische Maagdenburger halve bollen hadden een diameter van ca. 50 cm, zodat, aangenomen dat de ruimte binnenin volledig luchtledig is en aangenomen dat de luchtdruk 105 Pa bedraagt, een trekkracht van ca. 40.000 N benodigd is om de halve bollen van elkaar te scheiden.
[ Bericht 0% gewijzigd door Riparius op 30-09-2012 17:05:30 ]


Mooie post weer Riparius! Ik zal er morgen even beter naar kijken, maar het ziet er inderdaad uit als dat waar ik naar op zoek was! (wat overigens niet wil zeggen dat de post van lyrebird nutteloos was, want ik wou ook graag manieren om het op een wat intuïtieve manier aan mijn broertje te laten zien). Verder moet ik ook zeggen dat ik de vraag uit het natuurkundeboek een beetje lastig vind voor 4-vwo-ers, omdat het niet duidelijk is of je nou op je intuïtie af moet gaan of je een wat hardere argumentatie moet geven. (tegelijk wel een goede vraag voor het ontwikkelen van intuïtie voor dit soort problemen)quote:
Dank Riparius!


Ik denk niet dat je broertje iets opschiet met de post van Lyrebird. Maar het is heel goed mogelijk om het op een wat intuïtievere manier duidelijk te maken zonder echt gebruik te maken van infinitesimaalrekening als hij vertrouwd is met het voorstellen van krachten als vectoren en met het ontbinden daarvan in twee onderling loodrechte componenten (en ik mag toch hopen dat dat het geval is).quote:Op zaterdag 29 september 2012 14:25 schreef kutkloon7 het volgende:
[..]
Mooie post weer Riparius! Ik zal er morgen even beter naar kijken, maar het ziet er inderdaad uit als dat waar ik naar op zoek was! (wat overigens niet wil zeggen dat de post van lyrebird nutteloos was, want ik wou ook graag manieren om het op een wat intuïtieve manier aan mijn broertje te laten zien). Verder moet ik ook zeggen dat ik de vraag uit het natuurkundeboek een beetje lastig vind voor 4-vwo-ers, omdat het niet duidelijk is of je nou op je intuïtie af moet gaan of je een wat hardere argumentatie moet geven. (tegelijk wel een goede vraag voor het ontwikkelen van intuïtie voor dit soort problemen)
Dank Riparius!
Maak vooral een duidelijke tekening van de halve bol in zijaanzicht (dus: een halve cirkel met straal r in de kwadranten I en II van een assenstelsel en met het middelpunt van de halve cirkel in de oorsprong). Het bolsegmentje in zijaanzicht bestaat dan uit twee kleine cirkelboogjes die symmetrisch liggen ten opzichte van de y-as. Teken ook de loodrechte projecties van de cirkelboogjes op de x-as. Dan kun je aan de hand van de tekening laten zien dat de neerwaartse component van de kracht die op het bolsegmentje werkt gelijk is aan cos(½π - φ)∙p∙dA = sin φ∙p∙dA en dat dit weer gelijk is aan p∙dO omdat sin φ∙dA = dO. Daarmee heb je gerechtvaardigd dat je de grootte van de neerwaartse kracht die op de complete halve bol werkt eenvoudig kunt berekenen door het product p∙O = p∙π∙r2 te bepalen. Dit moet je dan nog met 2 vermenigvuldigen om de trekkracht te berekenen die nodig is om de twee luchtledige halve bollen van elkaar te scheiden.
[ Bericht 0% gewijzigd door Riparius op 29-09-2012 20:24:24 ]


Iemand die mijn scheikunde antwoord even wil controleren?
De vraag:
In de apotheek moet de assistent 'magnesiamelk' bereiden. Dit is een suspensie van magnesiumhydroxide. Hij voegt 150 mg Mg(OH)2 toe aan 1000 mL water.
Het is bekend dat slechts 10 mg hiervan oplost, de rest blijft als vaste stof aanwezig. Het eindvolume is nog steeds 1000 mL.
Bereken de pH van de ontstane suspensie bij 298 K.
Wat ik gedaan heb:
10*10-3g Mg(OH)2 lost op.
Mg(OH)2 = 1:2 = 20*10-3g OH-
20*10-3g in 1 L
OH- = 17,008 g mol-1
Aantal mol = aantal gram / molaire massa = 20*10-3 / 17,008 = 1,18*10-3 mol
Molariteit = aantal mol / aantal liter = 1,18*10-3 / 1 = 1,18*10-3 mol L-1
pOH = -log[OH-] = -log[1,18*10-3] = 2,92
pH = 14 - pOH = 14 - 2,92 = 11,08
Alvast bedankt.
De vraag:
In de apotheek moet de assistent 'magnesiamelk' bereiden. Dit is een suspensie van magnesiumhydroxide. Hij voegt 150 mg Mg(OH)2 toe aan 1000 mL water.
Het is bekend dat slechts 10 mg hiervan oplost, de rest blijft als vaste stof aanwezig. Het eindvolume is nog steeds 1000 mL.
Bereken de pH van de ontstane suspensie bij 298 K.
Wat ik gedaan heb:
10*10-3g Mg(OH)2 lost op.
Mg(OH)2 = 1:2 = 20*10-3g OH-
20*10-3g in 1 L
OH- = 17,008 g mol-1
Aantal mol = aantal gram / molaire massa = 20*10-3 / 17,008 = 1,18*10-3 mol
Molariteit = aantal mol / aantal liter = 1,18*10-3 / 1 = 1,18*10-3 mol L-1
pOH = -log[OH-] = -log[1,18*10-3] = 2,92
pH = 14 - pOH = 14 - 2,92 = 11,08
Alvast bedankt.


Je antwoord klopt niet en je gaat in de fout bij het dikgedrukte stuk. Hoe kan er 20 mg OH- opgesloten zitten in 10 mg Mg(OH)2?quote:Op dinsdag 2 oktober 2012 19:38 schreef Miraculously het volgende:
Iemand die mijn scheikunde antwoord even wil controleren?
De vraag:
In de apotheek moet de assistent 'magnesiamelk' bereiden. Dit is een suspensie van magnesiumhydroxide. Hij voegt 150 mg Mg(OH)2 toe aan 1000 mL water.
Het is bekend dat slechts 10 mg hiervan oplost, de rest blijft als vaste stof aanwezig. Het eindvolume is nog steeds 1000 mL.
Bereken de pH van de ontstane suspensie bij 298 K.
Wat ik gedaan heb:
10*10-3g Mg(OH)2 lost op.
Mg(OH)2 = 1:2 = 20*10-3g OH-
20*10-3g in 1 L
OH- = 17,008 g mol-1
Aantal mol = aantal gram / molaire massa = 20*10-3 / 17,008 = 1,18*10-3 mol
Molariteit = aantal mol / aantal liter = 1,18*10-3 / 1 = 1,18*10-3 mol L-1
pOH = -log[OH-] = -log[1,18*10-3] = 2,92
pH = 14 - pOH = 14 - 2,92 = 11,08
Alvast bedankt.
Je moet eerst de 10 mg Mg(OH)2 omrekenen naar een aantal mol, vervolgens bepalen hoeveel mol OH- daarin zit en dan via concentratie en pOH uiteindelijk de pH berekenen.


Dit is duidelijk ja, ik za eens kijken of hij nog zo geïnteresseerd is dat hij dit wil horen, ik begrijp het in ieder gevalquote:Op zaterdag 29 september 2012 18:04 schreef Riparius het volgende:
[..]
Ik denk niet dat je broertje iets opschiet met de post van Lyrebird. Maar het is heel goed mogelijk om het op een wat intuïtievere manier duidelijk te maken zonder echt gebruik te maken van infinitesimaalrekening als hij vertrouwd is met het voorstellen van krachten als vectoren en met het ontbinden daarvan in twee onderling loodrechte componenten (en ik mag toch hopen dat dat het geval is).
Maak vooral een duidelijke tekening van de halve bol in zijaanzicht (dus: een halve cirkel met straal r in de kwadranten I en II van een assenstelsel en met het middelpunt van de halve cirkel in de oorsprong). Het bolsegmentje in zijaanzicht bestaat dan uit twee kleine cirkelboogjes die symmetrisch liggen ten opzichte van de y-as. Teken ook de loodrechte projecties van de cirkelboogjes op de x-as. Dan kun je aan de hand van de tekening laten zien dat de neerwaartse component van de kracht die op het bolsegmentje werkt gelijk is aan cos(½π - φ)∙p∙dA = sin φ∙p∙dA en dat dit weer gelijk is aan p∙dO omdat sin φ∙dA = dO. Daarmee heb je gerechtvaardigd dat je de grootte van de neerwaartse kracht die op de complete halve bol werkt eenvoudig kunt berekenen door het product p∙O = p∙π∙r2 te bepalen. Dit moet je dan nog met 2 vermenigvuldigen om de trekkracht te berekenen die nodig is om de twee luchtledige halve bollen van elkaar te scheiden.


Hallo, zouden jullie mij kunnen helpen met wat vragen over lenzen.
1. stel ik moet van een torisch glas de sterkte opschrijven, gegeven in zo’n taboschema, hoe weet ik dan in welke richting de sferische zit en in welke richting de cilindrische sterkte?
2. transponeren, S+2,75 = C-1,75 as 160, wordt toch S1,00 = C1,75 as 70. En S-3,75 = C-0,50 as 100 wordt S-4,25 = C+0,50 as 10
3. Een plan-convexe cilinderlens heeft een kromtestraal van 8cm. De brekingsindex is 1,60, de asrichting is 90graden. Bereken de plaats van de tweede brandlijn en geef de richting aan.
Deze vraag had ik beantwoord door: (1,60-1,00)/(0,08)=7,50dpt 1/7,50=0,13m. Dit klopt, maar ik vroeg me af of ik misschein niet (1,00-1,60)/(-0,08)=7,50dpt moest doen omdat het om de tweede brandlijn gaat, of is dit bij cilinders anders? De asrichting is 90 graden. Waarom? Hoe weet je welke asrichting je moet geven? En als het om de tweede brandlijn asrichting ofzo gaat.. hoe weet je dan dat die 90 graden.
4. Een plan-convexe cilinderlens heeft een kromtestraal van 5cm, de brekingsindex is 1,50. De asrichting van de cilinder is 60graden. Bereken de plaats van de tweede brandlijn en geef de richting aan. het antwoord: oneindig en 150 graden. Waarom oneindig? Ik kom nergens op een getal uit dat ik door 0 dpt zou moeten delen, hoe moet ik op oneindig uitkomen? En waarom tel je hier bij de gegeven as wel 90 graden op en laat je bij de vorige gewoon de gegeven as staan?
5. Een concaaf-convexe cilinderlens heeft aan het eerste, concave grensvlak een kromtestraal van 13cm, aan het tweede grensvlak een kromtestraal van 8 cm. De brekingsindex is 1,52. de asrichtingen aan voor- en achterzijde zijn beide horizontaal.
a. bereken de cilindersterkte van het eerste grensvlak: (1,52-1,00)/(-0,13)=-4,00 dpt. Bereken ik dit goed of heb ik de brekingsindex verkeerd om afgetrokken… en kom ik zo toevallig op het goede antwoord uit.
b. Idem voor het tweede grensvlak: (1,00-1,52)/(-0.08)=6,50 dpt, hier m’n zelfde vraag als bij a
c. Bereken de sterkte van deze cilinderlens en geef de asrichting. : -4,00dpt+6,50dpt=2,50 dpt C2,50 as 0 graden. Waarom is de as hier 0 graden? Omdat in de inleiding staat aangegeven dat de asrichtingen horizontaal zijn?
d. Bereken de plaats van de tweede brandlijn en geef de richting aan. Hoe bereken je de tweede brandlijn? Moet ik dan van een andere asrichting uitgaan? Als ik asrichting 90 graden neem kan ik wel 1/0 doen om zo op oneindig uit te komen, maar anders zou ik het echt niet weten. Hoe moet ik nou weten wanneer welke asrichting.
6. Een cilinderlens heeft een cilindrisch eerste grensvlak met een r1 van +13cm en een cilindrisch tweede grensvlak met een r2 van +8cm. De brekingsindex is 1,52, de beide cilinderassen zijn horizontaal.
a. bereken de sterkte van het eerste cilindrische grensvlak: (1,52-1,00)/(0,13)=4,00 dpt
b. idem van het tweede grensvlak: (1,00-1,52)/(0,08)=-6,50dpt
c. bereken de sterket van de cilinderlens en geef de asrichting aan: 4+-6,50=-2,50dpt
vervolgens staat er Splan = C -2,50 as 0graden. Oke in het begin van de vraag stond beide cilinderassen zijn horizontaal.. maar als je de as aangeeft zo, dan hoort die as toch in de richting waar er geen sterkte is en in een cilinderas heb je toch wel sterkte???
d. beide brandlijnen zijn virtueel? Waarom? Dan moeten ze zich toch beide aan de zelfde kant bevinden, hoe kom je daarachter?
7. planconcaaf cilinderlens heeft aan het tweede grensvlak een kromtestraal van 17cm. Brekingsindex=1,68, asrichting 20graden. Bereken de plaats van de tweedebrandlijn en geef de richting aan. antwoord=oneindig en 110 graden. Waarom tel je er hier weer wel 90graden bij op, en hoe kom je op oneindig..
8. een torische lens heeft aan de convexe voorzijde overal een kromtestraal van 12cm. Aan de concave achterzijde is de horizontale kromtestraal 36cm en de verticale kromtestraal 72cm. De brekingsindex is 1,72. de diamter van de lens is 80 mm.
Bereken het glasvoorschrift. Hoe??
Hartelijk dank.
1. stel ik moet van een torisch glas de sterkte opschrijven, gegeven in zo’n taboschema, hoe weet ik dan in welke richting de sferische zit en in welke richting de cilindrische sterkte?
2. transponeren, S+2,75 = C-1,75 as 160, wordt toch S1,00 = C1,75 as 70. En S-3,75 = C-0,50 as 100 wordt S-4,25 = C+0,50 as 10
3. Een plan-convexe cilinderlens heeft een kromtestraal van 8cm. De brekingsindex is 1,60, de asrichting is 90graden. Bereken de plaats van de tweede brandlijn en geef de richting aan.
Deze vraag had ik beantwoord door: (1,60-1,00)/(0,08)=7,50dpt 1/7,50=0,13m. Dit klopt, maar ik vroeg me af of ik misschein niet (1,00-1,60)/(-0,08)=7,50dpt moest doen omdat het om de tweede brandlijn gaat, of is dit bij cilinders anders? De asrichting is 90 graden. Waarom? Hoe weet je welke asrichting je moet geven? En als het om de tweede brandlijn asrichting ofzo gaat.. hoe weet je dan dat die 90 graden.
4. Een plan-convexe cilinderlens heeft een kromtestraal van 5cm, de brekingsindex is 1,50. De asrichting van de cilinder is 60graden. Bereken de plaats van de tweede brandlijn en geef de richting aan. het antwoord: oneindig en 150 graden. Waarom oneindig? Ik kom nergens op een getal uit dat ik door 0 dpt zou moeten delen, hoe moet ik op oneindig uitkomen? En waarom tel je hier bij de gegeven as wel 90 graden op en laat je bij de vorige gewoon de gegeven as staan?
5. Een concaaf-convexe cilinderlens heeft aan het eerste, concave grensvlak een kromtestraal van 13cm, aan het tweede grensvlak een kromtestraal van 8 cm. De brekingsindex is 1,52. de asrichtingen aan voor- en achterzijde zijn beide horizontaal.
a. bereken de cilindersterkte van het eerste grensvlak: (1,52-1,00)/(-0,13)=-4,00 dpt. Bereken ik dit goed of heb ik de brekingsindex verkeerd om afgetrokken… en kom ik zo toevallig op het goede antwoord uit.
b. Idem voor het tweede grensvlak: (1,00-1,52)/(-0.08)=6,50 dpt, hier m’n zelfde vraag als bij a
c. Bereken de sterkte van deze cilinderlens en geef de asrichting. : -4,00dpt+6,50dpt=2,50 dpt C2,50 as 0 graden. Waarom is de as hier 0 graden? Omdat in de inleiding staat aangegeven dat de asrichtingen horizontaal zijn?
d. Bereken de plaats van de tweede brandlijn en geef de richting aan. Hoe bereken je de tweede brandlijn? Moet ik dan van een andere asrichting uitgaan? Als ik asrichting 90 graden neem kan ik wel 1/0 doen om zo op oneindig uit te komen, maar anders zou ik het echt niet weten. Hoe moet ik nou weten wanneer welke asrichting.
6. Een cilinderlens heeft een cilindrisch eerste grensvlak met een r1 van +13cm en een cilindrisch tweede grensvlak met een r2 van +8cm. De brekingsindex is 1,52, de beide cilinderassen zijn horizontaal.
a. bereken de sterkte van het eerste cilindrische grensvlak: (1,52-1,00)/(0,13)=4,00 dpt
b. idem van het tweede grensvlak: (1,00-1,52)/(0,08)=-6,50dpt
c. bereken de sterket van de cilinderlens en geef de asrichting aan: 4+-6,50=-2,50dpt
vervolgens staat er Splan = C -2,50 as 0graden. Oke in het begin van de vraag stond beide cilinderassen zijn horizontaal.. maar als je de as aangeeft zo, dan hoort die as toch in de richting waar er geen sterkte is en in een cilinderas heb je toch wel sterkte???
d. beide brandlijnen zijn virtueel? Waarom? Dan moeten ze zich toch beide aan de zelfde kant bevinden, hoe kom je daarachter?
7. planconcaaf cilinderlens heeft aan het tweede grensvlak een kromtestraal van 17cm. Brekingsindex=1,68, asrichting 20graden. Bereken de plaats van de tweedebrandlijn en geef de richting aan. antwoord=oneindig en 110 graden. Waarom tel je er hier weer wel 90graden bij op, en hoe kom je op oneindig..
8. een torische lens heeft aan de convexe voorzijde overal een kromtestraal van 12cm. Aan de concave achterzijde is de horizontale kromtestraal 36cm en de verticale kromtestraal 72cm. De brekingsindex is 1,72. de diamter van de lens is 80 mm.
Bereken het glasvoorschrift. Hoe??
Hartelijk dank.


Hoi,
Ik probeer de reactietijd uit te rekenen voor een simpele reactor, maar ik ga ergens hopeloos de mist in. Hopelijk weet één van jullie wat ik moet doen.
Ik heb twee reactors met ieder 6.000 kg lactose. Reactor 1 is in totaal 30.000 kg en reactor 2 is 10.000 kg. Het is gegeven dat beide reactors een volume van 5 m3 hebben en dat het een zero-order process is.
Verder is gegeven dat 95% van de lactose omgezet wordt en dat de conversieratio (k) van lactose gelijk is 0,008 mol/L.h Moleculaire gewicht van lactose is 342 g./mol.
Uit vorige opgaven weet ik dat de tijd die nodig is berekend kan worden met Ct = C0 - k * t
Waarbij Ct en C0 in mol/m3 zijn. 6000 kg geeft dan 6000/0,342/5000 = 3,51 mol/m3 welke Cs0 is.
Echter, dit is fout want zo krijg je voor beide reactoren dezelfde omzettingstijd terwijl deze bij reactor 1, 447 uur is en bij reactor 2, 427 uur.
Wat doe ik fout?
Ik probeer de reactietijd uit te rekenen voor een simpele reactor, maar ik ga ergens hopeloos de mist in. Hopelijk weet één van jullie wat ik moet doen.
Ik heb twee reactors met ieder 6.000 kg lactose. Reactor 1 is in totaal 30.000 kg en reactor 2 is 10.000 kg. Het is gegeven dat beide reactors een volume van 5 m3 hebben en dat het een zero-order process is.
Verder is gegeven dat 95% van de lactose omgezet wordt en dat de conversieratio (k) van lactose gelijk is 0,008 mol/L.h Moleculaire gewicht van lactose is 342 g./mol.
Uit vorige opgaven weet ik dat de tijd die nodig is berekend kan worden met Ct = C0 - k * t
Waarbij Ct en C0 in mol/m3 zijn. 6000 kg geeft dan 6000/0,342/5000 = 3,51 mol/m3 welke Cs0 is.
Echter, dit is fout want zo krijg je voor beide reactoren dezelfde omzettingstijd terwijl deze bij reactor 1, 447 uur is en bij reactor 2, 427 uur.
Wat doe ik fout?


Kun en/of moet je niet op een of andere manier de vullingsgraad van de reactor in de vergelijking verwerken? Daar zit volgens mij namelijk het enige verschil tussen beide reactoren.quote:Op dinsdag 23 oktober 2012 11:09 schreef Platina het volgende:
Hoi,
Ik probeer de reactietijd uit te rekenen voor een simpele reactor, maar ik ga ergens hopeloos de mist in. Hopelijk weet één van jullie wat ik moet doen.
Ik heb twee reactors met ieder 6.000 kg lactose. Reactor 1 is in totaal 30.000 kg en reactor 2 is 10.000 kg. Het is gegeven dat beide reactors een volume van 5 m3 hebben en dat het een zero-order process is.
Verder is gegeven dat 95% van de lactose omgezet wordt en dat de conversieratio (k) van lactose gelijk is 0,008 mol/L.h Moleculaire gewicht van lactose is 342 g./mol.
Uit vorige opgaven weet ik dat de tijd die nodig is berekend kan worden met Ct = C0 - k * t
Waarbij Ct en C0 in mol/m3 zijn. 6000 kg geeft dan 6000/0,342/5000 = 3,51 mol/m3 welke Cs0 is.
Echter, dit is fout want zo krijg je voor beide reactoren dezelfde omzettingstijd terwijl deze bij reactor 1, 447 uur is en bij reactor 2, 427 uur.
Wat doe ik fout?


Hmmm, nu je het zegt schiet mij opeens iets te binnen. Ik ga eens kijken of ik er nu uitkomquote:Op dinsdag 23 oktober 2012 13:17 schreef lyolyrc het volgende:
[..]
Kun en/of moet je niet op een of andere manier de vullingsgraad van de reactor in de vergelijking verwerken? Daar zit volgens mij namelijk het enige verschil tussen beide reactoren.
Edit: Ik ben er al uit, factor 1000 mis gerekend en schoonmaaktijd niet meegenomen want de som zegt ook dat na iedere run de reactor schoongemaakt moet worden. Dat duurt 5 uur. En aangezien (30k-10k)/5k = 4, zijn dit 4 runs extra voor reactor 2. Dat verklaard waarom die 20 uur langer duurt.
Je begint dan met 6000 kg lactose / 0,342 / 5 = 3508 mol/m3
En je houdt 300 kg lactose / 0,342 / 5 = 175 mol/m3 over.
3508-175 = 3333 mol/m3. / 0,008 mol/l (wordt dus 8 mol/m3) = 417 uur.
Voor de reactor van 10.0000 kg wordt hier 10 uur tijd bij opgeteld, en voor die van 30.000 kg 30 uur.
Te voor de hand liggend eigenlijk
[ Bericht 32% gewijzigd door Platina op 23-10-2012 16:19:20 ]


Mooi dat je het antwoord hebt gevonden, maar ik snap de uitleg niet helemaal.quote:Op dinsdag 23 oktober 2012 15:38 schreef Platina het volgende:
[..]
Hmmm, nu je het zegt schiet mij opeens iets te binnen. Ik ga eens kijken of ik er nu uitkom
Edit: Ik ben er al uit, factor 1000 mis gerekend en schoonmaaktijd niet meegenomen want de som zegt ook dat na iedere run de reactor schoongemaakt moet worden. Dat duurt 5 uur. En aangezien (30k-10k)/5k = 4, zijn dit 4 runs extra voor reactor 2. Dat verklaard waarom die 20 uur langer duurt.
Je begint dan met 6000 kg lactose / 0,342 / 5 = 3508 mol/m3
En je houdt 300 kg lactose / 0,342 / 5 = 175 mol/m3 over.
3508-175 = 3333 mol/m3. / 0,008 mol/l (wordt dus 8 mol/m3) = 417 uur.
Voor de reactor van 10.0000 kg wordt hier 10 uur tijd bij opgeteld, en voor die van 30.000 kg 30 uur.
Te voor de hand liggend eigenlijk
Hoe je de duur van de reactie uitrekent is wel duidelijk (al doe je dat naar mijn mening een beetje omslachtig), maar dat van die extra runs vind ik onduidelijk.
Wat voor opleiding doe je trouwens en op welk niveau?


Hmm, hoe kan ik die duur sneller uitrekenen dan?quote:Op dinsdag 23 oktober 2012 16:49 schreef lyolyrc het volgende:
[..]
Mooi dat je het antwoord hebt gevonden, maar ik snap de uitleg niet helemaal.
Hoe je de duur van de reactie uitrekent is wel duidelijk (al doe je dat naar mijn mening een beetje omslachtig), maar dat van die extra runs vind ik onduidelijk.
Wat voor opleiding doe je trouwens en op welk niveau?
In de opdracht staat dit over de runs:
"The reactor has a volume of 5m3. After each run the reactor has to be cleaned. It takes 5 hours to empty, clean and refill the reactor". en je hebt 10.000 kg ofwel 10 m3 en hebt dan dus 2 runs nodig.
Ik ben net begonnen met de Master in Food Technology (Wageningen). Dit is nog een Bachelor vak om mijn wiskunde bij te spijkeren (dat is wel nodig naar blijkt


Bijvoorbeeld zo: 0,95*6000/(0,342*5) = 3333 mol/m3quote:Op dinsdag 23 oktober 2012 17:04 schreef Platina het volgende:
[..]
Hmm, hoe kan ik die duur sneller uitrekenen dan?
In de opdracht staat dit over de runs:
"The reactor has a volume of 5m3. After each run the reactor has to be cleaned. It takes 5 hours to empty, clean and refill the reactor". en je hebt 10.000 kg ofwel 10 m3 en hebt dan dus 2 runs nodig.
Ik ben net begonnen met de Master in Food Technology (Wageningen). Dit is nog een Bachelor vak om mijn wiskunde bij te spijkeren (dat is wel nodig naar blijkt).
En dan verder: 3333/8 = 417 h.
Als je de 8 mol/l.h in de eerste berekening onder de deelstreep zet, kan het zelfs in één stap:
0,95*6000/(0,342*5*8) =417 h.
Zoals ik het nu lees, begrijp ik dus dat in reactor 1 in totaal 30.000 kg lactose wordt omgezet en in reactor 2 10.000 kg, telkens in batches van 6.000 kg. Dus dat betekent dat reactor 1 in totaal 5x wordt gebruikt en reactor 2 dan 2x. Is dan de totale bezettingstijd voor reactor 1 niet 5x 417 uur voor de reactie + 5x of 6x 5 uur voor het legen/schoonmaken/vullen?
Dit vind ik ook een beetje vreemd:
Heb je een dichtheid van 1000 kg/m3? Voor water geldt dat wel bij benadering, maar ook voor (een oplossing met) lactose?quote:en je hebt 10.000 kg ofwel 10 m3
Ik ben zelf overigens chemicus, maar niet opgeleid in de procestechniek en vind het wel interessant, vandaar dat ik nog even doorvraag.


Aah chemicus, helaas sloot mijn vooropleiding niet goed aan want anders had ik chemische technologie gekozen. Machtig interessante richting.quote:Op dinsdag 23 oktober 2012 17:32 schreef lyolyrc het volgende:
[..]
Bijvoorbeeld zo: 0,95*6000/(0,342*5) = 3333 mol/m3
En dan verder: 3333/8 = 417 h.
Als je de 8 mol/l.h in de eerste berekening onder de deelstreep zet, kan het zelfs in één stap:
0,95*6000/(0,342*5*8) =417 h.
Zoals ik het nu lees, begrijp ik dus dat in reactor 1 in totaal 30.000 kg lactose wordt omgezet en in reactor 2 10.000 kg, telkens in batches van 6.000 kg. Dus dat betekent dat reactor 1 in totaal 5x wordt gebruikt en reactor 2 dan 2x. Is dan de totale bezettingstijd voor reactor 1 niet 5x 417 uur voor de reactie + 5x of 6x 5 uur voor het legen/schoonmaken/vullen?
Dit vind ik ook een beetje vreemd:
[..]
Heb je een dichtheid van 1000 kg/m3? Voor water geldt dat wel bij benadering, maar ook voor (een oplossing met) lactose?
Ik ben zelf overigens chemicus, maar niet opgeleid in de procestechniek en vind het wel interessant, vandaar dat ik nog even doorvraag.
Oke, ik dacht even dat je een compleet andere methode hadquote:Bijvoorbeeld zo: 0,95*6000/(0,342*5) = 3333 mol/m3
En dan verder: 3333/8 = 417 h.
Als je de 8 mol/l.h in de eerste berekening onder de deelstreep zet, kan het zelfs in één stap:
0,95*6000/(0,342*5*8) =417 h.
In de opgave krijg je gegeven dat lactose 20% en 60% is en in beide gevallen 6.000 kg. Dit heb ik dan herleid en de aanname gedaan dat het overige gewicht water is. Dus de 20% wordt 30.000 en in batches van 5.000 kg (want 5m3). Beetje onduidelijk verwoord door mij.quote:Zoals ik het nu lees, begrijp ik dus dat in reactor 1 in totaal 30.000 kg lactose wordt omgezet en in reactor 2 10.000 kg, telkens in batches van 6.000 kg. Dus dat betekent dat reactor 1 in totaal 5x wordt gebruikt en reactor 2 dan 2x. Is dan de totale bezettingstijd voor reactor 1 niet 5x 417 uur voor de reactie + 5x of 6x 5 uur voor het legen/schoonmaken/vullen?
Over de dichtheid wordt niet gerept, dus ik heb aangenomen dat deze 1000 kg/m3 is. Wij voedingsmiddelentechnologen gebruiken nogal veel aannames, ik kan me voorstellen dat een chemicus heel wat preciezer te werk gaat.quote:Heb je een dichtheid van 1000 kg/m3? Voor water geldt dat wel bij benadering, maar ook voor (een oplossing met) lactose?


Je moet gewoon de berekeningsmethode kiezen die handig is voor jou. Misschien dat je op termijn de tussenstappen ook overslaat.quote:Op dinsdag 23 oktober 2012 17:41 schreef Platina het volgende:
[..]
Aah chemicus, helaas sloot mijn vooropleiding niet goed aan want anders had ik chemische technologie gekozen. Machtig interessante richting.
[..]
Oke, ik dacht even dat je een compleet andere methode had. Maar dus eigenlijk het versimpeld opschrijven. Vind het zelf handiger om de langere variant te gebruiken, als ik iets dan weer teruglees hoef ik niet eerst weer alle gebruikte getallen te gaan terugzoeken.
[..]
In de opgave krijg je gegeven dat lactose 20% en 60% is en in beide gevallen 6.000 kg. Dit heb ik dan herleid en de aanname gedaan dat het overige gewicht water is. Dus de 20% wordt 30.000 en in batches van 5.000 kg (want 5m3). Beetje onduidelijk verwoord door mij.
[..]
Over de dichtheid wordt niet gerept, dus ik heb aangenomen dat deze 1000 kg/m3 is. Wij voedingsmiddelentechnologen gebruiken nogal veel aannames, ik kan me voorstellen dat een chemicus heel wat preciezer te werk gaat.
Ik word inderdaad een beetje kriegelig van het door elkaar smijten van kilogrammen, liters en kubieke meters. Voor mijn reacties moest ik inderdaad preciezer zijn, maar dan heb je het ook over reacties op labschaal.


Moet het om 23:00 inleveren. Vetgedrukt zijn de vragen. Kloppen de antwoorden?
Ik twijfel erg.
In 1582 werd de gregoriaanse kalender ingevoerd.
Zoek uit welke schrikkelregeling in 1582 is afgesproken
Elk jaar dat deelbaar is door 4 of door 100 heeft 366 dagen, tenzij het jaartal deelbaar is door 400.
Waarom precies deze regeling (hoe lang is een jaar precies)? Een jaar is precies 365,2422 dagen. Zonder de schrikkelregeling zou een jaar 365 dagen duren maar met de schrikkelregeling 365,2425. Dat is veel preciezer.
Na hoeveel jaar loopt deze regeling toch weer een dag uit de pas?
365,2425-365,2422=0,0003
1/0,0003= 3333,33 jaar
Ik twijfel erg.
In 1582 werd de gregoriaanse kalender ingevoerd.
Zoek uit welke schrikkelregeling in 1582 is afgesproken
Elk jaar dat deelbaar is door 4 of door 100 heeft 366 dagen, tenzij het jaartal deelbaar is door 400.
Waarom precies deze regeling (hoe lang is een jaar precies)? Een jaar is precies 365,2422 dagen. Zonder de schrikkelregeling zou een jaar 365 dagen duren maar met de schrikkelregeling 365,2425. Dat is veel preciezer.
Na hoeveel jaar loopt deze regeling toch weer een dag uit de pas?
365,2425-365,2422=0,0003
1/0,0003= 3333,33 jaar


quote:Op zondag 28 oktober 2012 22:19 schreef anwanwanwanw het volgende:
Moet het om 23:00 inleveren. Vetgedrukt zijn de vragen. Kloppen de antwoorden?
Ik twijfel erg.
In 1582 werd de gregoriaanse kalender ingevoerd.
Zoek uit welke schrikkelregeling in 1582 is afgesproken
Elk jaar dat deelbaar is door 4 of door 100 heeft 366 dagen, tenzij het jaartal deelbaar is door 400.
Waarom precies deze regeling (hoe lang is een jaar precies)? Een jaar is precies 365,2422 dagen. Zonder de schrikkelregeling zou een jaar 365 dagen duren maar met de schrikkelregeling 365,2425. Dat is veel preciezer.
Na hoeveel jaar loopt deze regeling toch weer een dag uit de pas?
365,2425-365,2422=0,0003
1/0,0003= 3333,33 jaar
http://www.dekoepel.nl/zenit/schrikkel.htmlquote:Tabel: Enkele bekende waarden van het tropisch jaar in de geschiedenis
Callippus 4e eeuw v. Chr. 365,25 dagen 365 d 06 h
Hipparchus 2e eeuw v. Chr. 365,2465 dagen 365 d 05 h 55 m
Al-Battani ca. 900 365,2425 dagen 365 d 05 h 49 m 16 s
Alfonsische tafels 13e eeuw 365,2426 dagen 365 d 05 h 49 m 24 s
Newcomb 1896 365,242199 dagen 365 d 05 h 48 m 46 s
Juliaans jaar (gem.) 45 v. Chr. 365,2500 dagen 365 d 06 h 00 m 00 s
Gregoriaans jaar (gem.) 1582 365,2425 dagen 365 d 05 h 49 m 12 s
A. Zal wel, waar heb je dat gevonden?
B. Check, zie quote.
C. Check


In die bron staat: Op 400 jaar loopt de kalender nog geen drie uur achter. Het verschil bedraagt dus ongeveer een dag in 3200 jaarquote:Op zondag 28 oktober 2012 22:27 schreef Scuidward het volgende:
[..]
[..]
http://www.dekoepel.nl/zenit/schrikkel.html
A. Zal wel, waar heb je dat gevonden?
B. Check, zie quote.
C. Check
Dat is niet hetzelfde antwoord als bij vraag 3 bij mij.


Dat is dan een fout van je bron.quote:Op zondag 28 oktober 2012 22:31 schreef anwanwanwanw het volgende:
[..]
In die bron staat: Op 400 jaar loopt de kalender nog geen drie uur achter. Het verschil bedraagt dus ongeveer een dag in 3200 jaar
Dat is niet hetzelfde antwoord als bij vraag 3 bij mij.
400 jaar nog geen 3 uur (dus minder dan 3 uur), dan is 3200 jaar een te grove afrondingsfout van hun kant.
3 / 24 = 1 / 8
1 / 8 van 3333.33 = uhm ... 414.14 ?
Je hebt het wel goed hoor, immers 1 / 0.0003 is de juiste aanpak.


kan iemand me helpen/uitleggen hoe ik het volgende moet uitrekenen:
Construct separate 95% confidence intervals for each mean. (Round your intermediate tcrit value to 3 decimal places. Round your final answers to 2 decimal places.)
Mean Confidence interval
Xbar1= $1188 ( lower, uper)
Xbar2= $1792 (lower, upper)
de volgende statistics heb ik bij vorige vragen gekregen.
testgroup control group
Mean: $1188 $1792
Sample st. dev. $712 $800
sample n 16 14
Construct separate 95% confidence intervals for each mean. (Round your intermediate tcrit value to 3 decimal places. Round your final answers to 2 decimal places.)
Mean Confidence interval
Xbar1= $1188 ( lower, uper)
Xbar2= $1792 (lower, upper)
de volgende statistics heb ik bij vorige vragen gekregen.
testgroup control group
Mean: $1188 $1792
Sample st. dev. $712 $800
sample n 16 14


standaarddeviatie in het kwadraat * aantal metingen / aantal metingen * (aantal metingen - 1).
De uitkomst hiervan vermenigvuldigen met je gevonden t-waarde en dit dan optellen en aftrekken van je gemiddelde.
Maar helemaal 100% zeker ben ik niet.
edit: eerst de wortel nemen voordat je vermenigvuldigd met je t-waarde.
[ Bericht 13% gewijzigd door Platina op 04-11-2012 23:52:31 ]
De uitkomst hiervan vermenigvuldigen met je gevonden t-waarde en dit dan optellen en aftrekken van je gemiddelde.
Maar helemaal 100% zeker ben ik niet.
edit: eerst de wortel nemen voordat je vermenigvuldigd met je t-waarde.
[ Bericht 13% gewijzigd door Platina op 04-11-2012 23:52:31 ]


Hoi,
Graag wil ik een vraag stellen over het volgende:
• Write a class named GasTank containing:
• An instance variable named amount of type double, initialized to 0.
• An instance variable named capacity of type double.
• A constructor that accepts a parameter of type double. The value of the parameter is used to initialize the value of capacity .
• A method named addGas that accepts a parameter of type double . The value of the amount instance variable is increased by the value of the parameter. However, if the value of amount is increased beyond the value of capacity , amount is set to capacity .
• A method named useGas that accepts a parameter of type double . The value of the amount instance variable is decreased by the value of the parameter. However, if the value of amount is decreased below 0 , amount is set to 0 .
• A method named isEmpty that accepts no parameters. isEmpty returns a boolean value: true if the value of amount is less than 0.1 , and false otherwise.
• A method named isFull that accepts no parameters. isFull returns a boolean value: true if the value of amount is greater than capacity-0.1 , and false otherwise.
• A method named getGasLevel that accepts no parameters. getGasLevel returns the value of the amount instance variable.
• A method named fillUp that accepts no parameters. fillUp increases amount to capacity and returns the difference between the value of capacity and the original value of amount (that is, the amount of gas that is needed to fill the tank to capacity).
Nou heb ik al het volgende, maar ik weet niet waarom hij niet goed is..:
public class GasTank
{
private double amount = 0.0;
private double capacity;
public GasTank(double myCapacity){
capacity = myCapacity;
}
public void addGas(double myAmount){
amount = amount + myAmount;
if (amount > capacity)
amount = capacity;
}
public void useGas(double myUse){
amount = amount - myUse;
if (amount < 0)
amount = 0.0;
}
public boolean isEmpty(){
if (amount < 0.1)
return true;
else
return false;
}
public boolean isFull(){
if (amount > capacity -0.1)
return true;
else
return false;
}
public double getGasLevel(){
return amount;
}
public void fillUp(){
amount+=capacity;
return capacity-amount;
}
}
Kan iemand me helpen, zodat ik het goede antwoord weet ?
?
Graag wil ik een vraag stellen over het volgende:
• Write a class named GasTank containing:
• An instance variable named amount of type double, initialized to 0.
• An instance variable named capacity of type double.
• A constructor that accepts a parameter of type double. The value of the parameter is used to initialize the value of capacity .
• A method named addGas that accepts a parameter of type double . The value of the amount instance variable is increased by the value of the parameter. However, if the value of amount is increased beyond the value of capacity , amount is set to capacity .
• A method named useGas that accepts a parameter of type double . The value of the amount instance variable is decreased by the value of the parameter. However, if the value of amount is decreased below 0 , amount is set to 0 .
• A method named isEmpty that accepts no parameters. isEmpty returns a boolean value: true if the value of amount is less than 0.1 , and false otherwise.
• A method named isFull that accepts no parameters. isFull returns a boolean value: true if the value of amount is greater than capacity-0.1 , and false otherwise.
• A method named getGasLevel that accepts no parameters. getGasLevel returns the value of the amount instance variable.
• A method named fillUp that accepts no parameters. fillUp increases amount to capacity and returns the difference between the value of capacity and the original value of amount (that is, the amount of gas that is needed to fill the tank to capacity).
Nou heb ik al het volgende, maar ik weet niet waarom hij niet goed is..:
public class GasTank
{
private double amount = 0.0;
private double capacity;
public GasTank(double myCapacity){
capacity = myCapacity;
}
public void addGas(double myAmount){
amount = amount + myAmount;
if (amount > capacity)
amount = capacity;
}
public void useGas(double myUse){
amount = amount - myUse;
if (amount < 0)
amount = 0.0;
}
public boolean isEmpty(){
if (amount < 0.1)
return true;
else
return false;
}
public boolean isFull(){
if (amount > capacity -0.1)
return true;
else
return false;
}
public double getGasLevel(){
return amount;
}
public void fillUp(){
amount+=capacity;
return capacity-amount;
}
}
Kan iemand me helpen, zodat ik het goede antwoord weet


Kun je je code in [code]-tags plaatsen? Dan is het beter leesbaar ivm inspringen en zo.quote:Op zondag 4 november 2012 23:29 schreef superky het volgende:
Hoi,
Graag wil ik een vraag stellen over het volgende:
• Write a class named GasTank containing:
• An instance variable named amount of type double, initialized to 0.
• An instance variable named capacity of type double.
• A constructor that accepts a parameter of type double. The value of the parameter is used to initialize the value of capacity .
• A method named addGas that accepts a parameter of type double . The value of the amount instance variable is increased by the value of the parameter. However, if the value of amount is increased beyond the value of capacity , amount is set to capacity .
• A method named useGas that accepts a parameter of type double . The value of the amount instance variable is decreased by the value of the parameter. However, if the value of amount is decreased below 0 , amount is set to 0 .
• A method named isEmpty that accepts no parameters. isEmpty returns a boolean value: true if the value of amount is less than 0.1 , and false otherwise.
• A method named isFull that accepts no parameters. isFull returns a boolean value: true if the value of amount is greater than capacity-0.1 , and false otherwise.
• A method named getGasLevel that accepts no parameters. getGasLevel returns the value of the amount instance variable.
• A method named fillUp that accepts no parameters. fillUp increases amount to capacity and returns the difference between the value of capacity and the original value of amount (that is, the amount of gas that is needed to fill the tank to capacity).
Nou heb ik al het volgende, maar ik weet niet waarom hij niet goed is..:
[een hoop code]
Kan iemand me helpen, zodat ik het goede antwoord weet?


Jazeker.quote:Op dinsdag 13 november 2012 21:33 schreef thabit het volgende:
[..]
Kun je je code in [code]-tags plaatsen? Dan is het beter leesbaar ivm inspringen en zo.
| 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 | public class GasTank { private double amount = 0.0; private double capacity; public GasTank(double myCapacity){ capacity = myCapacity; } public void addGas(double myAmount){ amount = amount + myAmount; if (amount > capacity) amount = capacity; } public void useGas(double myUse){ amount = amount - myUse; if (amount < 0) amount = 0.0; } public boolean isEmpty(){ if (amount < 0.1) return true; else return false; } public boolean isFull(){ if (amount > capacity -0.1) return true; else return false; } public double getGasLevel(){ return amount; } public void fillUp(){ amount+=capacity; return capacity-amount; } } |


Het punt van code tags is dat meerdere spaties wel behouden blijven (onder andere). Als je dus gewoon je oude platte text uit je post in die code tags zet blijft het onleesbaar. Of heb je het ook op deze onleesbare manier geprogrammeerd?quote:


| 1 2 3 4 | public void fillUp() { amount += capacity; return capacity - amount; } |


U heeft gelijkt. Nogmaals bedankt voor uw hulpquote:Op woensdag 14 november 2012 09:57 schreef thabit het volgende:
[ code verwijderd ]
Zo dus. Het kan meestal ook geen kwaad om spaties om operatoren te zetten. Anyway, die methode is void gedeclareerd, terwijl hij wel een waarde returnt. Je moet dat void hier in double veranderen.


Iemand wat algemene tips over Lineaire Algebra? Momenteel bezig met quotientruimtes, restklassen en de homomorfiestelling, maar dit vak is echt niet voor mij gemaakt. Ik kan er uren lang geconcentreerd op zitten, maar zelfs met de uitwerkingen erbij snap ik er de ballen van.


Vertaal het naar het Engels en probeer dan eens te Googlen.quote:Op maandag 19 november 2012 17:49 schreef Crisisstudent het volgende:
Iemand wat algemene tips over Lineaire Algebra? Momenteel bezig met quotientruimtes, restklassen en de homomorfiestelling, maar dit vak is echt niet voor mij gemaakt. Ik kan er uren lang geconcentreerd op zitten, maar zelfs met de uitwerkingen erbij snap ik er de ballen van.


Je kan er vragen over stellen in het wiskundetopicquote:Op maandag 19 november 2012 17:49 schreef Crisisstudent het volgende:
Iemand wat algemene tips over Lineaire Algebra? Momenteel bezig met quotientruimtes, restklassen en de homomorfiestelling, maar dit vak is echt niet voor mij gemaakt. Ik kan er uren lang geconcentreerd op zitten, maar zelfs met de uitwerkingen erbij snap ik er de ballen van.


Ik heb pas een tentamen gekregen over het boek Werken met Logistiek: Supply Chain Management.
Op het tentamen vroegen ze welke 5 soorten koop je hebt.. Welke zijn dat precies?
Op het tentamen vroegen ze welke 5 soorten koop je hebt.. Welke zijn dat precies?


10+30+65=105%?quote:Op dinsdag 27 november 2012 22:15 schreef Bangarang het volgende:
Ik heb een op het oog simpele statistiekvraag, maar kom er niet helemaal uit.
Kans op wedstijd 1 winnen = 10 %
Kans op wedstrijd 2 winnen = 30%
Kans op wedstrijd 1 en 2 verliezen = 65%
Dus P(A) = 0.1
P(A^c) = 0.9
P(B) = 0.3
P(B^c) = 0.7
P(A^c en B^c) = 0,65
Gevraagd: kans op precies éen van de wedstrijden te winnen =
P(A of B) = P(A) + P(B) - P(A en B)
= 0.1 + 0.3 - P(A en B)
of
P(A of B) = P(A en B^c) + P(B en A^c)
Op beide manieren kom ik niet verder. Kan iemand mij uitleg geven? Alvast bedankt
Zijn de uitslagen onafhankelijk?


De twee wedstrijden zijn onafhankelijk ja. Kans op winnen eerste = 10% kans op winnen tweede = 30%. Kans op beide wedstrijden verliezen = 65%.quote:Op dinsdag 27 november 2012 22:31 schreef thenxero het volgende:
[..]
10+30+65=105%?
Zijn de uitslagen onafhankelijk?
If State's football team has a 10% chance of winning Saturday's game, a 30% chance of
winning two weeks from now, and a 65% chance of loosing both games, what are their
chances of winning exactly once? Assume for simplicity that no \draw/tie" is possible.
[ Bericht 9% gewijzigd door Bangarang op 27-11-2012 23:40:04 (-) ]


quote:Op dinsdag 27 november 2012 22:15 schreef Bangarang het volgende:
Ik heb een op het oog simpele statistiekvraag, maar kom er niet helemaal uit.
Kans op wedstijd 1 winnen = 10 %
Kans op wedstrijd 2 winnen = 30%
Kans op wedstrijd 1 en 2 verliezen = 65%
Dus P(A) = 0.1
P(A^c) = 0.9
P(B) = 0.3
P(B^c) = 0.7
P(A^c en B^c) = 0,65
Gevraagd: kans op precies éen van de wedstrijden te winnen =
P(A of B) = P(A) + P(B) - 2*P(A en B)
= 0.1 + 0.3 - 2* P(A en B)
P(A^c en B^c) = 1 - P( A of B) = 1 - (P(A) + P(B) - P( A en B)
0.65 = 1 - (0.1 + 0.3 - P(A en B). Hieruit volgt P(A en B) = 0.05
P(A of B) = P(A) + P(B) - P(A en B)
= 0.1 + 0.3 - 2*0.05
= 0.1 + 0.3 - 0.10 = 0.30 [/b]


Dus 90% kans dat je zaterdag verliest, 70% kans dat je over twee weken verliest. Dus de kans dat je beide verliest is vanwege onafhankelijkheid 63%. Maar het is gegeven dat dat 65% kans isquote:Op dinsdag 27 november 2012 22:34 schreef Bangarang het volgende:
[..]
De twee wedstrijden zijn onafhankelijk ja.
If State's football team has a 10% chance of winning Saturday's game, a 30% chance of
winning two weeks from now, and a 65% chance of loosing both games, what are their
chances of winning exactly once? Assume for simplicity that no \draw/tie" is possible.
Weet je zeker dat je onafhankelijkheid hebt?


Ze zijn inderdaad wel afhankelijk. Heb hem inmiddels opgelost en denk dat het goed is. Bedankt voor de moeite. Volgens mij win je 65% 0 wedstrijden, 30% 1 wedstrijd en 5% 2 wedstrijden.quote:Op dinsdag 27 november 2012 23:41 schreef thenxero het volgende:
[..]
Dus 90% kans dat je zaterdag verliest, 70% kans dat je over twee weken verliest. Dus de kans dat je beide verliest is vanwege onafhankelijkheid 63%. Maar het is gegeven dat dat 65% kans is.
Weet je zeker dat je onafhankelijkheid hebt?


Scheikunde
Bij het bepalen van kinine in tonic is de uv licht absorptie gemeten op een uv-vis spectrofotometer.
Hierbij is de tonic gemeten in oplossing in water en in oplossing in ethanol.
Bij de meting in oplossing in ethanol kwam er een veel hogere absorptie. De ethanol lijkt de meting te verstoren.
Kan dit komen doordat ethanol met kinine of met iets anders in de tonic reageert? Waarom? En waarom dan niet met water? Of mengt kinine gewoon niet goed met ethanol?
Als dit niet zo is, waarom dan wel? Ethanol zelf absorbeert nauwelijks uv licht.
En wat heeft de spleetbreedte van de uv-vis spectrofotometer voor een invloed op de meting?
Aan de metingen te zien lijkt het dat een bredere spleetbreedte een betere resolutie geeft.
Komt dit doordat er dan meer licht geabsorbeerd kan worden? Of waardoor dan wel?
Bij het bepalen van kinine in tonic is de uv licht absorptie gemeten op een uv-vis spectrofotometer.
Hierbij is de tonic gemeten in oplossing in water en in oplossing in ethanol.
Bij de meting in oplossing in ethanol kwam er een veel hogere absorptie. De ethanol lijkt de meting te verstoren.
Kan dit komen doordat ethanol met kinine of met iets anders in de tonic reageert? Waarom? En waarom dan niet met water? Of mengt kinine gewoon niet goed met ethanol?
Als dit niet zo is, waarom dan wel? Ethanol zelf absorbeert nauwelijks uv licht.
En wat heeft de spleetbreedte van de uv-vis spectrofotometer voor een invloed op de meting?
Aan de metingen te zien lijkt het dat een bredere spleetbreedte een betere resolutie geeft.
Komt dit doordat er dan meer licht geabsorbeerd kan worden? Of waardoor dan wel?


Voor ANW moet ik een aantal vragen beantwoorden over de productie van yoghurt in het groot en in het klein. De vraag hoe yoghurt wordt gemaakt heb ik al beantwoord, zie spoiler. Maar nu moet ik er een blokschema van maken. Hierin moet ik de stofstromen aangeven en het restafval in weergeven. Naar mijn idee is er geen restproduct bij de productie van yoghurt. Klopt dit?
Ook moet ik de vraag beantwoorden wat de verschillen zijn tussen de productie in het groot (fabriek) en de productie in het klein die wij gedaan hebben in het practicumlokaal. Ook moet ik 2 problemen noemen die je krijgt als je van de productie in het klein naar de productie in het groot gaat.
Hierin loop ik een beetje in vast. Het enige wat ik kan verzinnen is dat fabrieken veel goedkoper hun melk kunnen inkopen.
Iemand die me een beetje op weg wil helpen?
[ Bericht 45% gewijzigd door GlowMouse op 03-12-2012 00:08:08 ]
Ook moet ik de vraag beantwoorden wat de verschillen zijn tussen de productie in het groot (fabriek) en de productie in het klein die wij gedaan hebben in het practicumlokaal. Ook moet ik 2 problemen noemen die je krijgt als je van de productie in het klein naar de productie in het groot gaat.
Hierin loop ik een beetje in vast. Het enige wat ik kan verzinnen is dat fabrieken veel goedkoper hun melk kunnen inkopen.
Iemand die me een beetje op weg wil helpen?
[ Bericht 45% gewijzigd door GlowMouse op 03-12-2012 00:08:08 ]
mmmmmmmm


Eens even zien, extreem veel meer? Ethanol verdampt, alle potjes goed afgesloten, want je maakt ijklijnen? Heb je ook met blanco's gewerkt? Zou het raar vinden inderdaad, want ethanol heeft geen absorptie bij 350 nm. Zou je meer absorbtie verwachten als kinine minder goed oplost? Goed geschud?quote:Op woensdag 28 november 2012 00:02 schreef chermenex het volgende:
Waarom? En waarom dan niet met water? Of mengt kinine gewoon niet goed met ethanol?
Als dit niet zo is, waarom dan wel? Ethanol zelf absorbeert nauwelijks uv licht.
En, zowel een cuvet met ethanol als water parallel gemeten, er kunnen er twee in, en de tonic laten koken om de CO2 er uit te krijgen (ook moeten doen, zo'n proef)? Verder, als echte scheikunde student, wat zegt je labjournaal?
Een lagere absorptie als je de absorptie en extinctie door elkaar haalt kan je verklaren door het uitwisselen van je kinini tussen de tonic en de ethanol, zou je wel even moeten checken of dit ook daadwerkelijk kan.
Spleetbreedte, uhm ...als ik het even nazoek op internet zou een kleinere spleetbreedte moeten resulteren in een nauwkeurigere meting, omdat het binnenkomende licht dus automatisch een kleinere range heeft, en je de waarden die je vind dus kan toewijzen aan die golflengtes, terwijl je met een spleetbreedte van 4 nm dus een hogere onnauwkeurigheid hebt (staat in dit PDFje wel mooi voor benzeen.).
Volgens mij ook niet als ik jouw omschrijving zo lees, immers, alles gaat er in, en je eindigt met yoghurt. Kan het zo zijn dat de melk van 80 graden een laagje krijgt wat je ook op chocomel ziet, het bekende velletje?quote:Op vrijdag 30 november 2012 14:20 schreef lekkeryoghurt het volgende:
Naar mijn idee is er geen restproduct bij de productie van yoghurt. Klopt dit?
Verder, goedkoop melk kunnen inkopen zou ik niet als probleem zien. Wellicht moet je denken aan:
- Langer moeten roeren om dingen homogeen te krijgen.
- Andere manier van verhitten.
- Andere toevoeging van ingredienten.
Als voordeel heb je dat de verhoudingen minder gaan uit maken omdat je kilo's redelijk goed kan afwegen in tegenstelling tot milligrammen. Als in, 100L en 50 of 51L is globaal 1 op 2.
[ Bericht 2% gewijzigd door Scuidward op 30-11-2012 16:03:07 ]


Meeste stoffen zijn neutraal in hun natuurlijke vorm. Als een atoom een lading heeft geef je dat aan met X+1 dan wel X-1quote:Op zondag 2 december 2012 23:27 schreef Djeetje het volgende:
hoe weet je wat de lading is van een stof bij scheikunde ?
Wel heb je een dipoolmoment, daarvoor moet je kijken naar de elektronegativiteit van de atomen. Bekendste voorbeeld is het dipoolmoment van water. Zuurstof 'trekt' harder aan de gedeelde elektronen dan waterstof en het elektron van waterstof zal dan netto meer dichtbij het zuurstafatoom zitten waardoor deze een negatief dipoolmoment heeft en waterstof een positief dipoolmoment.
Of wat bedoel je precies?
[ Bericht 2% gewijzigd door Scuidward op 03-12-2012 21:38:03 ]


ik moet met de komende toets reactie vergelijkingen kloppend maken.quote:Op zondag 2 december 2012 23:40 schreef Scuidward het volgende:
[..]
Meeste stoffen zijn neutraal in hun natuurlijke vorm. Als een atoom een lading heeft geef je dat aan met X+1 dan wel X-1
Wel heb je een dipoolmoment, daarvoor moet je kijken naar de elektronegativiteit van de atomen. Bekendste voorbeeld is het dipoolmoment van water. Zuurstof 'trekt' harder aan de gedeelde elektronen dan waterstof en het elektron van waterstof zal dan netto meer dichtbij het zuurstafatoom zitten waardoor deze een positief dipoolmoment heeft en waterstof een negatief dipoolmoment.
Of wat bedoel je precies?
daarvoor moet ik wel weten wat voor lading een stof heeft.
bijvoorbeeld: zuurstof heeft een lading van 2.
Ik beuk jullie allemaal in elkaar.


A H2O (l) -> B H2 (g) + C O2 (g)?quote:Op zondag 2 december 2012 23:42 schreef Djeetje het volgende:
[..]
ik moet met de komende toets reactie vergelijkingen kloppend maken.
daarvoor moet ik wel weten wat voor lading een stof heeft.
bijvoorbeeld: zuurstof heeft een lading van 2.
Dat is een reactievergelijking. Een lading van 2, bedoel je O2+? Of heb je het over redoxreacties?


ja O2, maar dan die 2 lager dan de O dus niet er boven.quote:Op zondag 2 december 2012 23:49 schreef Scuidward het volgende:
[..]
A H2O (l) -> B H2 (g) + C O2 (g)?
Dat is een reactievergelijking. Een lading van 2, bedoel je O2+? Of heb je het over redoxreacties?
Ik beuk jullie allemaal in elkaar.


Dan heb je 2 zuurstofatomen, dat zegt niks over de lading maar over hoeveel atomen er in het molecuul zitten, in dit geval het zuurstofmolecuul. Gassen zijn van moleculen van die vorm.quote:Op zondag 2 december 2012 23:50 schreef Djeetje het volgende:
[..]
ja O2, maar dan die 2 lager dan de O dus niet er boven.


oo.quote:Op zondag 2 december 2012 23:51 schreef Scuidward het volgende:
[..]
Dan heb je 2 zuurstofatomen, dat zegt niks over de lading maar over hoeveel atomen er in het molecuul zitten, in dit geval het zuurstofmolecuul. Gassen zijn van moleculen van die vorm.
en hoe weet ik dan dus hoeveel zuurstofatomen er in een stof zitten ?
Ik beuk jullie allemaal in elkaar.


Stel, je hebt een stof, ethanol, CH3OH. Die heeft dus één zuurstofatoom, vier waterstofatomen en een koolstofatoom.quote:Op zondag 2 december 2012 23:52 schreef Djeetje het volgende:
[..]
oo.
en hoe weet ik dan dus hoeveel zuurstofatomen er in een stof zitten ?
Een stof met meerdere zuurstofatomen weet ik zo 1 2 3 niet


als er nou staat:quote:Op zondag 2 december 2012 23:56 schreef Scuidward het volgende:
[..]
Stel, je hebt een stof, ethanol, CH3OH. Die heeft dus één zuurstofatoom, vier waterstofatomen en een koolstofatoom.
Een stof met meerdere zuurstofatomen weet ik zo 1 2 3 niet
Ammoniak (g) --> stijstof (g) + waterstof (g)
hoe weet ik dan dat stikstof N2 is (zo staat het in mijn boek namelijk)
Ik beuk jullie allemaal in elkaar.


Dit leerde ik op de derde klas, weet dus niet of dit 100% goed is:quote:Op maandag 3 december 2012 00:09 schreef Djeetje het volgende:
[..]
als er nou staat:
Ammoniak (g) --> stijstof (g) + waterstof (g)
hoe weet ik dan dat stikstof N2 is (zo staat het in mijn boek namelijk)
Bij alle stoffen staat er een 1tje achter behalve bij:
CLaire Fietst Naar Haar Oma In BRunssum, daar staat er een 2 achter.
Dus Cl2, F2, N2, H2, O2, Br2
mmmmmmmm


En dit dan:quote:Op maandag 3 december 2012 00:13 schreef lekkeryoghurt het volgende:
[..]
Dit leerde ik op de derde klas, weet dus niet of dit 100% goed is:
Bij alle stoffen staat er een 1tje achter behalve bij:
CLaire Fietst Naar Haar Oma In BRunssum, daar staat er een 2 achter.
Dus Cl2, F2, N2, H2, O2, Br2
NH3 --> N2 (G) + H2 (G)
Waarom staat er bij NH een 3 achter ?
Want het is H2 en N2.
Ik beuk jullie allemaal in elkaar.


NH3 bestaat uit verschillende elementen en dan moet je het gewoon leren of opzoeken.quote:Op maandag 3 december 2012 00:17 schreef Djeetje het volgende:
[..]
En dit dan:
NH3 --> N2 (G) + H2 (G)
Waarom staat er bij NH een 3 achter ?
Want het is H2 en N2.
De vergelijking klopt trouwens niet omdat er aan beide kanten van het =-teken niet evenveel N'etjes en H'tjes staan. Je moet hem dan nog kloppend maken door getallen te zetten VOOR de stoffen.
Dan wordt het: 2 NH3 --> N2 (G) + 3 H2 (G)
mmmmmmmm


Je waarom slaat op waarom we het zo opschrijven. We noteren het zo omdat een molecuul nu eenmaal uit meerdere atomen bestaat. Het is een reactievergelijking, je zet iets om. Nu kunnen we het wel heel groot en uitgebreid opschrijven maar simpel volstaat in dit geval.quote:Op maandag 3 december 2012 00:17 schreef Djeetje het volgende:
[..]
En dit dan:
NH3 --> N2 (G) + H2 (G)
Waarom staat er bij NH een 3 achter ?
N heeft 3 valentie-elektronen. Waterstof (H) 1.
Dus N kan drie handen geven en H 1. En dan zijn ze verbonden.
C 4, H 1, methaan, aardgas, CH4
Benzeen, zes koolstofatomen in een ring, C6
Hopelijk is het nu duidelijker.quote:Op maandag 3 december 2012 00:09 schreef Djeetje het volgende:
[..]
als er nou staat:
Ammoniak (g) --> stijstof (g) + waterstof (g)
hoe weet ik dan dat stikstof N2 is (zo staat het in mijn boek namelijk)
Verder, stikstof is zowel de naam voor het molecuul als het atoom, net als waterstof etc.
Bij ethanol, benzeen, aspartaam en kinine heb je dat niet, die verwarring.
[ Bericht 17% gewijzigd door Scuidward op 03-12-2012 00:27:57 ]


Ik moet het dus gewoon uit me hoofd leren ?quote:Op maandag 3 december 2012 00:21 schreef Scuidward het volgende:
[..]
Je waarom slaat op waarom we het zo opschrijven. We noteren het zo omdat een molecuul nu eenmaal uit meerdere atomen bestaat. Het is een reactievergelijking, je zet iets om. Nu kunnen we het wel heel groot en uitgebreid opschrijven maar simpel volstaat in dit geval.
N heeft 3 valentie-elektronen. Waterstof (H) 1.
Dus N kan drie handen geven en H 1. En dan zijn ze verbonden.
C 4, H 1, methaan, aardgas, CH4
Benzeen, zes koolstofatomen in een ring, C6
[..]
Hopelijk is het nu duidelijker.
Verder, stikstof is zowel de naam voor het molecuul als het atoom, net als waterstof etc.
Bij ethanol, benzeen, aspartaam en kinine heb je dat niet, die verwarring.
En het staat ook niet ergens op het periodiek systeem ?
Ik beuk jullie allemaal in elkaar.


Je kan het maar het beste uit je hoofd leren, hoewel het heel simpel is eigenlijk.quote:Op maandag 3 december 2012 00:30 schreef Djeetje het volgende:
[..]
Ik moet het dus gewoon uit me hoofd leren ?
En het staat ook niet ergens op het periodiek systeem ?
Heb je een binas? Daar staat het bij mij op 66B, naamgeving chemische stoffen; enkele formules en hun namen, maar er staan een hoop moeilijkere dingen in. Ik denk dat je er nog te moeilijk naar kijkt. Toen ik op de middelbare school zat was het niet zo'n heel groot probleem. Als je de elementen kent, dan zit je wel goed.
Reactievergelijkingen kloppend maken is een kwestie van verhoudingen, je kan het zien als een grote optelsom. Alles voor de pijl moet ook aan de anderen kant van de pijl komen te staan. Een handig ezelsbruggetje hiervoor is eerst voor de pijl alle atomen op te tellen en op te schrijven, en vervolgens aan de andere kant van de pijl.
Met NH3 -> H2 + N2 krijg je dan:
- voor de pijl1xN en 3xH
- achter de pijl 2XH en 2xN
Dan kloot je wat met breuken, wiskundige gedoe, ik zeg, stel, ik heb 1 NH3 molecuul, daarmee kan ik 1/2 H2 molecuul maken en 3/2 N2 molecuul. 1/2 en 3/2, je wilt het liefst geen breuken hebben staan, dus als ik alles keer twee doe ben ik er al.
Want het is 2 NH3 -> 1 N2 + 3 H2
Dan heb je nog het opschrijven van moleculen met die kleine cijfertjes. Iets heel anders en totaal niet relevant voor het kloppend maken van reactievergelijkingen.
Je hebt organische chemie: Koolwaterstoffen.
C = koolstof = 4
H = waterstof = 1
O = zuurstof = 2
N = stikstof = 3
Soms heb je wat exotische dingen, Cl, of I, of Br, maar die, zijn allemaal 1.
Dus methanol, CH3OH. C had 4, drie gaan naar H, die andere van C gaat naar O, en die ene van O weer naar een andere H. Zo noteer je binnen deze chemie de structuur.
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Dan heb je anorganische chemie, metalen en zouten etc. Die hebben een roosterstructuur, dus dan praat je eigenlijk niet meer van moleculen maar zijn het meer kristallen. Dat is een hoop bullshit die ik je zal besparen maar zo goed als alle moleculen die jij vermoedelijk zal krijgen vallen wel onder die andere regel (als het niet al gewoon goed gegeven is).
Hoop dat je een goede leraar hebt als je evenwichtsvergelijkingen krijgt.
[ Bericht 0% gewijzigd door Scuidward op 03-12-2012 00:58:59 ]


quote:Op maandag 3 december 2012 00:53 schreef Scuidward het volgende:
[..]
Je kan het maar het beste uit je hoofd leren, hoewel het heel simpel is eigenlijk.
Heb je een binas? Daar staat het bij mij op 66B, naamgeving chemische stoffen; enkele formules en hun namen, maar er staan een hoop moeilijkere dingen in. Ik denk dat je er nog te moeilijk naar kijkt. Toen ik op de middelbare school zat was het niet zo'n heel groot probleem. Als je de elementen kent, dan zit je wel goed.
Reactievergelijkingen kloppend maken is een kwestie van verhoudingen, je kan het zien als een grote optelsom. Alles voor de pijl moet ook aan de anderen kant van de pijl komen te staan. Een handig ezelsbruggetje hiervoor is eerst voor de pijl alle atomen op te tellen en op te schrijven, en vervolgens aan de andere kant van de pijl.
Met NH3 -> H2 + N2 krijg je dan:
- voor de pijl1xN en 3xH
- achter de pijl 2XH en 2xN
Dan kloot je wat met breuken, wiskundige gedoe, ik zeg, stel, ik heb 1 NH3 molecuul, daarmee kan ik 1/2 H2 molecuul maken en 3/2 N2 molecuul. 1/2 en 3/2, je wilt het liefst geen breuken hebben staan, dus als ik alles keer twee doe ben ik er al.
Want het is 2 NH3 -> 1 N2 + 3 H2
Dan heb je nog het opschrijven van moleculen met die kleine cijfertjes. Iets heel anders en totaal niet relevant voor het kloppend maken van reactievergelijkingen.
Je hebt organische chemie: Koolwaterstoffen.
C = koolstof = 4
H = waterstof = 1
O = zuurstof = 2
N = stikstof = 3
Soms heb je wat exotische dingen, Cl, of I, of Br, maar die, zijn allemaal 1.
Dus methanol, CH3OH. C had 4, drie gaan naar H, die andere van C gaat naar O, en die ene van O weer naar een andere H. Zo noteer je binnen deze chemie de structuur.ik heb geen Binas gekregen.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Dan heb je anorganische chemie, metalen en zouten etc. Die hebben een roosterstructuur, dus dan praat je eigenlijk niet meer van moleculen maar zijn het meer kristallen. Dat is een hoop bullshit die ik je zal besparen maar zo goed als alle moleculen die jij vermoedelijk zal krijgen vallen wel onder die andere regel (als het niet al gewoon goed gegeven is).
Hoop dat je een goede leraar hebt als je evenwichtsvergelijkingen krijgt.
En bijvoorbeeld de reactie vergelijking van Methaan moet ik uit me hoofd leren ?Ik beuk jullie allemaal in elkaar.


Kan iemand mij vertellen wat de systematische naam van dit molecuul is? Ik kom er maar niet uit, en kan er op internet ook nergens iets over vinden.
CH3-CH-CH3
..........|..........
........NH3
Het is in ieder geval geen propaan-2-amine (daar is de NH3 een NH-2 groep)
CH3-CH-CH3
..........|..........
........NH3
Het is in ieder geval geen propaan-2-amine (daar is de NH3 een NH-2 groep)
Moo


De zijgroep kan dan alleen NH3+ (let op de positieve lading!) zijn. In dat geval heet de stof isopropylammonium.quote:Op maandag 3 december 2012 16:27 schreef Zuivelkoe het volgende:
Kan iemand mij vertellen wat de systematische naam van dit molecuul is? Ik kom er maar niet uit, en kan er op internet ook nergens iets over vinden.
CH3-CH-CH3
..........|..........
........NH3
Het is in ieder geval geen propaan-2-amine (daar is de NH3 een NH-2 groep)


De ontledingsreactie door verbranding van methaan onder invloed van zuurstof resulteert in een mengsel van CO2 en H2O. Dit geldt voor alle organische verbindingen. En ja, een hoop is leren en begrijpen, net als een hoop andere vakken.quote:Op maandag 3 december 2012 16:06 schreef Djeetje het volgende:
[..]
ik heb geen Binas gekregen.
En bijvoorbeeld de reactie vergelijking van Methaan moet ik uit me hoofd leren ?
Koop een binas


Misschien moet je eerst uitzoeken op welk niveau hij bezig is, voordat je zo'n advies geeft. Niet iedereen schiet veel op met een Binas tabellenboek.quote:Op maandag 3 december 2012 17:29 schreef Scuidward het volgende:
[..]
De ontledingsreactie door verbranding van methaan onder invloed van zuurstof resulteert in een mengsel van CO2 en H2O. Dit geldt voor alle organische verbindingen. En ja, een hoop is leren en begrijpen, net als een hoop andere vakken.
Koop een binas


Het punt wat ik probeerde te maken was dat een binas een goede oplossing is als je niet weet wat je uit je hoofd moet leren en wat niet. Voor de rest is scheikunde vooral oefenen.quote:Op maandag 3 december 2012 19:05 schreef lyolyrc het volgende:
[..]
Misschien moet je eerst uitzoeken op welk niveau hij bezig is, voordat je zo'n advies geeft. Niet iedereen schiet veel op met een Binas tabellenboek.
Hoop in elk geval dat zijn voornaamste vraag, reactievergelijkingen kloppend maken, nu helder is.


Ik zie Binas vooral als een naslagwerk. Wat je veel gebruikt ga je vanzelf wel onthouden, maar alles onthouden wat in Binas staat is natuurlijk onzin. Dan heb je Binas ook niet meer nodig.quote:Op maandag 3 december 2012 20:15 schreef Scuidward het volgende:
[..]
Het punt wat ik probeerde te maken was dat een binas een goede oplossing is als je niet weet wat je uit je hoofd moet leren en wat niet. Voor de rest is scheikunde vooral oefenen.
Hoop in elk geval dat zijn voornaamste vraag, reactievergelijkingen kloppend maken, nu helder is.


Ik heb een vraag betreft natuurkunde:
A. Je voert aan 3 kg aluminium 449 kJ aan warmte toe.
De beginstempratuur is 20 C. Gegeven: C aluminium = 0.88 kJ (kg*K)
Naar welk temperatuur stijgt het aluminium?
In de lesstof zijn de 5 formules besproken om het aantal joules te berekenen maar niet het aantal C of K.
Welke formule moet ik hiervoor gebruiken?
Alvast bedankt!
A. Je voert aan 3 kg aluminium 449 kJ aan warmte toe.
De beginstempratuur is 20 C. Gegeven: C aluminium = 0.88 kJ (kg*K)
Naar welk temperatuur stijgt het aluminium?
In de lesstof zijn de 5 formules besproken om het aantal joules te berekenen maar niet het aantal C of K.
Welke formule moet ik hiervoor gebruiken?
Alvast bedankt!


Soortelijke warmte is de hoeveelheid energie die nodig is in Joule om een hoeveelheid stof (hier dus in kg gegegeven) één graad in temperatuur te laten stijgen. Je hebt in principe nu alles al binnen handbereik om het uit te rekenen, namelijk:quote:Op dinsdag 4 december 2012 21:25 schreef Patronage het volgende:
Ik heb een vraag betreft natuurkunde:
A. Je voert aan 3 kg aluminium 449 kJ aan warmte toe.
De beginstempratuur is 20 C. Gegeven: C aluminium = 0.88 kJ (kg*K)
Naar welk temperatuur stijgt het aluminium?
In de lesstof zijn de 5 formules besproken om het aantal joules te berekenen maar niet het aantal C of K.
Welke formule moet ik hiervoor gebruiken?
Alvast bedankt!
- 3 kg Al @ 20 graden Celsius voeg je 449 kJ aan warmte toe
- 0.88 kJ (kg*K) suggereert dat er voor 1 kg Al 0.88 kJ nodig is om het één graad te laten stijgen.
De formule die je zoekt is denk ik Q = m c delta T en dan zoek je dus de delta T met:
Q = hoeveelheid warmte
m = 3kg
c = 0.88 kJ
Kom je er zo uit?


Ik check het morgen ff, heb het namelijk erg druk. Maar volgens mij moet dit hem zijn!quote:Op dinsdag 4 december 2012 21:34 schreef Scuidward het volgende:
[..]
Soortelijke warmte is de hoeveelheid energie die nodig is in Joule om een hoeveelheid stof (hier dus in kg gegegeven) één graad in temperatuur te laten stijgen. Je hebt in principe nu alles al binnen handbereik om het uit te rekenen, namelijk:
- 3 kg Al @ 20 graden Celsius voeg je 449 kJ aan warmte toe
- 0.88 kJ (kg*K) suggereert dat er voor 1 kg Al 0.88 kJ nodig is om het één graad te laten stijgen.
De formule die je zoekt is denk ik Q = m c delta T en dan zoek je dus de delta T met:
Q = hoeveelheid warmte
m = 3kg
c = 0.88 kJ
Kom je er zo uit?


weet niet zo goed of het hier thuishoort maar ik studeer wijsbegeerte en heb een beetje moeite met de teksten goed te begrijpen (vrij logisch), ben eigenlijk benieuwd of hier misschien wat tips/trucs voor zijn dat ik niet alles 3x opnieuw hoef te lezen. Ik hoor dit overigens ook van mijn studiegenoten dat ze dit doen maar was gewoon even benieuwd of het anders kan.


Overschrijven. Hoef je het maar 1 keer te lezen. Het schrijven zorgt ervoor dat je brein niet alleen passief (lezen) met de tekst omgaat, maar ook actief (schrijven).quote:Op maandag 10 december 2012 13:51 schreef TomasR het volgende:
weet niet zo goed of het hier thuishoort maar ik studeer wijsbegeerte en heb een beetje moeite met de teksten goed te begrijpen (vrij logisch), ben eigenlijk benieuwd of hier misschien wat tips/trucs voor zijn dat ik niet alles 3x opnieuw hoef te lezen. Ik hoor dit overigens ook van mijn studiegenoten dat ze dit doen maar was gewoon even benieuwd of het anders kan.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


ik heb dit al geprobeert maar ben dan klakkeloos aan het overnemen zonder er bij na te denken. Helpt dit dan alsnog? heb het namelijk niet bij grote teksten geprobeert omdat dit en te veel schrijfwerk is en vaak het idee heb er nog niks van te snappen.quote:Op maandag 10 december 2012 14:11 schreef Lyrebird het volgende:
[..]
Overschrijven. Hoef je het maar 1 keer te lezen. Het schrijven zorgt ervoor dat je brein niet alleen passief (lezen) met de tekst omgaat, maar ook actief (schrijven).
daarnaast om 80 pagina's per college over te schrijven is me ook net wat te veel.


quote:Op maandag 10 december 2012 14:14 schreef TomasR het volgende:
[..]
ik heb dit al geprobeertd maar ben dan klakkeloos aan het overnemen zonder er bij na te denken. Helpt dit dan alsnog? heb het namelijk niet bij grote teksten geprobeert omdat dit en te veel schrijfwerk is en vaak het idee heb er nog niks van te snappen.
daarnaast om 80 pagina's per college over te schrijven is me ook net wat te veel.
Nee, als je niet actief met de stof bezig bent, heeft het MI niet zoveel zin om te blijven schrijven. Hardop voorlezen, helpt dat? Je brein is er actiever mee bezig, als je jezelf hoort.
Onze (beta) studenten vertel ik vaak dat ze de stof leren snappen, door die aan anderen uit te leggen. Pas als je het volledig snapt, kun je iets uitleggen. Of die tactiek ook voor jou werkt, durf ik niet te zeggen.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


hardloplezen doe ik nu vaak idd. helpt wel wat maar vrij weinig nog, kzal et is proberen uit te leggen aan huisgenoten of i.d. denk dat dat idd wel goed kan helpen. dankjequote:Op maandag 10 december 2012 14:24 schreef Lyrebird het volgende:
[..]Een van de redenen dat ik een beta opleiding heb gevolgd - hoef je niet zo veel te lezen.
Nee, als je niet actief met de stof bezig bent, heeft het MI niet zoveel zin om te blijven schrijven. Hardop voorlezen, helpt dat? Je brein is er actiever mee bezig, als je jezelf hoort.
Onze (beta) studenten vertel ik vaak dat ze de stof leren snappen, door die aan anderen uit te leggen. Pas als je het volledig snapt, kun je iets uitleggen. Of die tactiek ook voor jou werkt, durf ik niet te zeggen.


Economie vraag
De vraag is :
Bereken het importaandeel in % van de gehele binnenlandse bestedingen.
En daar hoort de volgende bron bij :
Kan je de tekst niet lezen op de foto hieronder heb ik de 2 teksten/getalen die in de foto staan geschreven .
Importwaarde € 335900 miljoen ( Paarse Deel )
Binnenlandse bestedingen ( gehele circkel ) € 580200 Miljoen
Alvast bedankt!!
[ Bericht 1% gewijzigd door Beverwijker op 11-12-2012 20:03:39 (Spellingsfouten ) ]
De vraag is :
Bereken het importaandeel in % van de gehele binnenlandse bestedingen.
En daar hoort de volgende bron bij :
Kan je de tekst niet lezen op de foto hieronder heb ik de 2 teksten/getalen die in de foto staan geschreven .
Importwaarde € 335900 miljoen ( Paarse Deel )
Binnenlandse bestedingen ( gehele circkel ) € 580200 Miljoen
Alvast bedankt!!
[ Bericht 1% gewijzigd door Beverwijker op 11-12-2012 20:03:39 (Spellingsfouten ) ]


Bedankt!quote:Op dinsdag 11 december 2012 20:08 schreef bezemsteeltaart het volgende:
importaandeel/binnenlandse bestedingen x 100


Nog even over je probleem nagedacht: samenvattingen schrijven is waarschijnlijk de meest efficiente en actieve methode.quote:Op maandag 10 december 2012 23:07 schreef TomasR het volgende:
[..]
hardloplezen doe ik nu vaak idd. helpt wel wat maar vrij weinig nog, kzal et is proberen uit te leggen aan huisgenoten of i.d. denk dat dat idd wel goed kan helpen. dankje
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


kdenk dat ik dan maar markeerstift ofzo moet kopen, kan ik eerst tijdens lezen belangrijke punten benadrukken en vervolgens teruglezen om er een samenvatting van te maken. danku!quote:Op woensdag 12 december 2012 05:52 schreef Lyrebird het volgende:
[..]
Nog even over je probleem nagedacht: samenvattingen schrijven is waarschijnlijk de meest efficiente en actieve methode.


Goedemiddag allemaal 
Ik ben een voeding en dietetiek studente. Ik zoek een omgeving waar ik ''samen'' maar toch ''apart'' huiswerk kan maken. Mijn klasgenoten en vrienden zijn niet zo bezig met hun studie, wat mij demotiveert en ik een ander omgeving moet zoeken. Zit ik hier goed?
Mijn vakken biologie (anatomie en fysiologie) en scheikunde (schemie) komen overeen... Of moet ik een nieuwe topic openen? Ik ben niet zo ervaren in deze subforum.

Ik ben een voeding en dietetiek studente. Ik zoek een omgeving waar ik ''samen'' maar toch ''apart'' huiswerk kan maken. Mijn klasgenoten en vrienden zijn niet zo bezig met hun studie, wat mij demotiveert en ik een ander omgeving moet zoeken. Zit ik hier goed?
Mijn vakken biologie (anatomie en fysiologie) en scheikunde (schemie) komen overeen... Of moet ik een nieuwe topic openen? Ik ben niet zo ervaren in deze subforum.


Ik heb een vraagje over het onzekerheidsprincipe, dat me nu al enige tijd bezighoudt. Ik hoop dat iemand het zal kunnen beantwoorden:
het onzekerheidsprincipe van energie-tijd wordt steeds geformuleerd als ∆E∆t >= h/(4*π).
Ik begrijp hierbij echter niet goed waarvoor deze '∆t' staat. Als ik het goed begrepen heb, staat '∆E' voor de standaardafwijking op de energie (indien men deze als een kansverdeling beziet).
Nu wordt ∆t in mijn ogen afwisselend een andere betekenis toegekend, soms zegt men dat het de tijd is, dat het systeem in een bepaalde toestand blijft (in dit geval stelt het zelfs geen onzekerheid voor, maar eerder een gewoon tijdsinterval). En soms is het de onzekerheid op het tijdstip, dat het deeltje met die bepaalde energie E (waarop de onzekerheid ∆E is), in een bepaald punt terechtkomt.
Een laserpuls die 2 fs duurt (en een welbepaalde golflengte heeft, dus de fotonen hebben een bepaalde energie), geeft men zo onzekerheid ∆t = 2fs, omdat men niet weet, wanneer het foton uit de puls komt (en er heerst dus als bovengrens van ∆t = 2fs). Dit heeft echter niets te maken met hoe lang het systeem in een bepaalde toestand blijft.
Anderzijds zegt men dat er weinig onzekerheid is, op het grond-energieniveau bij atomen, daar elektronen daar een onbepaalde lange tijd ∆t -> ∞ kan in blijven.En de onzekerheid op de hogere energieniveau's is groter, daar het elektron slechts een beperkte tijd er kan vertoeven vooraleer het terugvalt (en men neemt de gemiddelde tijd dat het er kan verblijven als onzekerheidsinterval ∆t).
Dus ik vraag me af hoe het komt, dat men schijnbaar nu eens de ene, dan de andere betekenis aan ∆t toekent. Mogelijks kunnen ze beiden, en zijn het eigenlijk 2 onzekerheidsprincipes, maar daar ben ik niet zo zeker van momenteel. Ik hoop dat iemand dit zal kunnen ophelderen.
[ Bericht 0% gewijzigd door yarnamc op 19-12-2012 21:00:53 ]
het onzekerheidsprincipe van energie-tijd wordt steeds geformuleerd als ∆E∆t >= h/(4*π).
Ik begrijp hierbij echter niet goed waarvoor deze '∆t' staat. Als ik het goed begrepen heb, staat '∆E' voor de standaardafwijking op de energie (indien men deze als een kansverdeling beziet).
Nu wordt ∆t in mijn ogen afwisselend een andere betekenis toegekend, soms zegt men dat het de tijd is, dat het systeem in een bepaalde toestand blijft (in dit geval stelt het zelfs geen onzekerheid voor, maar eerder een gewoon tijdsinterval). En soms is het de onzekerheid op het tijdstip, dat het deeltje met die bepaalde energie E (waarop de onzekerheid ∆E is), in een bepaald punt terechtkomt.
Een laserpuls die 2 fs duurt (en een welbepaalde golflengte heeft, dus de fotonen hebben een bepaalde energie), geeft men zo onzekerheid ∆t = 2fs, omdat men niet weet, wanneer het foton uit de puls komt (en er heerst dus als bovengrens van ∆t = 2fs). Dit heeft echter niets te maken met hoe lang het systeem in een bepaalde toestand blijft.
Anderzijds zegt men dat er weinig onzekerheid is, op het grond-energieniveau bij atomen, daar elektronen daar een onbepaalde lange tijd ∆t -> ∞ kan in blijven.En de onzekerheid op de hogere energieniveau's is groter, daar het elektron slechts een beperkte tijd er kan vertoeven vooraleer het terugvalt (en men neemt de gemiddelde tijd dat het er kan verblijven als onzekerheidsinterval ∆t).
Dus ik vraag me af hoe het komt, dat men schijnbaar nu eens de ene, dan de andere betekenis aan ∆t toekent. Mogelijks kunnen ze beiden, en zijn het eigenlijk 2 onzekerheidsprincipes, maar daar ben ik niet zo zeker van momenteel. Ik hoop dat iemand dit zal kunnen ophelderen.
[ Bericht 0% gewijzigd door yarnamc op 19-12-2012 21:00:53 ]


Heb volgens mij niet de uitleg die voor jou het eureka-gevoel gaat opleveren, maar:
Het onzekerheidsprincipe komt voort uit twee grootheden die aan elkaar gerelateerd zijn. Een grote nauwkeurigheid in de ene grootheid moet daarom gepaard gaan met een kleinere nauwkeurigheid in de andere grootheid, volgens de relatie zoals jij die beschreven hebt. De betekenis die we toekennen aan de delta-T is dus een onnauwkeurigheid in de tijdsbepaling.
Dat van die lasers vind ik ook ietwat vaag, maar bij elektronen, en dan met name het aanslaan van elektronen naar een hoger gelegen schil, is het natuurlijk van belang dat je een langere meting kan uitvoeren om de nauwkeurigheid te vergroten. De grondtoestand van de elektronen kan je voor een lange tijd (stel 10 seconden) meten, maar een aangeslagen elektron zal snel willen terugvallen naar de oorspronkelijke baan, met als gevolg dat de meting van de energie van de aangeslagen toestand onnauwkeuriger is.
Beetje de inleiding van de wiki-pagina in een notendop: http://nl.wikipedia.org/wiki/Onzekerheidsrelatie_van_Heisenberg
Het onzekerheidsprincipe komt voort uit twee grootheden die aan elkaar gerelateerd zijn. Een grote nauwkeurigheid in de ene grootheid moet daarom gepaard gaan met een kleinere nauwkeurigheid in de andere grootheid, volgens de relatie zoals jij die beschreven hebt. De betekenis die we toekennen aan de delta-T is dus een onnauwkeurigheid in de tijdsbepaling.
Dat van die lasers vind ik ook ietwat vaag, maar bij elektronen, en dan met name het aanslaan van elektronen naar een hoger gelegen schil, is het natuurlijk van belang dat je een langere meting kan uitvoeren om de nauwkeurigheid te vergroten. De grondtoestand van de elektronen kan je voor een lange tijd (stel 10 seconden) meten, maar een aangeslagen elektron zal snel willen terugvallen naar de oorspronkelijke baan, met als gevolg dat de meting van de energie van de aangeslagen toestand onnauwkeuriger is.
Beetje de inleiding van de wiki-pagina in een notendop: http://nl.wikipedia.org/wiki/Onzekerheidsrelatie_van_Heisenberg


Is het (tot enkele maten groter) opzwellen van rubber handschoenen in olie een voorbeeld van degradatie (materiaal), en waarom?


Waarom, geen idee, maar volgens de wiki, jawel. Waarschijnlijk omdat oorspronkelijke materiaaleigenschappen verloren gaan. http://nl.wikipedia.org/wiki/Degradatie_(materiaal)quote:Op donderdag 20 december 2012 20:31 schreef PostScript het volgende:
Is het (tot enkele maten groter) opzwellen van rubber handschoenen in olie een voorbeeld van degradatie (materiaal), en waarom?


Aha! Bedanktquote:Op woensdag 19 december 2012 22:50 schreef Scuidward het volgende:
Heb volgens mij niet de uitleg die voor jou het eureka-gevoel gaat opleveren, maar:
Het onzekerheidsprincipe komt voort uit twee grootheden die aan elkaar gerelateerd zijn. Een grote nauwkeurigheid in de ene grootheid moet daarom gepaard gaan met een kleinere nauwkeurigheid in de andere grootheid, volgens de relatie zoals jij die beschreven hebt. De betekenis die we toekennen aan de delta-T is dus een onnauwkeurigheid in de tijdsbepaling.
Dat van die lasers vind ik ook ietwat vaag, maar bij elektronen, en dan met name het aanslaan van elektronen naar een hoger gelegen schil, is het natuurlijk van belang dat je een langere meting kan uitvoeren om de nauwkeurigheid te vergroten. De grondtoestand van de elektronen kan je voor een lange tijd (stel 10 seconden) meten, maar een aangeslagen elektron zal snel willen terugvallen naar de oorspronkelijke baan, met als gevolg dat de meting van de energie van de aangeslagen toestand onnauwkeuriger is.
Beetje de inleiding van de wiki-pagina in een notendop: http://nl.wikipedia.org/wiki/Onzekerheidsrelatie_van_Heisenberg


Niet specifiek beta maar:
Waarom is Het al dan niet defect zijn van 100 door Intel gefabriceerde computerchips een voorbeeld van kwalitatieve gegevens, terwijl de temperatuur in graden Celsius waarop elke eenheid in een steekproef van 20 stukjes hittebestendig plastic begint te smelten dat niet is (nl. kwantitatieve)?
Het is toch allebei op een numerieke schaal te meten?
Veel dank
[ Bericht 1% gewijzigd door PostScript op 22-12-2012 16:15:30 ]
Waarom is Het al dan niet defect zijn van 100 door Intel gefabriceerde computerchips een voorbeeld van kwalitatieve gegevens, terwijl de temperatuur in graden Celsius waarop elke eenheid in een steekproef van 20 stukjes hittebestendig plastic begint te smelten dat niet is (nl. kwantitatieve)?
Het is toch allebei op een numerieke schaal te meten?
Veel dank
[ Bericht 1% gewijzigd door PostScript op 22-12-2012 16:15:30 ]


Van chips verwacht je dat ze niet kapot zijn, zegt dus iets over de kwaliteit. Als je 20 stukjes plastic smelt vind je een gemiddeld smeltpunt (kwantiteit)?quote:Op zaterdag 22 december 2012 16:09 schreef PostScript het volgende:
Niet specifiek beta maar:
Waarom is Het al dan niet defect zijn van 100 door Intel gefabriceerde computerchips een voorbeeld van kwalitatieve gegevens, terwijl de temperatuur in graden Celsius waarop elke eenheid in een steekproef van 20 stukjes hittebestendig plastic begint te smelten dat niet is (nl. kwantitatieve)?
Het is toch allebei op een numerieke schaal te meten?
Veel dank


Ik vind het allebei kwantitatieve gegevens; het aantal defecten is bijvoorbeeld zeker kwantitatief net als het al dan niet defect zijn van 100 stuks.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Hmmm, als ik de wiki er bij pak, dan denk ik het volgende:quote:Op zaterdag 22 december 2012 20:06 schreef GlowMouse het volgende:
Ik vind het allebei kwantitatieve gegevens; het aantal defecten is bijvoorbeeld zeker kwantitatief net als het al dan niet defect zijn van 100 stuks.
Kwalitatief: Ja, die chip is kapot.quote:Een kwalitatieve uitspraak zegt iets zonder getallen te gebruiken: "De Domtoren is hoog" of "De Domtoren is hoger dan de Martinitoren". Een kwantitatieve uitspraak zou dit in getallen weergeven: "De Domtoren is 112 meter hoog" of "De Domtoren is 15 meter hoger dan de Martinitoren".
Kwantitatief: Voor de twintig stukken plastic vonden we deze twintig smeltpunten.
Hangt er vanaf hoe je de resultaten van de chips interpreteert gok ik. Als je eindconclusie is, van de zoveel chips waren er zoveel kapot, dan ben je weer kwantitatief bezig ja ....


Ik moet voor scheikunde de glucose concentratie in energiedrank bepalen d.m.v een titratie.
Ik wilde dit (m.b.v. een aantal vage internet pagina's) doen aan de hand van de volgende reacties:
1. C6H12O6 + 2 CU (2+) + 5 OH- ---> C6H11O7 + 3 H2O + CU2O
Deze reactie verloopt goed in mijn experiment. Hierna filter ik de neergeslagen koper(II)oxide uit het mengsel en wil ik de volgende reacties laten verlopen.
2. 4 I- + CU (2+) --> I2 + 2 CUI
De concentratie jood is dan te bepalen door een titratie met thiosulfaationen.
Het probleem zit m echter in de 2e reactie. Ik ben erachter gekomen dat de 1e reactie sowieso verloopt maar de 2e lijkt niet te verlopen. Nou is het potentiaalverschil volgens BINAS ook ong. -0,6V dus....
Daarbij zouden de OH-ionen in de oplossing ook eerder reageren met het koper dan toegevoegde jodide-ionen volgens BINAS.
Er stond op zo'n internetpagina ook dat er zwavelzuur werd gebruikt maar niet waarvoor, en het komt ook niet in de reacties voor.
Nou is mn vraag dus of iemand hier ervaring mee heeft of mij kan uitleggen wat ik fout doe.
Ik wilde dit (m.b.v. een aantal vage internet pagina's) doen aan de hand van de volgende reacties:
1. C6H12O6 + 2 CU (2+) + 5 OH- ---> C6H11O7 + 3 H2O + CU2O
Deze reactie verloopt goed in mijn experiment. Hierna filter ik de neergeslagen koper(II)oxide uit het mengsel en wil ik de volgende reacties laten verlopen.
2. 4 I- + CU (2+) --> I2 + 2 CUI
De concentratie jood is dan te bepalen door een titratie met thiosulfaationen.
Het probleem zit m echter in de 2e reactie. Ik ben erachter gekomen dat de 1e reactie sowieso verloopt maar de 2e lijkt niet te verlopen. Nou is het potentiaalverschil volgens BINAS ook ong. -0,6V dus....
Daarbij zouden de OH-ionen in de oplossing ook eerder reageren met het koper dan toegevoegde jodide-ionen volgens BINAS.
Er stond op zo'n internetpagina ook dat er zwavelzuur werd gebruikt maar niet waarvoor, en het komt ook niet in de reacties voor.
Nou is mn vraag dus of iemand hier ervaring mee heeft of mij kan uitleggen wat ik fout doe.


Hallo
Ik moet voor natuurkunde een verslag maken van een aantal proefjes. Gaat prima, alleen ben ik nu aangekomen bij het verwerken van de resultaten. Bij één proefje zijn er alleen geen concrete resultaten. Volgens het verslagmodel moet ik alles in tabellen zetten, alleen kan dat dus niet bij dat ene proefje waar ik niks concreets heb. Ik kan er eigenlijk alleen een conclusie aan vastknopen, maar dat komt later. Dus wat zouden jullie doen?
Ik moet voor natuurkunde een verslag maken van een aantal proefjes. Gaat prima, alleen ben ik nu aangekomen bij het verwerken van de resultaten. Bij één proefje zijn er alleen geen concrete resultaten. Volgens het verslagmodel moet ik alles in tabellen zetten, alleen kan dat dus niet bij dat ene proefje waar ik niks concreets heb. Ik kan er eigenlijk alleen een conclusie aan vastknopen, maar dat komt later. Dus wat zouden jullie doen?
Ik ben nie hier voor de pingpong te schpelen


Je hebt geen resultaten, maar wel een conclusie. News to me.
Blues ain't nothing but a good man feeling bad...


Wat doe je tussen de eerste en de tweede reactie? Je isoleert namelijk het ontstane koperoxide, maar hoe los je dat op om vervolgens de tweede reactie te doen?quote:Op vrijdag 4 januari 2013 19:01 schreef De-Haas het volgende:
Ik moet voor scheikunde de glucose concentratie in energiedrank bepalen d.m.v een titratie.
Ik wilde dit (m.b.v. een aantal vage internet pagina's) doen aan de hand van de volgende reacties:
1. C6H12O6 + 2 CU (2+) + 5 OH- ---> C6H11O7 + 3 H2O + CU2O
Deze reactie verloopt goed in mijn experiment. Hierna filter ik de neergeslagen koper(II)oxide uit het mengsel en wil ik de volgende reacties laten verlopen.
2. 4 I- + CU (2+) --> I2 + 2 CUI
De concentratie jood is dan te bepalen door een titratie met thiosulfaationen.
Het probleem zit m echter in de 2e reactie. Ik ben erachter gekomen dat de 1e reactie sowieso verloopt maar de 2e lijkt niet te verlopen. Nou is het potentiaalverschil volgens BINAS ook ong. -0,6V dus....
Daarbij zouden de OH-ionen in de oplossing ook eerder reageren met het koper dan toegevoegde jodide-ionen volgens BINAS.
Er stond op zo'n internetpagina ook dat er zwavelzuur werd gebruikt maar niet waarvoor, en het komt ook niet in de reacties voor.
Nou is mn vraag dus of iemand hier ervaring mee heeft of mij kan uitleggen wat ik fout doe.
Volgens mij levert de tweede reactie een klein, maar positief potentiaalverschil. Reacties met een negatief potentiaalverschil lopen helemaal niet. Dat is namelijk vergelijkbaar met voorwerpen die omhoog zouden vallen, terwijl er gewoon zwaartekracht is.
[ Bericht 0% gewijzigd door lyolyrc op 06-01-2013 19:23:42 (typo) ]


Ervaring heb ik er niet mee, en ik zou zo 1 2 3 ook niet kunnen zien waar het nu fout lijkt te gaan, welke vage internetsites heb je hiervoor gebruikt? Wellicht zie je iets over het hoofd of combineer je de verkeerde dingen?quote:Op vrijdag 4 januari 2013 19:01 schreef De-Haas het volgende:
Ik moet voor scheikunde de glucose concentratie in energiedrank bepalen d.m.v een titratie.
Ik wilde dit (m.b.v. een aantal vage internet pagina's) doen aan de hand van de volgende reacties:
1. C6H12O6 + 2 CU (2+) + 5 OH- ---> C6H11O7 + 3 H2O + CU2O
Deze reactie verloopt goed in mijn experiment. Hierna filter ik de neergeslagen koper(II)oxide uit het mengsel en wil ik de volgende reacties laten verlopen.
2. 4 I- + CU (2+) --> I2 + 2 CUI
De concentratie jood is dan te bepalen door een titratie met thiosulfaationen.
Het probleem zit m echter in de 2e reactie. Ik ben erachter gekomen dat de 1e reactie sowieso verloopt maar de 2e lijkt niet te verlopen. Nou is het potentiaalverschil volgens BINAS ook ong. -0,6V dus....
Daarbij zouden de OH-ionen in de oplossing ook eerder reageren met het koper dan toegevoegde jodide-ionen volgens BINAS.
Er stond op zo'n internetpagina ook dat er zwavelzuur werd gebruikt maar niet waarvoor, en het komt ook niet in de reacties voor.
Nou is mn vraag dus of iemand hier ervaring mee heeft of mij kan uitleggen wat ik fout doe.
In mijn boek in de tabel van standaard triiodide titraties zie ik de volgende reactie staan voor glucose en andere 'reducing sugars'.
R(C=O)H (glucose dus maar dan anders) + 3 OH- <-> RCO2- +2H2O + 2e-
1. Overmaat triiodide + NaOH toevoegen aan je sample.
2. Na 5 min HCl toevoegen en back-titrate met thiosulfate.
Je gebruikt zetmeel om het omslagpunt te vinden.
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Vergelijk het met een zwaartekrachtproefje. Je hebt een beker water, die schud je om, water valt eruit. Geen concrete resultaten, alleen een conclusie.quote:Op zondag 6 januari 2013 17:22 schreef GoodGawd het volgende:
Je hebt geen resultaten, maar wel een conclusie. News to me.
Ik ben nie hier voor de pingpong te schpelen


Het klinkt alsnog vrij vaag.quote:Op zondag 6 januari 2013 18:57 schreef Quotidien het volgende:
[..]
Vergelijk het met een zwaartekrachtproefje. Je hebt een beker water, die schud je om, water valt eruit. Geen concrete resultaten, alleen een conclusie.
Normaal zet je in de conclusie geen nieuwe dingen die niet eerder in je verslag vermeld staan dus ik zou je resultaten uitbreiden naar resultaten en discussie en in de discussie aangeven dat je proef mislukt is maar wel vermelden dat het resultaat alsnog relevant is voor je onderzoek.


Het gaat hier dus eigenlijk om een schuifweerstand en een lampje. As simple as that. Naarmate het schuifje in dit proefje naar links wordt geschoven, gaat het lampje minder fel branden omdat de weerstand groter wordt. Niks concreets dus. Er moet btw ook een diagram bij, en dat zou dan weer wel kunnen.quote:Op zondag 6 januari 2013 19:11 schreef Scuidward het volgende:
[..]
Het klinkt alsnog vrij vaag.
Normaal zet je in de conclusie geen nieuwe dingen die niet eerder in je verslag vermeld staan dus ik zou je resultaten uitbreiden naar resultaten en discussie en in de discussie aangeven dat je proef mislukt is maar wel vermelden dat het resultaat alsnog relevant is voor je onderzoek.
Ik ben nie hier voor de pingpong te schpelen


Ok, dat is in principe een prima resultaat inderdaad, enkel lastig in tabelvorm. Je zou het schuiven kunnen opsplitsen in stapjes van een kwart.quote:Op zondag 6 januari 2013 19:23 schreef Quotidien het volgende:
[..]
Het gaat hier dus eigenlijk om een schuifweerstand en een lampje. As simple as that. Naarmate het schuifje in dit proefje naar links wordt geschoven, gaat het lampje minder fel branden omdat de weerstand groter wordt. Niks concreets dus. Er moet btw ook een diagram bij, en dat zou dan weer wel kunnen.


Ik doe niets met de koperoxide, ik gebruik een overmaat koperionen om zo te bepalen hoeveel weggereageert is.quote:Op zondag 6 januari 2013 18:02 schreef lyolyrc het volgende:
[..]
Wat doe je tussen de eerste en de tweede reactie? Je isoleert namelijk het ontstane koperoxide, maar hoe los je dat op om vervolgens de tweede reactie te doen?
Volgens mij levert de tweede reactie een klein, maar positief potentiaalverschil. Reacties met een negatief potentiaalverschil lopen helemaal niet. Dat is namelijk vergelijkbaar met voorwerpen die omhoog zouden vallen, terwijl er gewoon zwaartekracht is.


quote:Op zondag 6 januari 2013 18:21 schreef Scuidward het volgende:
[..]
Ervaring heb ik er niet mee, en ik zou zo 1 2 3 ook niet kunnen zien waar het nu fout lijkt te gaan, welke vage internetsites heb je hiervoor gebruikt? Wellicht zie je iets over het hoofd of combineer je de verkeerde dingen?
In mijn boek in de tabel van standaard triiodide titraties zie ik de volgende reactie staan voor glucose en andere 'reducing sugars'.
R(C=O)H (glucose dus maar dan anders) + 3 OH- <-> RCO2- +2H2O + 2e-
1. Overmaat triiodide + NaOH toevoegen aan je sample.
2. Na 5 min HCl toevoegen en back-titrate met thiosulfate.
Je gebruikt zetmeel om het omslagpunt te vinden.Bedankt, hier heb ik wat aan. Ik ga eens kijken of het mogelijk is deze methode te gebruiken.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


quote:Op zondag 6 januari 2013 18:21 schreef Scuidward het volgende:
[..]
Ervaring heb ik er niet mee, en ik zou zo 1 2 3 ook niet kunnen zien waar het nu fout lijkt te gaan, welke vage internetsites heb je hiervoor gebruikt? Wellicht zie je iets over het hoofd of combineer je de verkeerde dingen?
In mijn boek in de tabel van standaard triiodide titraties zie ik de volgende reactie staan voor glucose en andere 'reducing sugars'.
R(C=O)H (glucose dus maar dan anders) + 3 OH- <-> RCO2- +2H2O + 2e-
1. Overmaat triiodide + NaOH toevoegen aan je sample.
2. Na 5 min HCl toevoegen en back-titrate met thiosulfate.
Je gebruikt zetmeel om het omslagpunt te vinden.R(C=O)H (glucose dus maar dan anders) + 3 OH- <-> RCO2- +2H2O + 2e-SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.
Deze reactie is dan de reductor-halfreactie.
Wat is de halfreactie van de oxidator?
Ik zat zelf te denken aan
2I3- + 2e- ----> I2 + 4I-
Of ga ik nu helemaal de verkeerde kant op?
Edit:
Ik kom ook deze reactie tegen
I3- + 2 e- ------> 3 I-
maar is die wel aan te tonen met zetmeel als indicator, of m.a.w. vormt zetmeel ook een complex met triiodide ionen?
http://en.wikipedia.org/wiki/Starch_indicator
Hier staat dat de bekende donkerblauwe kleur komt van een complex met triiodide dus dan moet dit te doen zijn. Bedankt voor de hulp en als er iets niet klopt laat het me weten.
[ Bericht 0% gewijzigd door De-Haas op 07-01-2013 22:50:56 ]


Ik heb dan nog 1 vraagje hoe kan ik de concentratie van een triiodide oplossing bepalen als ik die moet maken met joodwater en een oplossing met iodide-ionen, aangezien dit een evenwichtsreactie is.


Een vraagje over optica, niet mijn favoriete onderdeel van de natuurkunde.  Ik snap nog niet echt de begrippen en werking van bijziend en verziend. Namelijk, bij de volgende plaatjes zie je als eerste een bijziend oog en als tweede een verziend oog. Maar als ik naar de lichtstralen van het bijziend oog kijk, dan komen die samen nog voor de netvlies. Dat zou toch betekenen dat je een beeld hebt dat op zijn kop staat? Terwijl ze bij een verziend oog dan gewoon recht staan.
Ik snap nog niet echt de begrippen en werking van bijziend en verziend. Namelijk, bij de volgende plaatjes zie je als eerste een bijziend oog en als tweede een verziend oog. Maar als ik naar de lichtstralen van het bijziend oog kijk, dan komen die samen nog voor de netvlies. Dat zou toch betekenen dat je een beeld hebt dat op zijn kop staat? Terwijl ze bij een verziend oog dan gewoon recht staan.
Het technische verhaal achter lenzen (vergroting, lenzenformule) krijg ik al behoorlijk onder de knie. Maar dit nog niet echt.
http://upload.wikimedia.org/wikipedia/commons/3/30/Myopia.svg
http://upload.wikimedia.o(...)f3/Hypermetropia.svg
Het technische verhaal achter lenzen (vergroting, lenzenformule) krijg ik al behoorlijk onder de knie. Maar dit nog niet echt.
http://upload.wikimedia.org/wikipedia/commons/3/30/Myopia.svg
http://upload.wikimedia.o(...)f3/Hypermetropia.svg


Het is ook zo dat het beeld verkeerd om is (niet alleen als je bijziend bent). Je hersenen zetten het dan weer "recht". Er zijn ook wel eens experimenten gedaan waar mensen een bril droegen zodat ze alles op zijn kop zagen. Na een tijdje pasten de hersenen zich zo aan dat de proefpersonen het als normaal gingen ervaren.


De dissociatieconstate van de vergelijking (joodwater is water met jood I2 toch?):quote:Op maandag 7 januari 2013 22:24 schreef De-Haas het volgende:
Ik heb dan nog 1 vraagje hoe kan ik de concentratie van een triiodide oplossing bepalen als ik die moet maken met joodwater en een oplossing met iodide-ionen, aangezien dit een evenwichtsreactie is.
I3- <-> I2 + I-
is 1.4 x 10-3 = 0.0014
0.0014 maal de concentratie I3- = concentratie I2 maal de concentratie I-.
Dus het grootste deel zal dan I3- zijn is mijn vermoeden (in elk geval ruim 95+ %). Helaas ben ik ook even druk bezig maar ik kan morgenavond vermoedelijk wat uitgebreider nadenken mocht je er niet uit komen voor die tijd.
[ Bericht 1% gewijzigd door Scuidward op 07-01-2013 23:12:48 ]


Klopt, dat wist ik al. Maar ook al hou je daar rekening mee, dan zou bij bijziend alles 2x op zijn kop staan en bij verziend dus 1x.quote:Op maandag 7 januari 2013 23:06 schreef thenxero het volgende:
Het is ook zo dat het beeld verkeerd om is (niet alleen als je bijziend bent). Je hersenen zetten het dan weer "recht". Er zijn ook wel eens experimenten gedaan waar mensen een bril droegen zodat ze alles op zijn kop zagen. Na een tijdje pasten de hersenen zich zo aan dat de proefpersonen het als normaal gingen ervaren.


Ah zo. Je bedoelt dat als je heel erg verziend bent, dan komen die lichtstralen als het ware niet meer aan de verkeerde kant van je netvlies terecht. Dat kan ook best wel kloppen, alleen merk je er niks van omdat je dan zo verziend bent dat je toch alleen maar een waas ziet.quote:Op maandag 7 januari 2013 23:10 schreef Moos. het volgende:
[..]
Klopt, dat wist ik al. Maar ook al hou je daar rekening mee, dan zou bij bijziend alles 2x op zijn kop staan en bij verziend dus 1x.


Joodwater is idd I2(aq)quote:Op maandag 7 januari 2013 23:07 schreef Scuidward het volgende:
[..]
De dissociatieconstate van de vergelijking (joodwater is water met jood I2 toch?):
I3- <-> I2 + I-
is 1.4 x 10-3 = 0.0014
0.0014 maal de concentratie I3- = concentratie I2 maal de concentratie I-.
Dus het grootste deel zal dan I3- zijn is mijn vermoeden (in elk geval ruim 95+ %). Helaas ben ik ook even druk bezig maar ik kan morgenavond vermoedelijk wat uitgebreider nadenken mocht je er niet uit komen voor die tijd.
Het uitvoeren van de proef is gelukt, dus heel erg bedankt voor je hulp. Ik ga morgenmiddag het verslag opmaken en dan kijk ik ook wel even hiernaar maar als dit zo rond de 95% zit is dit verwaarloosbaar gezien de nauwkeurigheid van de materialen waarmee ik werk, pipetten en buretten die niet precies afleesbaar zijn e.d.
En is het niet zo dat wanneer het evenwicht verstoord wordt door het verlopen van de redoxreactie met de glucose dat het evenwicht weer hersteld wordt en er weer triiodide gevormd wordt. Dan zou het namelijk helemaal verwaarloosbaar omdat ik de reactie enige tijd heb laten doorgaan.


Heb geen idee wat ik je nu precies heb laten doen, enkel wat knip en plak werk uit wat dikkere boeken die ik op de plank heb staan vergeleken met middelbare school boeken + dan dat handige filmpje op youtube. Goed te horen dat het gelukt is anders had ik een week van je tijd verspild.quote:Op dinsdag 8 januari 2013 14:58 schreef De-Haas het volgende:
En is het niet zo dat wanneer het evenwicht verstoord wordt door het verlopen van de redoxreactie met de glucose dat het evenwicht weer hersteld wordt en er weer triiodide gevormd wordt. Dan zou het namelijk helemaal verwaarloosbaar omdat ik de reactie enige tijd heb laten doorgaan.
Maar zo werken evenwichtsreacties inderdaad. Elke keer als je iets toevoegt of weg zou halen veranderen de concentraties van de stoffen in je mengsel tot de breuk weer dezelfde k-waarde heeft bereikt. De k-waarde hangt echter wel af van de temperatuur maar het gros doe je toch op kamertemperatuur (en de schaal is kelvin dus globaal maakt het ook niet echt veel uit of je iets op 300K of 310K uitvoert).
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Volgensmij is gwn het volgende gebeurt,quote:Op dinsdag 8 januari 2013 16:21 schreef Scuidward het volgende:
[..]
Heb geen idee wat ik je nu precies heb laten doen, enkel wat knip en plak werk uit wat dikkere boeken die ik op de plank heb staan vergeleken met middelbare school boeken + dan dat handige filmpje op youtube. Goed te horen dat het gelukt is anders had ik een week van je tijd verspild.
C6H12O6 + 3 OH- + I3 (-) ----> organ. restproduct + 2H2O + 3I-
Daarna heb ik de hoeveelheid I3 (-) bepaald met een titratie met S2O3 (-) en het komt wel aardig uit dus volgensmij zit het wel snor.
Studeer jij btw scheikunde? Zo ja waar en bevalt het een beetje? Ik ben namelijk ook van plan om scheikunde te gaan studeren.


Ah, duidelijk ... dat klinkt wel goed en mooi ja. De rest zal ik je per PM sturen.quote:Op dinsdag 8 januari 2013 16:43 schreef De-Haas het volgende:
[..]
Volgensmij is gwn het volgende gebeurt,
C6H12O6 + 3 OH- + I3 (-) ----> organ. restproduct + 2H2O + 3I-
Daarna heb ik de hoeveelheid I3 (-) bepaald met een titratie met S2O3 (-) en het komt wel aardig uit dus volgensmij zit het wel snor.
Studeer jij btw scheikunde? Zo ja waar en bevalt het een beetje? Ik ben namelijk ook van plan om scheikunde te gaan studeren.


Wie o wie kan mij helpen met de volgende vraag en uitleggen welke het goede antwoord is??
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.


Dat is statistiek en dus wiskunde. Beter stel je de vraag even hier: SES / [Bèta wiskunde] Huiswerk- en vragentopicquote:Op vrijdag 18 januari 2013 10:54 schreef RedroseSK het volgende:
Wie o wie kan mij helpen met de volgende vraag en uitleggen welke het goede antwoord is??
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.


En nog een vraag: 5. De proportie geslaagden bij een tentamen wat 700 studenten gemaakt hebben is 0,60. Wat is de kans op meer dan 4 geslaagden in een steekproef van 6 willekeurig geselecteerde studenten uit deze groep van 700 studenten? (op 2 decimalen nauwkeurig)?
a) 0.19
b) 0.23
c) 0.77
d) 0.81
Ik weet hoe ik de sommen moet oplossen als het zou gaan om p=0,69 n=6 en x=4 of 5, maar niet als deze steekproef getrokken wordt uit een grotere steekproef. Wat moet ik dan doen?
a) 0.19
b) 0.23
c) 0.77
d) 0.81
Ik weet hoe ik de sommen moet oplossen als het zou gaan om p=0,69 n=6 en x=4 of 5, maar niet als deze steekproef getrokken wordt uit een grotere steekproef. Wat moet ik dan doen?


Er zijn nog meer verdelingen dan de z of t-verdeling, dus de vraag is niet volledig. Maar als het een z of een t-verdeling is, dan is het een symmetrische verdeling. Bij een symmetrische verdeling is de kans dat je minstens een bepaalde hoeveelheid x boven het gemiddelde zit is gelijk aan de kans dat je hoogstens x onder het gemiddelde zit. Als je weet wat één en tweezijdig toetsen is dan moet het nu een inkoppertje zijn.quote:Op vrijdag 18 januari 2013 10:54 schreef RedroseSK het volgende:
Wie o wie kan mij helpen met de volgende vraag en uitleggen welke het goede antwoord is??
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.


De kansverdeling hoeft helemaal niet symmetrisch te zijn, antwoord d is onjuist.quote:Op vrijdag 18 januari 2013 13:14 schreef thenxero het volgende:
[..]
Er zijn nog meer verdelingen dan de z of t-verdeling, dus de vraag is niet volledig. Maar als het een z of een t-verdeling is, dan is het een symmetrische verdeling. Bij een symmetrische verdeling is de kans dat je minstens een bepaalde hoeveelheid x boven het gemiddelde zit is gelijk aan de kans dat je hoogstens x onder het gemiddelde zit. Als je weet wat één en tweezijdig toetsen is dan moet het nu een inkoppertje zijn.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Kijk eens naar de hypergeometrische verdeling. Omdat 700 studenten al vrij veel is, kun je de binomiale verdeling als benadering pakken, die je op zijn beurt weer met een normale verdeling kunt benaderen.quote:Op vrijdag 18 januari 2013 11:39 schreef RedroseSK het volgende:
En nog een vraag: 5. De proportie geslaagden bij een tentamen wat 700 studenten gemaakt hebben is 0,60. Wat is de kans op meer dan 4 geslaagden in een steekproef van 6 willekeurig geselecteerde studenten uit deze groep van 700 studenten? (op 2 decimalen nauwkeurig)?
a) 0.19
b) 0.23
c) 0.77
d) 0.81
Ik weet hoe ik de sommen moet oplossen als het zou gaan om p=0,69 n=6 en x=4 of 5, maar niet als deze steekproef getrokken wordt uit een grotere steekproef. Wat moet ik dan doen?
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Nee maar ik snap deze vraag nog steeds niet:
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.
Ik dacht namelijk dat je bij tweezijdig toetsen moest verdubbelen (2 x 0,003) = 0,006. Maar waarom is het nu 0.0015?
23. Bij een tweezijdige toetsing is de overschrijdingskans 0.003. Wat zou de overschrijdingskans zijn bij eenzijdig toetsen bij dezelfde gegevens?
a) 0.0015
b) 0.003
c) 0.006
d) niet te bepalen zonder te weten of het een z-verdeling of t-verdeling is.
Ik dacht namelijk dat je bij tweezijdig toetsen moest verdubbelen (2 x 0,003) = 0,006. Maar waarom is het nu 0.0015?


De 0.003 is bij een tweezijdige toetsing, en is dus al verdubbeld.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


0.003 is twee keer de helft, dus de helft is 0.0015.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Bedankt voor je reactie, ik ken de binomiale verdeling, maar weet nu alsnog niet hoe ik verder moet gaan.. (n*p=420, gemiddelde & wortel (420*0,4)=12,96, standaarddeviatie) Hoe pak ik dit aan, Zou je me dit kunnen uitleggen?quote:Op vrijdag 18 januari 2013 14:17 schreef GlowMouse het volgende:
[..]
Kijk eens naar de hypergeometrische verdeling. Omdat 700 studenten al vrij veel is, kun je de binomiale verdeling als benadering pakken, die je op zijn beurt weer met een normale verdeling kunt benaderen.


Nee, n = 6 en p = 0.60. Je kunt daarna de Z-waarde berekenen.quote:Op vrijdag 18 januari 2013 16:14 schreef RedroseSK het volgende:
[..]
Bedankt voor je reactie, ik ken de binomiale verdeling, maar weet nu alsnog niet hoe ik verder moet gaan.. (n*p=420, gemiddelde & wortel (420*0,4)=12,96, standaarddeviatie) Hoe pak ik dit aan, Zou je me dit kunnen uitleggen?
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Oke, maar hoe bereken je dan met deze gegevens de Z-waarde?
Ik dacht.. misschien moet ik doen: 4.0 - 3.6 / (1.2 / wortel 700) , maar dit komt niet uit
Heb deze vraag nog nooit eerder gezien, dus heb echt geen idee hoe ik hem moet aanpakken
Ik dacht.. misschien moet ik doen: 4.0 - 3.6 / (1.2 / wortel 700) , maar dit komt niet uit
Heb deze vraag nog nooit eerder gezien, dus heb echt geen idee hoe ik hem moet aanpakken


X is binomiaal verdeeld met n = 6 en p = 0.60. Bereken P(X >= 4). Als je dit niet kunt en met wortel700 aan komt zetten, moet je je boek eens openen.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


ja maar dan bereken je toch geen z waarde? ik weet wel hoe je P (X >=4) moet berekenen via binomiale verdeling, (komt namelijk uit op 0.432) maar op welke manier betrek je dan die 700 erbij? Enkel de gegevens n=6, p=0,6 en de 4 gebruiken is niet genoeg..


Als je de 700 wilt betrekken, dan heb je de hypergeometrische verdeling nodig.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Oke, maar dat hebben wij niet gehad (vraag zat overigens wel in tentamen en niemand wist hem), wat bedoel je met de hypergeometrische verdeling? En welke berekeningen voer je dan uit?


Bedankt voor de link, had ik zelf ook al op gekeken, maar daar kom ik nog niet verder mee.
Daar gaat het om 2 verschillende groepen Voorbeeld
Stel in een bak bevinden zich 5 blauwe en 4 rode ballen. Je pakt willekeurig 3 ballen uit de bak. Hoe groot is de kans dat je (precies) twee blauwe ballen hebt gepakt?.
In dit geval is N = 9, M = 5 en n = 3. De kans op m = 2 blauwe ballen is dus ..........
Maar hoe doe je dat nu voor deze vraag, want daar zijn er immer niet 2 groepen (blauw/rood) maar een steekproef binnen een steekproef. Hoe werk je deze uit?
Daar gaat het om 2 verschillende groepen Voorbeeld
Stel in een bak bevinden zich 5 blauwe en 4 rode ballen. Je pakt willekeurig 3 ballen uit de bak. Hoe groot is de kans dat je (precies) twee blauwe ballen hebt gepakt?.
In dit geval is N = 9, M = 5 en n = 3. De kans op m = 2 blauwe ballen is dus ..........
Maar hoe doe je dat nu voor deze vraag, want daar zijn er immer niet 2 groepen (blauw/rood) maar een steekproef binnen een steekproef. Hoe werk je deze uit?


Je hebt een bak met 700 studenten, waarvan 60% rood en 40% blauw. Je pakt zes studenten uit de bak.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Oké, ik zal wel heel erg dom zijn.....................maar kom er nog steeds niet uit :-(
Ik doe :
(420 nCr 4) * (280 nCr 2) / (700 nCr 6) + (420 nCr 5) * (280 nCr 1) / (700 nCr 6)+ (420 nCr 6) / (700 nCr 6) , maaaar komt geen 1 van de 4 antwoorden uit! Wat doe ik nu weer fout?
Ik doe :
(420 nCr 4) * (280 nCr 2) / (700 nCr 6) + (420 nCr 5) * (280 nCr 1) / (700 nCr 6)+ (420 nCr 6) / (700 nCr 6) , maaaar komt geen 1 van de 4 antwoorden uit! Wat doe ik nu weer fout?


Het gaat om 'meer dan 4', dus 4 niet meetellen. Mijn fout.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Nog even een vraag over onderstaande tentamen vraag. Ik dacht dat je, om de z score te berekenen, 0.20-0.25 moest doen, omdat 0.25 het gemiddelde was en dat er dus een - getal uit zou komen. Moet je er bij deze som vanuit gaan dat het gemiddelde 0,20 is?
9. In een random steekproef van 80 eerstejaars studenten in Groningen zijn 20 thuiswonend. Wat is de waarde van de toetsingsgrootheid die toetst in hoeverre het percentage thuiswonende studenten significant lager dan 20 procent is?
a) z = -1.12
b) z = -1.03
c) z = 1.03
d) z = 1.12
9. In een random steekproef van 80 eerstejaars studenten in Groningen zijn 20 thuiswonend. Wat is de waarde van de toetsingsgrootheid die toetst in hoeverre het percentage thuiswonende studenten significant lager dan 20 procent is?
a) z = -1.12
b) z = -1.03
c) z = 1.03
d) z = 1.12


Nog zon lastige vraag: stel,een aantal gegevens uit de tabel die ik hierboven heb toegevoegd zijn weggevaagd, namelijk van type 1 het gemiddelde en de standaarddeviatie, en daarnaast van beide groepen het aantal vrijheidsgraden, de Sig (two-tailed) en de mean difference.
Hoe kan je er dan toch achterkomen wat het gemiddelde van type 1 is? (ofwel van de bovenste rij)
Hoe kan je er dan toch achterkomen wat het gemiddelde van type 1 is? (ofwel van de bovenste rij)


Wie kan mij deze vraag uitleggen:
17. Een hoogleraar wil de nulhypothese toetsen (α = .10) of het gemiddelde IQ van kinderen
op zogenaamde Jenaplanscholen hoger is dan het gemiddelde IQ van andere kinderen
(dat 100 is). Hiervoor wil deze hoogleraar een steekproef nemen van 100 willekeurig
gekozen kinderen van een Jenaplanschool. Zij gaat er daarbij vanuit dat deze scores
normaal verdeeld zullen zijn met een standaarddeviatie van 15. Wat is de power van dit
onderzoek als in werkelijkheid het gemiddelde IQ van kinderen op een Jenaplanschool
102 is?
a. Z > 101.28 - 102 / 1.5
b. Z < 101.28 - 102 / 1.5
c. Z > 101.92 - 102/ 1.5
d. Z < 101.92 - 102/ 1.5
17. Een hoogleraar wil de nulhypothese toetsen (α = .10) of het gemiddelde IQ van kinderen
op zogenaamde Jenaplanscholen hoger is dan het gemiddelde IQ van andere kinderen
(dat 100 is). Hiervoor wil deze hoogleraar een steekproef nemen van 100 willekeurig
gekozen kinderen van een Jenaplanschool. Zij gaat er daarbij vanuit dat deze scores
normaal verdeeld zullen zijn met een standaarddeviatie van 15. Wat is de power van dit
onderzoek als in werkelijkheid het gemiddelde IQ van kinderen op een Jenaplanschool
102 is?
a. Z > 101.28 - 102 / 1.5
b. Z < 101.28 - 102 / 1.5
c. Z > 101.92 - 102/ 1.5
d. Z < 101.92 - 102/ 1.5


Ik mis telkens je eigen uitwerking.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Ja dat is nou juist het probleem, ik heb geen idee hoe die 101,28 & 101,92 berekend worden.
Z waarde berekenen x - u / standaarddev.
Z waarde berekenen x - u / standaarddev.


Eerst reject region berekenen:
linkergrens daarvan is dus 1.28*15/sqrt(100)=1.92
Dan de kans dat de uitkomst in de reject region ligt. Antwoord is dus c, aannemende dat er wat haakjes ontbreken en dat de echte verdeling ook een sd van 15 heeft.
linkergrens daarvan is dus 1.28*15/sqrt(100)=1.92
Dan de kans dat de uitkomst in de reject region ligt. Antwoord is dus c, aannemende dat er wat haakjes ontbreken en dat de echte verdeling ook een sd van 15 heeft.


Ja ik moet de kritieke waarde (onder 0,10) aflezen in de tabel, maar hoe moet ik dat bekijken?
Moet ik dan z waarde zoeken die als eerst onder de 0,10 komt?
Moet ik dan z waarde zoeken die als eerst onder de 0,10 komt?


Het idee achter de vraag is dat E << K. Bij een ideaal incompressible materiaal is K oneindig groot. Indien K echter in vergelijking met de modulus geassocieerd met de vormverandering (= elasticiteitsmodulus) veel groter is, kan bij benadering worden gesteld dat het materiaal incompressible is.
Dat principe denk ik te begrijpen. Het probleem is dat ik in de war ben hoe E uit de gegeven data bepaald moet worden. Het is vast enorm simpel maar ik heb de neiging om 0.2/0.1 = 2MPa te nemen als waarde voor de elasticiteitsmodulus. Echter is volgens de beknopte uitwerking E gelijk aan 1.87MPa. Weet iemand wat ik over het hoofd zie?
Alvast enorm bedankt!


Ik heb een vraag over significantie niveaus in de statistiek. Ik vind het lastig om te bepalen wanneer ik het significantie niveau moet verdubbelen of halveren. Kan iemand mij uitleggen hoe ik goed kan onthouden wanneer ik moet verdubbelen en wanneer ik moet halveren?
Als een significantieniveau wordt gegeven, zonder dat er bij staat of het niveau geldt voor een eenzijdige of tweezijdige toets, moet je dan halveren of verdubbelen?
Ik vind het daarnaast ook lastig om te bepalen wanneer betrouwbaarheidsintervallen en significantieniveaus op elkaar aansluiten. Bijv. ik zou zeggen, een 95% BHI sluit aan op een eenzijdige toets van 5% of een tweezijdige toets van 2,5% (95 + 5 = 100% of 95 + (2x 2,5%)= 100. En volgens mij is het juist net andersom of niet?
Als een significantieniveau wordt gegeven, zonder dat er bij staat of het niveau geldt voor een eenzijdige of tweezijdige toets, moet je dan halveren of verdubbelen?
Ik vind het daarnaast ook lastig om te bepalen wanneer betrouwbaarheidsintervallen en significantieniveaus op elkaar aansluiten. Bijv. ik zou zeggen, een 95% BHI sluit aan op een eenzijdige toets van 5% of een tweezijdige toets van 2,5% (95 + 5 = 100% of 95 + (2x 2,5%)= 100. En volgens mij is het juist net andersom of niet?


Natuurlijk! 0.2/0.1 = 2GPa, echter is dat natuurlijk de compressive modulus (H). Ik moet de modulus of elasticity (E) hebben. Dan komt er inderdaad gewoon 1.87GPa uit.


Iemand tips hoe Bedrijfseconomie het beste te leren? Gewoon maken maken maken of is er een snellere manier?
Oh wacht, zie nu pas dat dit Beta shizzle is, laat maar zitten dan.
Oh wacht, zie nu pas dat dit Beta shizzle is, laat maar zitten dan.
Flesje bier


Wij hebben bij natuurkunde als opdracht gekregen iets te maken met als thema energie.
Nu willen we een setup maken met een windmolen, ventilator, dynamo en gloeilampje. Energie opwekken en omzetten, en het ziet er wel tof uit.
Is dat haalbaar? Of kunnen we beter iets anders doen? Suggesties?
Klas moet het beoordelen, dus het moet er sowieso een beetje leuk uitzien.
Nu willen we een setup maken met een windmolen, ventilator, dynamo en gloeilampje. Energie opwekken en omzetten, en het ziet er wel tof uit.
Is dat haalbaar? Of kunnen we beter iets anders doen? Suggesties?
Klas moet het beoordelen, dus het moet er sowieso een beetje leuk uitzien.
Ik ben nie hier voor de pingpong te schpelen


Je kan ook iets met water doen. Zwaartekracht, uitstroom opening blabla, lekker simpel berekeningen aan te hangen
Blues ain't nothing but a good man feeling bad...


hoi, scheikunde vraagje hier  , ik weet alle elementen die een 2tje achter zich hebben, zoals waterstof, maar in veel formules heb je gewoon H staan, dus geldt dat alleen als het element alleen staat?
, ik weet alle elementen die een 2tje achter zich hebben, zoals waterstof, maar in veel formules heb je gewoon H staan, dus geldt dat alleen als het element alleen staat?
bij een evenwicht, waarbij de ene kant in het voordeel staat, bijvoorbeeld links ( xmol naoh ofso) staat in het voordeel, moet je daar een berekening ofso mee kunnen maken? dat er dan meer mol is ? wij zijn nu met het hoofdstuk begonnen en hebben geleerd hoe je de mol berekent met de verdelingsgraad en oplosbaarheidsproduct, en we hebben evenwicht gehad, maar dat evenwicht, ze laten geen berekening zien, alleen dat de ene kant dan in het voordeel is, of hoe je zo'n evenwicht noteert,
bij een evenwicht, waarbij de ene kant in het voordeel staat, bijvoorbeeld links ( xmol naoh ofso) staat in het voordeel, moet je daar een berekening ofso mee kunnen maken? dat er dan meer mol is ? wij zijn nu met het hoofdstuk begonnen en hebben geleerd hoe je de mol berekent met de verdelingsgraad en oplosbaarheidsproduct, en we hebben evenwicht gehad, maar dat evenwicht, ze laten geen berekening zien, alleen dat de ene kant dan in het voordeel is, of hoe je zo'n evenwicht noteert,


Wat is nou je vraag eigenlijk ofso?quote:Op maandag 28 januari 2013 06:39 schreef lazypenguin het volgende:
hoi, scheikunde vraagje hier, ik weet alle elementen die een 2tje achter zich hebben, zoals waterstof, maar in veel formules heb je gewoon H staan, dus geldt dat alleen als het element alleen staat?
bij een evenwicht, waarbij de ene kant in het voordeel staat, bijvoorbeeld links ( xmol naoh ofso) staat in het voordeel, moet je daar een berekening ofso mee kunnen maken? dat er dan meer mol is ? wij zijn nu met het hoofdstuk begonnen en hebben geleerd hoe je de mol berekent met de verdelingsgraad en oplosbaarheidsproduct, en we hebben evenwicht gehad, maar dat evenwicht, ze laten geen berekening zien, alleen dat de ene kant dan in het voordeel is, of hoe je zo'n evenwicht noteert,


Die 2 achter H, N, O, F, Cl. Br of I betekent dat er twee dezelfde atomen aan elkaar verbonden zijn. Er zweven dus bijvoorbeeld geen losse atomen zuurstof (O) door de lucht, maar twee atomen zuurstof zijn aan elkaar gebonden en vormen moleculair zuurstof (O2). In moleculen waarin verschillende elementen voorkomen, kan het wel voorkomen dat er maar een atoom van een soort voorkomt, of juist veel meer. Denk bijvoorbeeld aan de stof die het meest voorkomt in aardgas, methaan. Dat heeft als formule CH4. Er zijn in zo'n molecuul dus een koolstofatoom en vier waterstofatomen aanwezig.quote:Op maandag 28 januari 2013 06:39 schreef lazypenguin het volgende:
hoi, scheikunde vraagje hier, ik weet alle elementen die een 2tje achter zich hebben, zoals waterstof, maar in veel formules heb je gewoon H staan, dus geldt dat alleen als het element alleen staat?
Beter vraag je je docent dan om een uitwerking van de opgaves die je niet begrijpt. Eventueel kun je hier opgaves posten die je niet begrijpt, nadat je uiteraard eerst zelf hebt geprobeerd om een opgave te maken.quote:bij een evenwicht, waarbij de ene kant in het voordeel staat, bijvoorbeeld links ( xmol naoh ofso) staat in het voordeel, moet je daar een berekening ofso mee kunnen maken? dat er dan meer mol is ? wij zijn nu met het hoofdstuk begonnen en hebben geleerd hoe je de mol berekent met de verdelingsgraad en oplosbaarheidsproduct, en we hebben evenwicht gehad, maar dat evenwicht, ze laten geen berekening zien, alleen dat de ene kant dan in het voordeel is, of hoe je zo'n evenwicht noteert,


dank je, ik zal er dan nog een naar kijken en proberen een voorbeeld som te plaatsen als ik het geprobeerd heb uit te werkenquote:Op maandag 28 januari 2013 11:06 schreef lyolyrc het volgende:
[..]
Die 2 achter H, N, O, F, Cl. Br of I betekent dat er twee dezelfde atomen aan elkaar verbonden zijn. Er zweven dus bijvoorbeeld geen losse atomen zuurstof (O) door de lucht, maar twee atomen zuurstof zijn aan elkaar gebonden en vormen moleculair zuurstof (O2). In moleculen waarin verschillende elementen voorkomen, kan het wel voorkomen dat er maar een atoom van een soort voorkomt, of juist veel meer. Denk bijvoorbeeld aan de stof die het meest voorkomt in aardgas, methaan. Dat heeft als formule CH4. Er zijn in zo'n molecuul dus een koolstofatoom en vier waterstofatomen aanwezig.
[..]
Beter vraag je je docent dan om een uitwerking van de opgaves die je niet begrijpt. Eventueel kun je hier opgaves posten die je niet begrijpt, nadat je uiteraard eerst zelf hebt geprobeerd om een opgave te maken.


Misschien bedoel je met voordeel dat het evenwicht nog niet aanwezig is in de oplossing, dus dat het uit balans is. Dan kan je met behulp van het oplosbaarheidsproduct de juiste verdelingsgraad bepalen.quote:Op maandag 28 januari 2013 06:39 schreef lazypenguin het volgende:
bij een evenwicht, waarbij de ene kant in het voordeel staat, bijvoorbeeld links ( xmol naoh ofso) staat in het voordeel, moet je daar een berekening ofso mee kunnen maken? dat er dan meer mol is ? wij zijn nu met het hoofdstuk begonnen en hebben geleerd hoe je de mol berekent met de verdelingsgraad en oplosbaarheidsproduct, en we hebben evenwicht gehad, maar dat evenwicht, ze laten geen berekening zien, alleen dat de ene kant dan in het voordeel is, of hoe je zo'n evenwicht noteert,


Het volgende is iets wat me blijft storen, hoewel het redelijk basic zou moeten zijn.
Bij het beschouwen van rotaties geldt dat de som van alle momenten rond een as gelijk is aan de inertie rond die as vermenigvuldigd met de hoekversnelling. Maar dikwijls, indien er geen vaste as is, kan ik meerdere assen kiezen waarrond een netto moment bestaat. Betekent dit dan dat het object rond meerdere assen tegelijkertijd roteert? Bijvoorbeeld een balk waar langs de zijkanten tegenwerkende krachten op werken, neemt men een punt in een midden dan is er een netto moment, neemt men het punt aan de zijkant ook, dus er is een hoekversnelling rond beide punten. Dit lijkt me tamelijk vreemd eigenlijk, hopelijk kan iemand dit ophelderen.
Bij het beschouwen van rotaties geldt dat de som van alle momenten rond een as gelijk is aan de inertie rond die as vermenigvuldigd met de hoekversnelling. Maar dikwijls, indien er geen vaste as is, kan ik meerdere assen kiezen waarrond een netto moment bestaat. Betekent dit dan dat het object rond meerdere assen tegelijkertijd roteert? Bijvoorbeeld een balk waar langs de zijkanten tegenwerkende krachten op werken, neemt men een punt in een midden dan is er een netto moment, neemt men het punt aan de zijkant ook, dus er is een hoekversnelling rond beide punten. Dit lijkt me tamelijk vreemd eigenlijk, hopelijk kan iemand dit ophelderen.


ja klopt ! ddat bedoelde ik , dank je! zal ik ook mee proberen te oefenenquote:Op maandag 28 januari 2013 18:07 schreef Scuidward het volgende:
[..]
Misschien bedoel je met voordeel dat het evenwicht nog niet aanwezig is in de oplossing, dus dat het uit balans is. Dan kan je met behulp van het oplosbaarheidsproduct de juiste verdelingsgraad bepalen.


Een theatervoorstelling trekt 200 bezoekers. Een kinderkaartje kost €2,00 en een kaartje voor volwassenen kost €3,50. In totaal is er voor €580,00 aan inkomsten door de kaartverkoop. Bereken hoeveel kinderen er in de zaal zitten.
Hoe kun je dat nou zeggen? Alsof het aantal kinderen precies in verhouding staat met het aantal volwassenen. Ik bedoel, er kunnen 160 volwassenen in de zaal zitten tegenover 10 kinderen, 0 volwassenen tegen 290 kinderen, 100 volwassenen tegen 115 kinderen, dan kom je allemaal op €580,00 uit.
Alsof het aantal kinderen precies in verhouding staat met het aantal volwassenen. Ik bedoel, er kunnen 160 volwassenen in de zaal zitten tegenover 10 kinderen, 0 volwassenen tegen 290 kinderen, 100 volwassenen tegen 115 kinderen, dan kom je allemaal op €580,00 uit.
Hoe kun je dat nou zeggen?


Haha nog niet helemaal wakker.
Maar dan nog is dat niet helemaal te zegggen, toch? In de voorbeeldopgave staat bijvoorbeeld 10x en 2y (het gaat over tien schriften en 2 boeken die gekocht moeten worden). Bij de vraag waar ik mee zit weet je alleen dat er 200 bezoekers waren, en €580,00 aan inkomsten. Je kunt alsnog een scheve verhouding hebben.
[ Bericht 46% gewijzigd door Ypmaha op 08-02-2013 10:06:44 ]
Maar dan nog is dat niet helemaal te zegggen, toch? In de voorbeeldopgave staat bijvoorbeeld 10x en 2y (het gaat over tien schriften en 2 boeken die gekocht moeten worden). Bij de vraag waar ik mee zit weet je alleen dat er 200 bezoekers waren, en €580,00 aan inkomsten. Je kunt alsnog een scheve verhouding hebben.
[ Bericht 46% gewijzigd door Ypmaha op 08-02-2013 10:06:44 ]


Het valt wel te berekenen. Noem het aantal kinderen x en het aantal volwassenen 200-x. Stel dan een vergelijking op met het aantal kinderen, het aantal volwassenen en de prijzen die de kaartjes voor die groepen kosten.quote:Op vrijdag 8 februari 2013 09:46 schreef Ypmaha het volgende:
Haha nog niet helemaal wakker.
Maar dan nog is dat niet helemaal te zegggen, toch? In de voorbeeldopgave staat bijvoorbeeld 10x en 2y (het gaat over tien schriften en 2 boeken die gekocht moeten worden). Bij de vraag waar ik mee zit weet je alleen dat er 200 bezoekers waren, en €580,00 aan inkomsten. Je kunt alsnog een scheve verhouding hebben.


Ik ben op zoek naar een manier waarop je de bitrate kunt berekenen voor:
- het lezen van een tekst op papier of digitaal
- het luisteren naar een audioboek op CD.
Weet zelf net wat een bitrate is, dus kan mezelf ook niet heel erg op weg helpen.
- het lezen van een tekst op papier of digitaal
- het luisteren naar een audioboek op CD.
Weet zelf net wat een bitrate is, dus kan mezelf ook niet heel erg op weg helpen.


Deze vraag is niet te beantwoorden als je niet eerst tenminste specificeert hoeveel verschillende tekens er moeten kunnen worden onderscheiden c.q. hoe die tekens zijn gecodeerd als ze digitaal gelezen worden, en hoe snel de tekst wordt gelezen. Het lezen van een stuk Chinees vanaf papier is iets heel anders dan het lezen van een stuk Nederlands vanaf papier. En bij digitaal uitlezen van een tekst moet je je bijvoorbeeld afvragen hoeveel bits er voor de codering van elk teken worden gebruikt. Een stukje ASCII tekst is iets anders dan een stukje Unicode tekst.quote:Op dinsdag 12 februari 2013 21:11 schreef Jiveje het volgende:
Ik ben op zoek naar een manier waarop je de bitrate kunt berekenen voor:
- het lezen van een tekst op papier of digitaal
Deze vraag is wel te beantwoorden, hoewel je ook deze vraag nauwkeuriger zou moeten formuleren. Ik ga er maar even van uit dat je standaard audio CD's bedoelt die voldoen aan de Red Book specificatie, want als je iets anders bedoelt, bijvoorbeeld MP3 bestanden die toevallig op een CD zijn opgeslagen, dan wordt het weer een heel ander verhaal.quote:- het luisteren naar een audioboek op CD.
Het CD audio systeem werkt met een uitgekiende foutcorrectie, dus zou je ook moeten vertellen of je nu de raw bit rate bedoelt of de netto bit rate die uit het systeem komt na foutcorrectie.
CD audio werkt met twee kanalen (stereo) elk met een 16-bits lineare kwantisatie en een sample frequentie van 44,1 kHz, dus dat komt (netto) neer op 2∙16∙44100 bits per seconde oftewel 1411200 bits per seconde.
Je moet niet je onwetendheid als excuus proberen te gebruiken om geen initiatief te ontplooien, met een beetje googelen is hier genoeg over te vinden. Ik vraag me wel af wat je hier verder mee wil.quote:Weet zelf net wat een bitrate is, dus kan mezelf ook niet heel erg op weg helpen.


Ik moet een commercial maken voor Engels + Script schrijven voor de Tower Of London.
Alleen ik kan echt niets bedenken.
Iemand idee om een commercial voor de Tower Of London te maken ?
Alleen ik kan echt niets bedenken.
Iemand idee om een commercial voor de Tower Of London te maken ?


Verkeerde draad. Hier worden enkel bètavragen beantwoord. Het lijkt me trouwens vrij gemakkelijk om zelf iets goeds te bedenken aangezien er genoeg informatie te vinden is over dit gebouw en je met deze informatie gemakkelijk een spotje kan bedenken. Bedenk hoe je deze informatie kan gebruiken om mensen te verleiden om dit historische gebouw te bezoeken.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Een grappig verhaaltje hierover. Bij de demonstratie van de CD door Philips (de uitvinder van de hardware, Sony droeg bij aan de software) werd een schijfje doormidden gebroken om te demonstreren dat je zelfs dan nog de muziek zou kunnen beluisteren.quote:Op dinsdag 12 februari 2013 22:51 schreef Riparius het volgende:
Het CD audio systeem werkt met een uitgekiende foutcorrectie, dus zou je ook moeten vertellen of je nu de raw bit rate bedoelt of de netto bit rate die uit het systeem komt na foutcorrectie.
Jiveje, Riparius heeft jou goed op weg geholpen. Over de CD heeft hij genoeg verteld dat je er nu zelf wel wijs uit moet komen. Voor de tekst moet je vooral eens kijken naar hoe letters door computersoftware worden verwerkt, begin eens met te zoeken naar de verschillende coderingstechniekjes zoals ASCII en Unicode. Bedenk hoeveel tekens er gecodeerd moeten worden en hoeveel bits je dus minimaal nodig hebt om dit aantal tekens te kunnen coderen. Hoeveel mogelijke combinaties van ene en nullen zijn er bij X bits?
Voor een CD hebben ze niet voor niets gekozen voor een X aantal bits voor het betrouwbaar reproduceren van geluid, dat is gebaseerd op het frequentiesbereik van het menselijk gehoor, op frequentiesverschillen die wij nog kunnen waarnemen en op het terug een analoog signaal (sinusoïdes) vormen na digitalisaties. Het immense analoge bereik van de frequenties wordt verdeeld over een beperkt aantal stappen. Op basis hiervan wordt bepaald hoeveel bits er nodig zijn om alle frequenties weer te kunnen geven. De frequentie is gekozen omdat het bekend is dat wanneer je een analoog signaal digitaliseert dat je dan minstens 2 keer de maximale frequenties (20 kHz) nodig hebt om van dat digitale signaal terug hetzelfde analoge signaal te maken. Als je wat informatie opzoekt op de Engelstalige Wikipedia dan zal je de naam van die theorie wel tegenkomen.
[ Bericht 11% gewijzigd door Bram_van_Loon op 13-02-2013 18:04:43 ]
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Dat lijkt me redelijk excessief. De spindel kan het schijfje dan niet eens meer goed vasthouden, laat staan afspelen. En nee, zo goed is de foutcorrectie nu ook weer niet ... Ik meen me te herinneren dat volgens de specificaties van het rode boekje gaps tot ongeveer 2,5 mm nog opgevangen kunnen worden zonder gevolgen, maar het kritische punt is dan de servo tracking van de laser die het daarbij, of al veel eerder, kan laten afweten in minder goede loopwerken.quote:Op woensdag 13 februari 2013 17:55 schreef Bram_van_Loon het volgende:
[..]
Een grappig verhaaltje hierover. Bij de demonstratie van de CD door Philips (de uitvinder van de hardware, Sony droeg bij aan de software) werd een schijfje doormidden gebroken om te demonstreren dat je zelfs dan nog de muziek zou kunnen beluisteren.
Vroeger waren er talrijke broodje aap verhalen over de vermeende onverwoestbaarheid van de audio CD, net zo goed als er nu minstens zulke onzinnige verhalen de ronde doen over de vermeende korte levensduur van CD's (en DVD's). Mensen hebben kennelijk een sterke behoefte om ongehinderd door enige kennis van zaken of realiteitszin te overdrijven.
Een hele tijd geleden werd ik hier op het forum zo ongeveer voor leugenaar uitgemaakt toen ik vertelde dat ik heel wat CD's heb staan die inmiddels meer dan kwart eeuw oud zijn en die nog altijd in onberispelijke staat verkeren, zonder C2 errors (en dat is, evenals vele andere karakteristieken, ook na te meten op een Plextor drive met het programma Plextools Pro XL).


Het is niet moeilijk.quote:Op vrijdag 8 februari 2013 09:43 schreef Ypmaha het volgende:
Een theatervoorstelling trekt 200 bezoekers. Een kinderkaartje kost €2,00 en een kaartje voor volwassenen kost €3,50. In totaal is er voor €580,00 aan inkomsten door de kaartverkoop. Bereken hoeveel kinderen er in de zaal zitten.
Hoe kun je dat nou zeggen?Alsof het aantal kinderen precies in verhouding staat met het aantal volwassenen. Ik bedoel, er kunnen 160 volwassenen in de zaal zitten tegenover 10 kinderen, 0 volwassenen tegen 290 kinderen, 100 volwassenen tegen 115 kinderen, dan kom je allemaal op €580,00 uit.
Je weet dat:
2x + 3.5y = 580
x+y = 200
Je drukt x uit in y of andersom en berekent x of y. Daarna is het een koud kunstje toch?


Ik neem aan dat ze niet echt dat schijfje hebben afgespeeld maar het werd volgens een docent van mij wel echt doormidden gebroken om het statement te maken dat de foutencorrectie zeer goed was. Het verhaal diende als illustratie van de sterke foutencorrectie.quote:Op woensdag 13 februari 2013 18:29 schreef Riparius het volgende:
[..]
Dat lijkt me redelijk excessief. De spindel kan het schijfje dan niet eens meer goed vasthouden, laat staan afspelen. En nee, zo goed is de foutcorrectie nu ook weer niet ... Ik meen me te herinneren dat volgens de specificaties van het rode boekje gaps tot ongeveer 2,5 mm nog opgevangen kunnen worden zonder gevolgen, maar het kritische punt is dan de servo tracking van de laser die het daarbij, of al veel eerder, kan laten afweten in minder goede loopwerken.
Zolang je apparatuur goed werkt en je geen gekke dingen doet gaat dat natuurlijk prima. Heb je ze veel afgespeeld in al die tijd?quote:Een hele tijd geleden werd ik hier op het forum zo ongeveer voor leugenaar uitgemaakt toen ik vertelde dat ik heel wat CD's heb staan die inmiddels meer dan kwart eeuw oud zijn en die nog altijd in onberispelijke staat verkeren, zonder C2 errors (en dat is, evenals vele andere karakteristieken, ook na te meten op een Plextor drive met het programma Plextools Pro XL).
Mensen geven naturlijk al snel het voorwerp de schuld wanneer ze zelf onhandig met het voorwerp omgaan. Hoeveel mensen pakken het schijfje niet daar vast waar de data staat en laten per ongeluk eens het schijfje, al dan niet in een hoesje, vallen? Dat kan gebeuren maar geef dan niet de CD de schuld.
Ik heb trouwens een slechte ervaring met de Plextor-DVD-readers/writers. Ik heb er een gehad die na slechts een paar jaar (2?) ineens van de ene op de andere dag niet meer kon lezen (kon blijkbaar wel nog schrijven afgaande op informatie die ik had gevonden). Het zal wel pech zijn, bij elke merk doet 1 op de X apparaten niet wat het zou moeten doen.
[ Bericht 5% gewijzigd door Bram_van_Loon op 13-02-2013 20:21:10 ]
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Daar is een hoop op af te dingen hoor. Philips wilde oorspronkelijk een 14 bits lineaire kwantisatie omdat ze dat mooi genoeg vonden, maar Sony wist toen zijn 16 bits systeem door te drukken waarmee ze al wat ervaring hadden in de vorm van losse converters (de legendarische PCM-F1). Er bestonden destijds (eind jaren '70) helemaal geen bruikbare harddisks en ook geen andere opslagmedia met voldoende capaciteit om pakweg een uurtje digitale audio in hoge kwaliteit op te kunnen slaan. De enig werkbare optie was om het digitale audiosignaal om te zetten naar een analoog (!) videosignaal dat met een videorecorder kon worden opgenomen. Dat kon dan zowel een (semi-)professionele machine zijn (destijds bijvoorbeeld een U-Matic), alsook een consumentenrecorder met het Betamax of het VHS systeem, want ook die hadden voldoende bandbreedte. Iets later leidde het idee om een LPCM signaal om te zetten naar een (pseudo-)videosignaal tot de ontwikkeling van de DAT recorders, die evenals videorecorders met een roterende koppentrommel moesten werken om de noodzakelijke bandbreedte te realiseren, met alle mechanische ellende van dien.quote:Op woensdag 13 februari 2013 17:55 schreef Bram_van_Loon het volgende:
[..]
Voor een CD hebben ze niet voor niets gekozen voor een X aantal bits voor het betrouwbaar reproduceren van geluid, dat is gebaseerd op het frequentiesbereik van het menselijk gehoor, op frequentiesverschillen die wij nog kunnen waarnemen en op het terug een analoog signaal (sinusoïdes) vormen na digitalisaties. Het immense analoge bereik van de frequenties wordt verdeeld over een beperkt aantal stappen. Op basis hiervan wordt bepaald hoeveel bits er nodig zijn om alle frequenties weer te kunnen geven.
Het feit dat er verschillende (analoge) televisiesystemen bestonden dicteerde toen min of meer de keuze voor de samplefrequentie, want het moest ook nog eens zo zijn dat je per analoge beeldlijn een geheel aantal samples moest kunnen opslaan. Welnu, de dominante analoge televisiesystemen eind jaren '70 werkten met 30 Hz frame rate (60 Hz field rate interlaced) en nominaal 525 lijnen (lijnfrequentie 30*525 Hz = 15750 Hz, VS en Japan) of met 25 Hz frame rate (50 Hz field rate interlaced) en nominaal 625 lijnen (lijnfrequentie 25*625 Hz = 15625 Hz, Europa), waarbij je moet bedenken dat daarvan effectief ca. 490 resp. ca. 590 lijnen overbleven omdat er tijd nodig is voor de verticale retrace van een elektronenstraal in een kathodestraalbuis. Als je nu uitgaat van 3 samples per beeldlijn per audiokanaal, dan levert een eenvoudig rekensommetje op dat je hebt:
Voor NTSC:
490 * 30 * 3 = 44100 Hz
Voor PAL:
588 * 25 * 3 = 44100 Hz
En daarmee was de zaak beklonken, het moest dus wel 44,1 kHz zijn gezien de technische beperkingen van destijds en de eis om zowel PAL als NTSC videoapparatuur voor mastering te kunnen gebruiken. Achteraf (en trouwens ook toen al) is dat sterk te betreuren, want er bestond ook vóór de komst van de CD al wel digitale opname-apparatuur die in bijvoorbeeld platenstudio's werd ingezet en die met 48 kHz werkte. Het album The Visitors van Abba bijvoorbeeld (uit 1981) is digitaal opgenomen met 48 kHz, hoewel er toen nog geen CD bestond. Later, met de komst van de DVD Video (en DVD Audio), is men zo verstandig geweest om te kiezen voor 48 kHz (en, optioneel, 96 kHz en 192 kHz), maar voor de CD was het te laat om er nog iets aan te veranderen. Een consequentie daarvan is bijvoorbeeld dat geluidskaarten in computers tot op de dag van vandaag zowel 48 als 44,1 kHz samplefrequentie moeten ondersteunen, wat de kaarten complexer en duurder maakt dan nodig en kwalitatief niet optimaal is omdat een verliesvrije conversie van 48 naar 44,1 kHz samplefrequentie of omgekeerd onmogelijk is.
Sony wilde het destijds trouwens nog bonter maken qua samplefrequentie. Omdat al in de jaren '50 de field rate voor NTSC iets omlaag was gebracht van 60 Hz naar 59,94 Hz (een noodzakelijke aanpassing bij NTSC om daar met kleur te kunnen werken) wilde Sony eigenlijk een sample frequentie van 44,056 kHz voor de CD, maar dat zagen ze bij Philips niet zitten omdat het niet helemaal compatibel was met PAL videoapparatuur. Na wat getouwtrek kreeg Philips zijn zin met 44,1 kHz in ruil voor het toegeven aan de 16 bits eis van Sony. Gevolg was wel dat je bij NTSC eigenlijk van zwart-wit video apparatuur gebruik moest maken voor een correcte mastering met 44,1 kHz, maar daar werd ook wel eens tegen gezondigd zodat sommige opnamen of analoge transfers uit die beginperiode ietsje te snel lopen ...
Sommige bronnen beweren dat Sony Philips mogelijk een commerciële hak heeft willen zetten bij de onderhandelingen over de standaards omdat ze wisten dat Philips al heel veel geld had geïnvesteerd in een 14 bits DAC (de TDA1540 om precies te zijn), die werd ontwikkeld en geproduceerd in de toenmalige chipsfabriek in Nijmegen. Philips kon onmogelijk nog op tijd voor de introductie van de CD een 16 bits D/A converter ontwikkelen, en dus was de gedachte dat de eerste Philips modellen bij introductie meteen al een achterstand zouden hebben op de spelers van Sony, die immers wel met 16 bits converters werkten (overigens ingekocht bij Burr-Brown, dus niet door Sony zelf ontwikkeld).
Maar dit pakte toch even anders uit. De Japanners hadden buiten de creativiteit van de Philips technici gerekend, die een bijzondere truc bedachten: oversampling. Door de 14 bits converter niet met 44,1 kHz te laten werken, maar met het viervoudige hiervan, dus 176,4 kHz, kon men de twee minst significante databits (bit 15 en bit 16) gebruiken om vier 14 bits samples gemaakt van één oorspronkelijk 16 bits sample ieder apart in de laatste (14de) bit aan te passen, zodat je na conversie naar analoog en middeling (i.e. filtering) daadwerkelijk een echte 16 bits resolutie hebt. En dat niet alleen, de low level lineariteit was ook nog eens stukken beter dan bij de toenmalige 16 bits converters van Burr-Brown. En zo klonken de eerste Philips spelers duidelijk beter dan de eerste Japanse producten. Dat had overigens ook te maken met de filtering: door de viervoudige samplefrequentie in de speler waren veel minder steile filters nodig die o.a. minder fasevervorming en ringing opleverden bij frequenties tot 20 kHz.
Jaja, na lezing van het bovenstaande zul je daar wel iets genuanceerder over denken. Trouwens, over het theorema van Shannon gesproken (want daar doel je op): dat is eigenlijk niet van toepassing bij digitale audio. Shannon gaat er namelijk van uit dat je de waarden van al je samples exact kent, maar dit is niet zo: door de kwantisatie krijg je afrondingsfouten, en dan heb ik het nog even niet gehad over zaken als thermische drift en niet-lineariteiten in PCM converters. Door de digitalisering krijg je zo kwantisatieruis. In het begin werden de gevolgen daarvan niet goed begrepen, maar na enige tijd leerde men dat je de nadelige effecten hiervan kunt verminderen door het toevoegen van wat ruis, de zogeheten dither.quote:De frequentie is gekozen omdat het bekend is dat wanneer je een analoog signaal digitaliseert dat je dan minstens 2 keer de maximale frequenties (20 kHz) nodig hebt om van dat digitale signaal terug hetzelfde analoge signaal te maken. Als je wat informatie opzoekt op de Engelstalige Wikipedia dan zal je de naam van die theorie wel tegenkomen.
Eigenlijk zijn 16 bits niet voldoende voor hoogwaardige audio met lineaire pulscodemodulatie. Het gangbare argument (ook in reclame-uitingen) was destijds dat elke bit ca. 6 dB aan signaal-ruis verhouding opleverde, en dat je dus met een 16 bits systeem een signaal-ruis verhouding van zo'n 96 dB zou kunnen krijgen, en dat zou veruit superieur zijn aan wat er met analoge systemen mogelijk was en meer dan voldoende. Dat is ook wel zo, maar het gaat niet alleen om die signaal-ruis verhouding. Bij een lineaire kwantisatie wordt de resolutie effectief slechter naarmate het signaalniveau lager wordt, omdat de stapgrootte in dB uitgedrukt bij lagere signaalniveaux steeds groter wordt. En dat is niet in overeenstemming met de manier waarop ons gehoor werkt. Bij hoge signaalniveaux is er een grote overkill aan resolutie die we niet waar kunnen nemen, en bij lage signaalniveaux komt het systeem resolutie tekort. En dat gaat ten koste van de subtiliteit van de weergave en van de ruimtelijke informatie.
Eigenlijk zou je geen lineaire maar een logaritmische kwantisatie moeten hebben, maar dat was - en is - technisch niet goed te realiseren, en zeker niet in een consumentenproduct. Blijft dus over om te gaan werken met meer dan 16 bits als je tenminste bij lineaire pulscodemodulatie wil blijven (maar: SACD gebruikt een vorm van deltamodulatie). Ik heb er destijds bij de introductie van de audio CD al op gewezen dat 16 bits niet voldoende zijn en dat je minimaal 24 bits zou moeten hebben voor een niet te bekritiseren audiosysteem maar dat was toen een volstrekt onhaalbare kaart en werd geloof ik ook niet serieus genomen. Maar inmiddels zijn we 30 jaar verder, en is het volkomen geaccepteerd dat 24 bits wenselijk zijn. Het medium DVD Video kan bijvoorbeeld gebruik maken van LPCM audio met 16 óf 24 bits resolutie en met een samplefrequentie van 48 of 96 kHz. Jammer genoeg wordt daar weinig gebruik van gemaakt uitgezonderd op sommige muziek DVD's. Bij DVD Audio (nooit echt doorgebroken mede door de format war met SACD) zijn (alleen voor stereo) zelfs 176,4 kHz en 192 kHz samplefrequentie mogelijk, ook met 24 bits resolutie.
Over het nut van hogere samplefrequenties is ook een hoop te zeggen, maar ik moet het kort houden omdat ik merk dat deze post al weer veel langer is geworden dan eigenlijk de bedoeling was. Er is uiteraard niets mis met het theorema van Shannon, maar net zo min als een exacte signaalreconstructie mogelijk is door de kwantisatie is een oneindig steil filter met een perfecte doorlaatkarakteristiek te realiseren, en dat betekent dat de praktijk toch stukken weerbarstiger is dan de theorie. Je zult om te beginnen een flinke marge moeten nemen met de samplefrequentie om de nadelige effecten van de (analoge dan wel digitale) filtering in de doorlaatband binnen de perken te houden, en verder is het twijfelachtig of een beperking van de doorlaatband tot 20 kHz überhaupt wel verstandig is. Het is inderdaad zo dat mensen (uitgezonderd wellicht heel jonge kinderen) geen sinustonen boven 20 kHz kunnen waarnemen, maar het is een denkfout om daaraan de conclusie te verbinden dat een doorlaatband tot 20 kHz dan ook voldoende is. Er zijn namelijk aanwijzingen dat het menselijk gehoor snellere stijgtijden kan waarnemen dan je op grond van die 20 kHz zou verwachten, en ook is het zo dat het niet-lineaire gedrag van ons gehoor maakt dat boventonen met een frequentie boven 20 kHz in combinatie met grondtonen met een (veel) lagere frequentie aanleiding geven tot intermodulatieproducten die erin resulteren dat die an sich onhoorbare boventonen wel degelijk een bijdrage leveren aan onze geluidsperceptie, en dus feitelijk onmisbaar zijn in een high-end audiosysteem. En inderdaad hadden goede analoge audiosystemen vroeger een doorlaatband die verder doorliep dan die 20 kHz. Voor studiorecorders, snijtafels, high-end elementen en versterkers en sommige speakersystemen (elektrostaten) was een min of meer vlakke karakteristiek tot 30 of 40 kHz helemaal niet ongewoon.
Van de - naïeve - veronderstellingen die destijds (naast hetgeen commercieel en technisch haalbaar was) hebben geleid tot de CD audio standaard met een 16 bits lineaire kwantisatie en een samplefrequentie van 44,1 kHz is dus inmiddels weinig meer over, maar intussen zitten we wel nog steeds met die standaard opgescheept voor diverse vormen van digitale audio, en dus niet alleen bij weergave van een audio CD. En hoewel er al lang superieure standaards zijn is helaas te verwachten dat die niet meer echt door zullen breken. Er is inmiddels door allerlei oorzaken (loudness wars, dynamiekcompressie, personal audio, lossy codecs), een hele generatie op aan het groeien die nog nooit echt goede audioweergave heeft gehoord en daar deels waarschijnlijk ook niet eens meer toe in staat is omdat gehoorschade onder jongeren de laatste jaren dramatische vormen heeft aangenomen. Sic transit gloria sonitus.


Voor mij zeker niet te lang, ik heb het met veel interesse gelezen.quote:Over het nut van hogere samplefrequenties is ook een hoop te zeggen, maar ik moet het kort houden omdat ik merk dat deze post al weer veel langer is geworden dan eigenlijk de bedoeling was.
Ik wist natuurlijk wel dat de exacte frequentie op de een of andere manier afhing van de aanwezige apparatuur en dat de samplefrequentie die het dichtst boven de 40 kHz lag daarom werd gekozen maar het precieze hoe en wat wist ik niet.quote:Jaja, na lezing van het bovenstaande zul je daar wel iets genuanceerder over denken.
Er zit een adder onder het gras. Waarom vier 14-bits samples als enkel de 14de bit werd aangepast?quote:Door de 14 bits converter niet met 44,1 kHz te laten werken, maar met het viervoudige hiervan, dus 176,4 kHz, kon men de twee minst significante databits (bit 15 en bit 16) gebruiken om vier 14 bits samples gemaakt van één oorspronkelijk 16 bits sample ieder apart in de laatste (14de) bit aan te passen, zodat je na conversie naar analoog en middeling (i.e. filtering) daadwerkelijk een echte 16 bits resolutie hebt.
Sample 1: de eerste 14 bits
Sample 2: bits 1 t/m13 + bit 15
Sample 3: bits 1 t/m 14 + bit 16
Ik weet niet wat overheerst: de teleurstelling dat Philips genoegen nam met 14 bits of de vreugde dat Philips met zo'n creatieve oplossing kwam die ook nog eens superieur was t.o.v. de toen der tijd gebruikte 16-bits DAC.
Ik erger mij er ook al jarenlang aan:quote:Er is inmiddels door allerlei oorzaken (loudness wars, dynamiekcompressie, personal audio, lossy codecs), een hele generatie op aan het groeien die nog nooit echt goede audioweergave heeft gehoord en daar deels waarschijnlijk ook niet eens meer toe in staat is omdat gehoorschade onder jongeren de laatste jaren dramatische vormen heeft aangenomen. Sic transit gloria sonitus.
- de vicieuze spiraal (vind ik een betere uitdrukking dan een vicieuze cirkel) die leidt tot gehoorbeschadiging: steeds maar het gehoor beschadigen van mensen door het geluid harder te zetten zodat de mensen het slechter horen, het geluid weer harder moet worden gezet, ... Het schijnt dat er een effect is wat ze geluidsdoping noemen wat stimuleert om deze zinloze vicieuze spiraal voort te zetten
- de MP3-gekte. Leuke uitvinding hoor maar met een eenvoudige hoofdtelefoon of eenvoudige speakers hoor je al dat het geluid slechter klinkt (minder helder/doffer). Het is te begrijpen dat Apple toen der tijd voor dit formaat koos maar tegenwoordig zijn er MP3-spelers die ook FLAC-formaat en niet-gecomprimeerde formaten kunnen afspelen. Dat mensen het op hun computer nog steeds afspelen begrijp ik helemaal niet met een prijs van 5 cent per gigabyte, dus 5 cent per pak hem beet 20-25 ongecomprimeerde liedjes.
Over de smaak van veel leeftijdsgenoten zal ik me maar niet uitlaten, dat is te subjectief.
Ik heb goede hoop dat het standaard audioformaat in de toekomst gaat verbeteren dankzij de grotere opslagcapaciteit van de opslagmedia en de lagere prijs van deze opslagmedia per gigabyte. Ja, veel mensen interesseert het niet meer wat de geluidskwaliteit is zolang het maar luid is en veel mensen hebben een te beschadigd gehoor voor hun leeftijd maar ook in deze tijd zijn er muzikale mensen die wel zuinig zijn op hun gehoor en die voor highendapparatuur kiezen voor zo ver ze dat kunnen betalen. Ik had al diverse keren gelezen dat veel muzikanten klagen dat 16 bits te weinig zouden zijn na deze audio te hebben vergeleken met 24 bits, na jouw verhaal gelezen te hebben begrijp ik beter waarom 16 bits inderdaad niet genoeg zijn (zelf had ik trouwens als amateurmuzikant al het vermoeden dat die boventonen mogelijk lagere frequenties zouden kleuren maar dat was nog louter speculatie). Er zijn mensen die geld teveel hebben en denken dat ze een audiofiel zijn maar wanneer professionele muzikanten, soundengineers enz. stellen een kwaliteitsverschil waar te nemen dan neem ik dat serieus. Deze mensen zullen om een format vragen wat wel in optimale kwaliteit het geluid aanbiedt. Helaas worden ze, in dit geval letterlijk, overschreeuwd door de niet-fijnproevers en besteden deze niet-fijnproevers samen veel meer geld dan de roependen in de woestijn. Gelukkig blijkt het in de audiowereld zo te zijn dat er altijd wel bedrijven en zelfs individuen (http://nwavguy.blogspot.nl/2011/07/o2-design-process.html) te zijn die alles uit de kast halen om hierin te voorzien.
Voor de korte termijn zou de overheid eens wat moeten doen aan die gehoorbeschadiging. Begin eens met als overheid een maximum geluidsintensiteit (zowel gemiddeld als piek met duur van piek gespecificeerd) op te leggen aan bioscopen, cafés, festivals, studieverenigingen, sportverenigingen enz.
Ik herinner me dat begin 2000 een politieke partij (SGP of CU als ik me niet vergis) dit voorstelde, deze partij werd zeer ten onrechte hierom belachelijk gemaakt. Jammer. Tot die tijd zouden ouders zich hiervan bewust moeten worden en hun jongeren moeten stimuleren om in zulke omstandigheden gehoorbescherming te gebruiken die alle frequenties even sterk tegenhouden. Triest dat het nodig is maar ik zou het zeker doen als ik een vader zou zijn. Toch gek, zo lang geleden waarschuwden politici hier al voor en in de media zijn er al jarenlang verhalen van KNO-artsen die waarschuwen voor het feit dat steeds meer jongeren op steeds jongere leeftijd steeds meer doof worden. Deze jongeren komen zelf aan het woord en leggen uit hoe die doofheid hun hindert in hun dagelijkse leven (pieptoon, concentratieproblemen) en nog doen de politici er niets aan. Als mensen om te beginnen eens beschermd zouden worden tegen onvrijwillige gehoorbeschadiging dan zou er een flinke stap zijn gezet. De technische bedrijven die geluidsapparatuur maken zouden ook meer hun verantwoordelijkheid kunnen nemen. Waarom niet een begrenzer die omzeild kan worden? Je ontneemt mensen niet hun vrijheid maar je zorgt er wel voor dat ze niet tegen hun intentie worden blootgesteld aan te luid geluid.
[ Bericht 2% gewijzigd door Bram_van_Loon op 14-02-2013 08:09:53 ]
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Nee, zo werkt het niet. Ik kan geen goede beschrijving vinden, maar heel kort kun je het je als volgt voorstellen. Staan bit 15 en bit 16 in je oorspronkelijke sample beiden op 0, dan kap je deze af en gebruik je het resterende 14 bit sample voor alle vier je samples die als input dienen voor je 14 bits converter die werkt met 176,4 kHz. Staan bits 15 en 16 in je oorspronkelijke 16 bits sample daarentegen niet beiden op 0, dan heb je voor bit 15 en 16 drie mogelijkheden, namelijk 01, 10 en 11. In dit geval tel je bij resp. 1, 2 of 3 van je vier 14 bits samples (opgevat als binair getal) één op en de resterende resp. 3, 2 of 1 van je vier 14 bits samples laat je onveranderd. Het effect na D/A conversie en filtering (en daarmee middeling) met je 14 bits DAC is dan dat je tussen de niveaux die corresponderen met twee opeenvolgende 14 bits waarden nog drie tussenliggende niveaux hebt gecreëerd, die corresponderen met resp. 1/4, 2/4 en 3/4 van het niveauverschil tussen die opeenvolgende 14 bits waarden. En omdat die tussenliggende niveaux weer corresponderen met de status van je oorspronkelijke bits 15 en 16 is er dus geen resolutie verloren gegaan en heb je de echte 16 bits resolutie van de bron met je 14 bits DAC. Geniaal toch?quote:Op donderdag 14 februari 2013 07:50 schreef Bram_van_Loon het volgende:
Er zit een adder onder het gras. Waarom vier 14-bits samples als enkel de 14de bit werd aangepast?
Sample 1: de eerste 14 bits
Sample 2: bits 1 t/m13 + bit 15
Sample 3: bits 1 t/m 14 + bit 16
Later is men overigens op dit principe gaan voortborduren, want je hoeft natuurlijk niet op te houden bij viervoudige oversampling. Uiteindelijk heeft dit geleid tot de ontwikkeling van 1-bits converters die een heel goede lineariteit hebben en tegenwoordig in vrijwel alle CD spelers worden gebruikt. En dit leidde weer tot het idee om in de gehele keten direct met 1-bits codering te gaan werken voor de SACD. Prachtig stukje fundamenteel onderzoek dat hier in Nederland is gedaan. Kees Schouhamer Immink, de unsung hero achter de ontwikkeling van de CD bij Philips schijft het idee voor de oversampling toe aan ene Karel Dijkmans.
Philips heeft er nogal eens een handje van gehad voor consumentenproducten uit te gaan van minimalistische standaarden. En dat heeft ze in het verleden geen windeieren gelegd, denk alleen maar aan de audiocassette. Daartegenover staat dat enkele consumentenproducten waarbij ze het qua techniek ambitieuzer aanpakten dan weer gigantisch zijn geflopt en hebben geresulteerd in miljoenenverliezen (denk aan het Video 2000 systeem en de DCC).quote:Ik weet niet wat overheerst: de teleurstelling dat Philips genoegen nam met 14 bits of de vreugde dat Philips met zo'n creatieve oplossing kwam die ook nog eens superieur was t.o.v. de toen der tijd gebruikte 16-bits DAC.
De audio CD is (overigens mede door de inbreng van Sony) wel een doorslaand succes geworden, zodat je daar gezien het bovenstaande met tevredenheid op terug kunt kijken. Helaas blijft het bij terugkijken, want dit soort werk wordt in Nederland al lang niet meer gedaan bij Philips, en voor zover mij bekend evenmin bij andere bedrijven. Immink is dan ook lang geleden opgestapt bij Philips omdat hij niet meer in de gelegenheid werd gesteld verder te gaan met zijn baanbrekende en fundamentele werk op het gebied van optische gegevensdragers, digitale signaalverwerking en foutcorrectie, en digitale audio en video, en dat nadat hij substantiële en onmisbare bijdragen had geleverd aan het meest succesvolle consumentenproduct dat Philips ooit heeft gekend.
[ Bericht 3% gewijzigd door Riparius op 15-02-2013 14:26:05 ]


Die Karel Dijkmans heb ik in mijn tijd bij Philips nog wel eens gezien. Die man had vaak een hoed op. Kees Schouhamer Immink zou ik ook moeten hebben gezien, maar die had waarschijnlijk nooit een hoed op, want zijn gezicht komt me niet bekend voor. Zat die club in WY?
Hier in Japan wordt nog steeds aan optische recording gewerkt. Zowel in de VS als in Europa zit die techniek zo ver ik weet op een dood spoor.
Hier in Japan wordt nog steeds aan optische recording gewerkt. Zowel in de VS als in Europa zit die techniek zo ver ik weet op een dood spoor.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Ik moet dit blok voor het vak Statistische methodes en technieken een case maken. We zijn op het punt dat we een aantal variabelen moeten benoemen. De variabele waar we er niet uitkomen is de variabele profit. Dit is een afhankelijke variabele. We twijfelen of het een interval variabele is of een ratio variabele. Is er iemand die me hiermee kan helpen?
Elke zweetneus van je sokken krijg iedereen. En zo is het.


Hallo hier  Ik kreeg in het Beta wiskundetopic de tip dat hier misschien iemand is die bekend is met QM en me wat verder kan helpen. Ik ben bezig met een cursus Quantum mechanics and quantum computation en ik loop tegen de volgende opdracht aan:
Ik kreeg in het Beta wiskundetopic de tip dat hier misschien iemand is die bekend is met QM en me wat verder kan helpen. Ik ben bezig met een cursus Quantum mechanics and quantum computation en ik loop tegen de volgende opdracht aan:
A qubit is either in the state |u>=cos((π/4)−(x/2))|0> +sin((π/4)−(x/2))|1> or |v>=cos((π/4)+(x/2))|0>+sin((π/4)+(x/2))|1> and we want to determine which is the case by measuring it. One of the following two measurements is optimal in terms of the probability of success.
Measurement I: Measure in the |u>=cos((π/4)−(x/2))|0>+sin((π/4)−(x/2))|1>, |u⊥>=−sin((π/4)−(x/2))|0>+cos((π/4)−(x/2))|1> basis and interpret the outcome u as |u> and u⊥ as |v>.
Measurement II: Measure in the standard basis and interpret 0 as |u> and 1 as |v>.
The probability of success is defined as (1/2)pu+(1/2)pv, where pu=Pr[we output |u>∣the qubit was in the state |u>] and pv=Pr[we output |v>∣the qubit was in the state |v>].
The probability of success of Measurement I as a function of x is
(1+sin2x ) / 2. Why?
The probability of success of Measurement II as a function of x is
cos2 ((π/2) - (x/2)). Why? Opgelost, zie edit 2
En dan om vrolijk verder te gaan:
Now note that the following becomes good approximations as θ→0:
sinθ≈θ
sin2((π/4)−θ)≈12−c⋅θ
(where c is some constant.) Use these approximations to estimate the probability of success of the two measurements as x→0 (as a function of x and c).
Is er iemand die me hier verder kan helpen?
Edit: Misschien een goede aanvullende opmerking die misschien duidelijk maakt waar ik verkeerd ga (?)
En weer een edit: Er gaat een lampje branden. De kans dat |u> nul is is natuurlijk gelijk aan de kans dat |v> 1 is. Dus dat klopt inderdaad omdat ze allebei x/2 afwijken van π/2. Goed, dat is één
[ Bericht 4% gewijzigd door KapiteinGasthof op 18-02-2013 02:38:53 ]
A qubit is either in the state |u>=cos((π/4)−(x/2))|0> +sin((π/4)−(x/2))|1> or |v>=cos((π/4)+(x/2))|0>+sin((π/4)+(x/2))|1> and we want to determine which is the case by measuring it. One of the following two measurements is optimal in terms of the probability of success.
Measurement I: Measure in the |u>=cos((π/4)−(x/2))|0>+sin((π/4)−(x/2))|1>, |u⊥>=−sin((π/4)−(x/2))|0>+cos((π/4)−(x/2))|1> basis and interpret the outcome u as |u> and u⊥ as |v>.
Measurement II: Measure in the standard basis and interpret 0 as |u> and 1 as |v>.
The probability of success is defined as (1/2)pu+(1/2)pv, where pu=Pr[we output |u>∣the qubit was in the state |u>] and pv=Pr[we output |v>∣the qubit was in the state |v>].
The probability of success of Measurement I as a function of x is
(1+sin2x ) / 2. Why?
The probability of success of Measurement II as a function of x is
cos2 ((π/2) - (x/2)). Why? Opgelost, zie edit 2
En dan om vrolijk verder te gaan:
Now note that the following becomes good approximations as θ→0:
sinθ≈θ
sin2((π/4)−θ)≈12−c⋅θ
(where c is some constant.) Use these approximations to estimate the probability of success of the two measurements as x→0 (as a function of x and c).
Is er iemand die me hier verder kan helpen?
Edit: Misschien een goede aanvullende opmerking die misschien duidelijk maakt waar ik verkeerd ga (?)
Hier zou ik zeggen dat de kans op succes cos2 (π/2) is.quote:The probability of success of Measurement II as a function of x is
cos2 ((π/2) - (x/2)). Why?
En weer een edit: Er gaat een lampje branden. De kans dat |u> nul is is natuurlijk gelijk aan de kans dat |v> 1 is. Dus dat klopt inderdaad omdat ze allebei x/2 afwijken van π/2. Goed, dat is één
[ Bericht 4% gewijzigd door KapiteinGasthof op 18-02-2013 02:38:53 ]
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Je zou even een PM naar Netflanders kunnen sturen (om haar te attenderen op deze vraag), zij is een afgestudeerd natuurkundige. Er zijn nog een paar mensen die natuurkunde studeren of die afgestudeerd zijn in natuurkunde maar die lezen niet dagelijks wat er hier wordt gevraagd, meestal ontstijgen de vragen hier (bij wiskunde anders!) niet het HAVO/VWO-niveau.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Tnx, zal het eens proberen!quote:Op zondag 17 februari 2013 21:14 schreef Bram_van_Loon het volgende:
Je zou even een PM naar Netflanders kunnen sturen (om haar te attenderen op deze vraag), zij is een afgestudeerd natuurkundige.
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Hoe kan ik hem vergeten? Haushofer wil jou vast wel helpen als jij hem even attendeert op deze vraag en hij is hier nog 'dagelijks' actief.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Ah ga het gelijk proberen, nogmaals tnxquote:Op zondag 17 februari 2013 21:35 schreef Bram_van_Loon het volgende:
Hoe kan ik hem vergeten? Haushofer wil jou vast wel helpen als jij hem even attendeert op deze vraag en hij is hier nog 'dagelijks' actief.
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Hij is een aardige jongen op dit forum, zolang jij laat zien dat jij je best doet twijfel ik er niet aan dat hij je wel even een handje helpt. Het kan natuurlijk wel een paar dagen duren voordat hij toevallig actief is op dit forum.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Ik verwacht niet dat ik het allemaal voorgekauwd krijg hoorquote:Op zondag 17 februari 2013 21:42 schreef Bram_van_Loon het volgende:
Hij is een aardige jongen op dit forum, zolang jij laat zien dat jij je best doet twijfel ik er niet aan dat hij je wel even een handje helpt.
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Bij dit niveau verwacht ik niet anders maar op een lager niveau (die stellen ook regelmatig vragen)zijn er nogal wat mensen die de verkeerde attitude hebben.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Van geef mij het antwoord en het waarom hoef ik niet te weten?quote:Op zondag 17 februari 2013 21:46 schreef Bram_van_Loon het volgende:
Bij dit niveau verwacht ik niet anders maar op een lager niveau (die stellen ook regelmatig vragen)zijn er nogal wat mensen die de verkeerde attitude hebben.
Ik moet mijn opdrachten morgen insturen maar dat kan ook zonder deze, dan maar wat minder punten. Maar ik heb er denk ik wel veel aan als ik het goed snap in de volgende weken
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


En vandaag nog want morgen moet ik het inleveren!quote:Op zondag 17 februari 2013 21:49 schreef KapiteinGasthof het volgende:
[..]
Van geef mij het antwoord en het waarom hoef ik niet te weten?
Ja.
Jammer van die punten (ik weet hoe het voelt, je krijgt in Nederland niet altijd de tijd om het rustig voor te bereiden en op te zoeken en dan spelen velen ook nog eens vals), houd het forum vanavond wat in de gaten maar reken er niet op dat je vanavond nog antwoord krijgt. Ik heb vooralsnog slechts een oppervlakkige inleiding gehad tot de quantummechanica (alweer weggezakt doordat het te oppervlakkig was) dus ik kan je er niet mee helpen.quote:Ik moet mijn opdrachten morgen insturen maar dat kan ook zonder deze, dan maar wat minder punten. Maar ik heb er denk ik wel veel aan als ik het goed snap in de volgende weken
Wat studeer je en waar?
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Die kom ik al genoeg tegen op mijn werkquote:Op zondag 17 februari 2013 21:52 schreef Bram_van_Loon het volgende:
[..]
En vandaag nog want morgen moet ik het inleveren!
Ja.
Ik studeer niet, heb gewoon een brede interessequote:[..]
Jammer van die punten (ik weet hoe het voelt, je krijgt in Nederland niet altijd de tijd om het rustig voor te bereiden en op te zoeken en dan spelen velen ook nog eens vals), houd het forum vanavond wat in de gaten maar reken er niet op dat je vanavond nog antwoord krijgt.
Wat studeer je en waar?
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Ah voor de duidelijkheid, het is een MOOC cursus. Dus alles via filmpjes e.d. op het blackboard van Edx. Dit is een cursus van zeven weken.
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Nu niet, ik wil wel alle zeven weken en de midterm en final genoeg punten halen natuurlijkquote:
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Prima dat jij uit interesse je hierin verdiept. Waarom niet? Jammer dat je met school hebt moeten afhaken, misschien toch eens OU (rechten bijv.) overwegen? Je kan dat lekker individueel doen en je krijgt een papiertje waar je net wat meer mee kan en wat toegang geeft tot masteropleidingen. Je zou de eerste niet zijn die op die manier bijv. rechter wordt. Sommigen begonnen er zelfs pas mee op latere leeftijd. Het nadeel is de kostprijs.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


De praktijk was voor mij ook wel een goede leerschoolquote:Op zondag 17 februari 2013 22:06 schreef Bram_van_Loon het volgende:
Prima dat jij uit interesse je hierin verdiept. Waarom niet? Jammer dat je met school hebt moeten afhaken, misschien toch eens OU (rechten bijv.) overwegen? Je kan dat lekker individueel doen en je krijgt een papiertje waar je net wat meer mee kan en wat toegang geeft tot masteropleidingen. Je zou de eerste niet zijn die op die manier bijv. rechter wordt. Sommigen begonnen er zelfs pas mee op latere leeftijd. Het nadeel is de kostprijs.
Ik lees graag en veel, onderweg dus een hoop bijgeleerd en als ik weer een nieuwe uitdaging vind qua werk dan doe ik net zoals nu uit interesse zelfstudie of als dat beschikbaar is een MOOC cursus. Vooral de docenten van Berkeley zijn erg prettig en leggen goed uit. De onderwijskundige dingen heb ik bij Open Universiteit NL weggehaald. Er is best veel kennis beschikbaar, het is alleen telkens even zoeken waar je het beste terecht kan. En het mooie is dat alles meestal gratis kan ook.
Ik heb wel vaker nagedacht over een "echte" studie naast werk maar het zijn inderdaad meestal de kosten die me tegenhouden. En daarnaast weet ik niet of het me lukt om vier jaar lang maar op één vakgebied bezig te zijn.
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Wel, het lijkt er op dat jij je op deze manier ook prima redt. Mooi zo. Daar heb ik als TU-student veel respect voor. 
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


Tnxquote:Op zondag 17 februari 2013 22:15 schreef Bram_van_Loon het volgende:
Wel, het lijkt er op dat jij je op deze manier ook prima redt. Mooi zo. Daar heb ik als TU-student veel respect voor.
Ik ga morgen weer op die opgave kauwen, ik zie in ieder geval op het blackboard dat er meer mensen moeite hebben met dit deel dus ik ben in ieder geval niet alleen
Zoon van goldfinger1963 O+
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742
Tegen vaccinaties en inentingen? http://www.flabber.nl/art(...)-gelijk-hebben-49742


Hallo,
ik heb een vraag over spiegelbeeldisomeren. Volgens de site waar ik dit plaatje vandaan heb, heeft dit molecuul 3 isomeren (2^2-1)
Waarom dan? Er is een inwendig spiegelvlak en je kan dit molecuul 180 graden draaien, linksom of rechtsom en je hebt volgens mij nog hetzelfde molecuul. Dan tel ik er maar twee en geen drie.
Oftewel ik snap de formule 2^n wel (geen symmetrie) maar de formule 2^n-1 niet (wel symmetrie)
ik heb een vraag over spiegelbeeldisomeren. Volgens de site waar ik dit plaatje vandaan heb, heeft dit molecuul 3 isomeren (2^2-1)
Waarom dan? Er is een inwendig spiegelvlak en je kan dit molecuul 180 graden draaien, linksom of rechtsom en je hebt volgens mij nog hetzelfde molecuul. Dan tel ik er maar twee en geen drie.
Oftewel ik snap de formule 2^n wel (geen symmetrie) maar de formule 2^n-1 niet (wel symmetrie)
Unbowed, Unbent, Unbroken.


Rondom C1 en C3 heb je vier verschillende atomen. Die maken allemaal een hoek van 102 graden (zoiets) onderling. Als je oranje en groen van plaats verwisselt kan je hem door te draaien niet hetzelfde krijgen als in jouw plaatje.quote:Op dinsdag 19 februari 2013 17:59 schreef BeyondTheGreen het volgende:
Hallo,
ik heb een vraag over spiegelbeeldisomeren. Volgens de site waar ik dit plaatje vandaan heb, heeft dit molecuul 3 isomeren (2^2-1)
[ afbeelding ]
Waarom dan? Er is een inwendig spiegelvlak en je kan dit molecuul 180 graden draaien, linksom of rechtsom en je hebt volgens mij nog hetzelfde molecuul. Dan tel ik er maar twee en geen drie.
Oftewel ik snap de formule 2^n wel (geen symmetrie) maar de formule 2^n-1 niet (wel symmetrie)
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Hm, ik vind het nogal lastig om er een beeld van te krijgen. Hoe ik het zie is als twee (verschillende) chirale centrums aan elkaar vastzitten dat je vier combinaties hebt (11, 12, 21, 22) 1 = wel gespiegeld, 2 is niet gespiegeld. Dit kan dus alleen bij twee verschillende chirale centrums.
Wat jij zegt, die groene en oranje omwisselen zie ik dan wel voor me dat je op drie komt ipv twee maar dan begrijp ik het niet meer. Je kunt de witte en groene omwisselen, maar ook de groene en oranje. Heb je dan niet drie mogelijkheden? Nu snap ik het niet meer.

Wat jij zegt, die groene en oranje omwisselen zie ik dan wel voor me dat je op drie komt ipv twee maar dan begrijp ik het niet meer. Je kunt de witte en groene omwisselen, maar ook de groene en oranje. Heb je dan niet drie mogelijkheden? Nu snap ik het niet meer.
Unbowed, Unbent, Unbroken.


Elk chiraal centrum kan of de R- of de S-configuratie hebben. Dat zou 22 = 4 isomeren moeten opleveren. Toch zijn het er maar 22-1 = 3. Met andere woorden 2 van de in theorie mogelijk 4 isomeren zijn hetzelfde. Welke?quote:Op dinsdag 19 februari 2013 18:22 schreef BeyondTheGreen het volgende:
Hm, ik vind het nogal lastig om er een beeld van te krijgen. Hoe ik het zie is als twee (verschillende) chirale centrums aan elkaar vastzitten dat je vier combinaties hebt (11, 12, 21, 22) 1 = wel gespiegeld, 2 is niet gespiegeld. Dit kan dus alleen bij twee verschillende chirale centrums.
Wat jij zegt, die groene en oranje omwisselen zie ik dan wel voor me dat je op drie komt ipv twee maar dan begrijp ik het niet meer. Je kunt de witte en groene omwisselen, maar ook de groene en oranje. Heb je dan niet drie mogelijkheden? Nu snap ik het niet meer.


Oké, eens zien, als ik groen en wit omwissel kom ik dus op twee combinaties (door draaien). Dat is niet goed. Want:quote:Op dinsdag 19 februari 2013 18:23 schreef lyolyrc het volgende:
[..]
Elk chiraal centrum kan of de R- of de S-configuratie hebben. Dat zou 22 = 4 isomeren moeten opleveren. Toch zijn het er maar 22-1 = 3. Met andere woorden 2 van de in theorie mogelijk 4 isomeren zijn hetzelfde. Welke?
Optie 1: het plaatje
Optie 2: groen en wit omwisselen
Bij oranje en groen omwisselen:
-optie 1: het plaatje
-optie 2: oranje en groen aan beide kanten omwisselen
-optie 3: oranje en groen alleen links omwisselen
-optie 4: oranje en groen alleen rechts omwisselen
Voor mij zijn ze alle vier verschillend.
Ofwel ik heb nu opeens zes opties, of ik heb er twee of ik heb er vier.
En ja, ik weet dat er geen jota van mijn verhaal klopt.
Unbowed, Unbent, Unbroken.


Probeer eens in te zien wat er gebeurt als je die moleculen draait. Als je hiermee moeite hebt dan is er een oplossing. Als het goed is dan hebben ze op jouw school (vraag het aan jouw leraar!) bouwsteentjes waar je moleculen mee kan maken (plastic staafjes en plastic balletjes). Ik raad je aan om alle vier de mogelijkheden die jij ziet (waarvan dus twee hetzelfde zijn) te maken en ze dan eens te draaien en zien wat er gebeurt.
Als jij bij voldoende opgaves die bouwsteentjes gebruikt dan ga je, als het goed is, vanzelf patronen zien waardoor je na een tijdje ook zonder die bouwsteentjes die vragen kan beantwoorden.
Als jij bij voldoende opgaves die bouwsteentjes gebruikt dan ga je, als het goed is, vanzelf patronen zien waardoor je na een tijdje ook zonder die bouwsteentjes die vragen kan beantwoorden.
ING en ABN investeerden honderden miljoenen euro in DAPL.
#NoDAPL
#NoDAPL


In dat geval moet ik nu opgeven en wachten tot de voorjaarsvakantie voorbij is. Dat ga ik niet doen.quote:Op dinsdag 19 februari 2013 18:49 schreef Bram_van_Loon het volgende:
Probeer eens in te zien wat er gebeurt als je die moleculen draait. Als je hiermee moeite hebt dan is er een oplossing. Als het goed is dan hebben ze op jouw school (vraag het aan jouw leraar!) bouwsteentjes waar je moleculen mee kan maken (plastic staafjes en plastic balletjes). Ik raad je aan om alle vier de mogelijkheden die jij ziet (waarvan dus twee hetzelfde zijn) te maken en ze dan eens te draaien en zien wat er gebeurt.
Als jij bij voldoende opgaves die bouwsteentjes gebruikt dan ga je, als het goed is, vanzelf patronen zien waardoor je na een tijdje ook zonder die bouwsteentjes die vragen kan beantwoorden.
Ik ben al een stapje verder. Groen en wit omwisselen/groen en oranje omwisselen heeft hetzelfde effect. Als ik groen en wit omwissel en ik draai dat atoom een stukje, dan ziet het er van mijn oogpunt op een gegeven moment hetzelfde uit als dat ik oranje en groen omwissel, elk chiraal centrum heeft één spiegelbeeld.
Unbowed, Unbent, Unbroken.


Het maakt inderdaad niet uit welke twee groepen rond een chiraal centrum je verwisselt, de nieuwe configuratie is altijd dezelfde. Dus of je bij een R-configuratie nou groen en wit of groen en oranje of oranje en wit verwisselt, het levert telkens de S-configuratie op.quote:Op dinsdag 19 februari 2013 19:39 schreef BeyondTheGreen het volgende:
[..]
In dat geval moet ik nu opgeven en wachten tot de voorjaarsvakantie voorbij is. Dat ga ik niet doen.
Ik ben al een stapje verder. Groen en wit omwisselen/groen en oranje omwisselen heeft hetzelfde effect. Als ik groen en wit omwissel en ik draai dat atoom een stukje, dan ziet het er van mijn oogpunt op een gegeven moment hetzelfde uit als dat ik oranje en groen omwissel, elk chiraal centrum heeft één spiegelbeeld.
Dat wil zeggen dat je isomeren met deze combinaties van configuraties kunt krijgen:
R-R
S-S
R-S
S-R
Welk isomeer kun je nou (als geheel) zo draaien dat die overeenkomt met een van de andere drie?


Beide atomen spiegelen komt overeen met geen van de atomen spiegelen.
Bam!
Dat is 'm of niet?
Bam!
Dat is 'm of niet?
Unbowed, Unbent, Unbroken.


Als je het isomeer van het plaatje bedoelt, dan klopt het inderdaad.quote:Op dinsdag 19 februari 2013 19:46 schreef BeyondTheGreen het volgende:
Beide atomen spiegelen komt overeen met geen van de atomen spiegelen.
Bam!
Dat is 'm of niet?
Beide configuraties wisselen bij R-S geeft S-R. Het hele S-R-isomeer kun je wentelen en dan valt het weer precies samen met wat je had, namelijk R-S.
| Forum Opties | |
|---|---|
| Forumhop: | |
| Hop naar: | |