1e tijdvak
dinsdag 29 mei 2012 13:30-16:30
2e tijdvak
woensdag 20 juni 2012 13:30-16:30
Zag nog geen centraal topic dus maar ff een aangemaakt.
Het zal voor velen wel de laatste zijn.
http://www2.cito.nl/vo/ex2012/VW-1028-a-12-1-s.pdf
25 vragen 70 punten
2 x 1 punt
8 x 2 punten
9 x 3 punten
5 x 4 punten
1 x 5 punten
allemaalquote:Op woensdag 23 mei 2012 13:20 schreef Duderd het volgende:
Weet iemand welke examens uit het verleden lastig waren?dan kan ik die nog eens maken
Alles toch?quote:Op vrijdag 25 mei 2012 10:41 schreef TheDutchguy het volgende:
Wat moeten we niet leren voor scheikunde?
Oh, dat is een tegenvallerquote:
Scheikunde heeft van alle vakken de minste examenstof denk ik, dus het valt best wel mee.quote:
http://www.chem.kuleuven.(...)2h3h4h5h6sedesv2.pdf
http://www.schoolsamenvat(...)examen-stof-2011.pdf
DANK U!quote:Op vrijdag 25 mei 2012 17:53 schreef Nutkicker22 het volgende:
Handig:
http://www.chem.kuleuven.(...)2h3h4h5h6sedesv2.pdf
http://www.schoolsamenvat(...)examen-stof-2011.pdf
Dat is het zeker..quote:
Minste?quote:Op vrijdag 25 mei 2012 17:18 schreef meneer_valk het volgende:
[..]
Scheikunde heeft van alle vakken de minste examenstof denk ik, dus het valt best wel mee.
Kunnen nog best wat overslaan dus
Nou niet echt.. alleen die basisdingen.. voor de rest moet je al het moeilijke weten.quote:Op vrijdag 25 mei 2012 23:39 schreef TheDutchguy het volgende:
http://www.examenblad.nl/(...)_vwo_2012_101021.pdf
Kunnen nog best wat overslaan dus
En al het moeilijke is bijna alle stof. ;|;|
Anyway, hoe ga jij het aanpakken? Hoe zorg je ervoor dat je een voldoende gaat halen?quote:Op vrijdag 25 mei 2012 23:39 schreef TheDutchguy het volgende:
http://www.examenblad.nl/(...)_vwo_2012_101021.pdf
Kunnen nog best wat overslaan dus
Als ik scheikunde niet haal, zak ik.. ;|;|
Ik heb vanmiddag de stof nog een keer doorgelezen om al die termen weer even op te halen. Ben van plan dit weekend en maandag examens te maken, dus geen strand of zonnen voor mijquote:Op vrijdag 25 mei 2012 23:42 schreef MissEll het volgende:
[..]
Anyway, hoe ga jij het aanpakken? Hoe zorg je ervoor dat je een voldoende gaat halen?
Als ik scheikunde niet haal, zak ik.. ;|;|
Morgen maak ik examen, kijk wat ik fout doe en ga dan dat nog ff extra oefenen.
Goedzo. Ja idd, voor mij ook niet. Kan je zo'n examen wel maken dan. Ik begrijp de eerste vraag niet eens. Maar da's wat ik ook zal moeten doen..quote:Op vrijdag 25 mei 2012 23:44 schreef TheDutchguy het volgende:
[..]
Ik heb vanmiddag de stof nog een keer doorgelezen om al die termen weer even op te halen. Ben van plan dit weekend en maandag examens te maken, dus geen strand of zonnen voor mijKan ik die 3 maanden daarna nog altijd doen.
Morgen maak ik examen, kijk wat ik fout doe en ga dan dat nog ff extra oefenen.
Ik zal morgen zien of ik het kanquote:Op vrijdag 25 mei 2012 23:47 schreef MissEll het volgende:
[..]
Goedzo. Ja idd, voor mij ook niet. Kan je zo'n examen wel maken dan. Ik begrijp de eerste vraag niet eens. Maar da's wat ik ook zal moeten doen..
Als ik jou was zou ik gewoon eerst de stof doorlezen en alles begrijpen. Als je de stof nog niet begrijpt heeft het weinig nut om proberen een examen te oefenen.
http://wp.digischool.nl/scheikunde/powerpoint/
Ik had per hoofdstuk gewoon ff die powerpoints bekeken.
Ja haha, die heb ik ook. Maar nog niet aan begonnen. En, heeft het geholpen?quote:Op vrijdag 25 mei 2012 23:49 schreef TheDutchguy het volgende:
[..]
Ik zal morgen zien of ik het kan
Als ik jou was zou ik gewoon eerst de stof doorlezen en alles begrijpen. Als je de stof nog niet begrijpt heeft het weinig nut om proberen een examen te oefenen.
http://wp.digischool.nl/scheikunde/powerpoint/
Ik had per hoofdstuk gewoon ff die powerpoints bekeken.
Thanks!quote:Op vrijdag 25 mei 2012 17:53 schreef Nutkicker22 het volgende:
Handig:
http://www.chem.kuleuven.(...)2h3h4h5h6sedesv2.pdf
http://www.schoolsamenvat(...)examen-stof-2011.pdf
Heerlijk zo'n lang weekend met nog maar ��n examen te gaan. Kun je je helemaal daarop richten.
oefenen leer je ook van, dus is wel genoeg denk ik.quote:Op zaterdag 26 mei 2012 16:11 schreef h.lalala het volgende:
Als ik uit examenbundel, deel 1 (oefenen op onderwerp) alles ga maken, en nog een paar hele examens, denken jullie dat dat genoeg is? Tis toch meer oefenen dan leren?
2011-I is idd wel te doen, ik heb er een 6,8 op gehaald. Ik hoop dat het dinsdag ook zo zal gaanquote:Op zaterdag 26 mei 2012 16:47 schreef Lutte het volgende:
Alle stof herhaalt door het jaar heen, en ik ken alle regeltjes maar ik kan het gewoon niet toepassen. Al ben ik nu 2011-1 aan het maken en dat gaat helemaal niet slecht!
Okeequote:Op zaterdag 26 mei 2012 16:16 schreef Zamorak het volgende:
[..]
oefenen leer je ook van, dus is wel genoeg denk ik.
Heb m wel goed, maar dacht dat dat nou juist een ketenpolymeer was?
heeft een netwerk geen bindingen tussen lange slierten?quote:Op zaterdag 26 mei 2012 17:32 schreef Lutte het volgende:
Oh helpWat is het verschil tussen een netwerk- en een ketenpolymeer? 2011-1 vraag 21
Heb m wel goed, maar dacht dat dat nou juist een ketenpolymeer was?
Nee HCl moet je altijd gesplitst schrijven als H3O+quote:Op zaterdag 26 mei 2012 19:08 schreef metanite het volgende:
Dus je kan HCl niet zomaar met een base laten reageren>??
Hier exact het zelfde.. iedere vraag die ik tegenkom denk ik; Que?!?! Dat dacht ik overigens ook bij ieder SE. Het hele jaar 6jes gehaald en 1x een 8... gemiddelde 6.4, laagste punt 5.9 en toch heb ik sterke twijfels of ik mijn benodigde 4,6 wel ga halen :Squote:Op zaterdag 26 mei 2012 19:13 schreef metanite het volgende:
Oki doki loki! ben echt een wandelende ramp in sk (bewonderenswaardig afgerond met een 6,3)
Same here :Squote:Op zondag 27 mei 2012 00:54 schreef Vincent. het volgende:
Ik ben vooral een ramp wat betreft rekenen in de chemie. Als ik de vraag lees zie ik alle dingen die ze geven, maar ik heb geen flauw idee waar ik moet beginnen met rekenen...En als ik kijk naar het antwoord blijkt de berekening meestal vrij simpel, maar zelf was ik er nooit op gekomen. Iemand tips wat betreft het aanpakken van reken-vragen?
Precies, daar moet ik het ook van hebben. Die berekeningen snap ik echt de ballen van.quote:Op zondag 27 mei 2012 14:57 schreef zoodan het volgende:
Haha ik ook echt helemaaal niet, ik hoop dat je met het snappen van hoe je reacties moet opschrijven, zuur base reacties. blokschema's en chometografiedinges een 4 kunt halen
wat sta je nu dan? wij hadden een docent die alleen maar onaangepaste examenopgaves in de toets deed, dus daaraan heb ik mijn 7 te danken..quote:Op zondag 27 mei 2012 15:26 schreef TheDutchguy het volgende:
[..]
Precies, daar moet ik het ook van hebben. Die berekeningen snap ik echt de ballen van.
Een 6,4. Dus grote kans dat ik een onvoldoende sta na de examens.quote:Op zondag 27 mei 2012 15:45 schreef zoodan het volgende:
[..]
wat sta je nu dan? wij hadden een docent die alleen maar onaangepaste examenopgaves in de toets deed, dus daaraan heb ik mijn 7 te danken..
Wat ik altijd doe, Eerst de reactie vergelijking opstellen en dan zoveel mogelijk gegevens omschrijven naar mol. Verder heb ik dit plaatje altijd in m'n hoofd:quote:Op zondag 27 mei 2012 00:54 schreef Vincent. het volgende:
Ik ben vooral een ramp wat betreft rekenen in de chemie. Als ik de vraag lees zie ik alle dingen die ze geven, maar ik heb geen flauw idee waar ik moet beginnen met rekenen...En als ik kijk naar het antwoord blijkt de berekening meestal vrij simpel, maar zelf was ik er nooit op gekomen. Iemand tips wat betreft het aanpakken van reken-vragen?
http://webcc.corlaercollege.nl/scheikunde/mol.png
Vanuit mol reken ik dan altijd verder naar het gevraagde. Let goed wel goed op de verhoudingen van mol in de reactie. Bijv. 1:2
tabel 66Bquote:Op zondag 27 mei 2012 17:02 schreef metanite het volgende:
ehmm de meeste heb ik in een programmatje in mijn gr staan, maar er staan er ook heel wat in binas
@metanite welk programma (A)
Programmatje kan ik het eigenlijk niet noemen het is een noteflio bestandje wat ik zelf heb gemaakt gebaseerd op een stencil van mij sk leraar wat we vroeger uit onze kop moesten leren (nooit gedaan xD)quote:
ah okee, als er de mogelijkheid is het zonder teveel moeite te uploaden, graag!quote:Op zondag 27 mei 2012 17:10 schreef metanite het volgende:
[..]
Programmatje kan ik het eigenlijk niet noemen het is een noteflio bestandje wat ik zelf heb gemaakt gebaseerd op een stencil van mij sk leraar wat we vroeger uit onze kop moesten leren (nooit gedaan xD)
Alvast bedankt.
Oke ik heb nu echt stress want ik snap echt heel weinig van scheikunde en als ik niet hoger dan een 4 heb dan ben ik gezakt...
Ik heb morgen nog de hele dag om te leren, ik hoop echt heeel erg dat dat genoeg tijd is om een 4 te halen. :s
eeeh... nee.quote:Op zondag 27 mei 2012 18:19 schreef .Paul het volgende:
Het betekent dat de zout gekristalliseerd is door het water. Er zitten dus H2O moleculen om de ionen.
Je moet je voorstellen dat je een bak met water hebt, daar gooi je twee stofjes bij die met elkaar een verbinding aangaan in het water. Door de ruimtelijke vorm van die stof (meestal een zout, maar hoeft niet, eiwitjes zouden bijvoorbeeld ook kunnen) ontstaat er een soort rooster, waar gaten in zitten. Tijdens de vorming van de stof gaan er watermoleculen in die gaten zitten, namelijk een x aantal H2O moleculen. Ze zitten dus zeg maar vast in het molecuul, maar zijn er geen gedeelte van, daar staat die punt voor.
Het water wat in het molecuul zit is 'kristalwater', de volledige stof zelf is een hydraat.
Je hydraat verhitten en het water gaat eruit.
Eerst lees en analyseer ik de bronnen/tekst/plaatjes. Daarna lees ik de vraag en bedenk ik wat ik moet bewijzen/berekenen om het vraagstuk op te lossen (in eenheden denken). En dan patsboem is het antwoord er!
Ik hoop dat er zoveel mogelijk rekenvragen in zitten. Die heb ik meestal in mijn zak.
pff maar met titraties rekenen enzo is lastig joh! wat moet je kunnen met buffers..?quote:Op zondag 27 mei 2012 21:30 schreef Intercam het volgende:
Okee dit gaat waarschijnlijk weinig helpen. Maar ik doe het volgende als ik een reken vraag zie:
Eerst lees en analyseer ik de bronnen/tekst/plaatjes. Daarna lees ik de vraag en bedenk ik wat ik moet bewijzen/berekenen om het vraagstuk op te lossen (in eenheden denken). En dan patsboem is het antwoord er!
Ik hoop dat er zoveel mogelijk rekenvragen in zitten. Die heb ik meestal in mijn zak.
Leer als je er moeite mee hebt de standaard berekening van een titratie uit je hoofd.
standaard berekening? ik doe het met een soort van blokschema's maar daar kom ik vaak niet uit, wat is de standaard berekening?quote:Op zondag 27 mei 2012 21:40 schreef Lilliesleaf het volgende:
Titraties is eigenlijk altijd dezelfde vraag, alleen met een ander verhaaltje. Dus zodra je ziet: titratie. Gelijk niet meer nadenken over het verhaaltje maar bewust opzoek gaan naar: wat zit hier in de buret, wat zit er in het bakje, wat is de molariteit, welke onbekende heb ik, wat voor indicator is het? etc en dan pas bekijken waar ze nou precies naartoe willen met de vraag.
Leer als je er moeite mee hebt de standaard berekening van een titratie uit je hoofd.
Ik heb juist een hekel aan de beschrijf-een-proefopstelling-vragen.
residu is niet perse het afval, soms wil je juist filtreren om het residu te gebruiken.quote:Op zondag 27 mei 2012 22:27 schreef dramatic het volgende:
filtraat residu? wat is wat? residu is over als afval?
Titreren komt toch niet op 't examen dit jaar..quote:Op zondag 27 mei 2012 22:20 schreef dramatic het volgende:
titreren vind je of makkelijk of moeilijk.. ik t laatste
Ik heb echt het gevoel dat je daar niets van hoeft te weten.
Maar ja, laat je gevoel het nou mis hebben..
Een cijfer lager dan 5.5 en ik ben gezakt.
Wat nemen jullie nog ff door?
Ja, gelijk heb je. Ben er echt bang voor..quote:Op maandag 28 mei 2012 01:06 schreef Lilliesleaf het volgende:
Geen veel oude examens oefenen. Dan loop je er vanzelf tegen aan wat je nog wel en niet kunt. Scheikunde is typisch zo'n vak waarbij je zo vaak als je wil dingen kunt 'doornemen' maar als je het niet vaak genoeg hebt 'gedaan' lukt het alsnog niet.
Alleen begrijp ik de examens weer niet.
quote:Op maandag 28 mei 2012 07:47 schreef zoodan het volgende:
goedemorgen! hopelijk snap ik vanavond genoeg om een 4 te halen :p
quote:Op maandag 28 mei 2012 07:47 schreef zoodan het volgende:
goedemorgen! hopelijk snap ik vanavond genoeg om een 5.5 te halen :p
Maar veel succ6 iedereen!
Ik heb morgen lekker een tentamen
http://static.examenblad.nl/9336110/d/ex2010/vw-1028-a-10-2-o.pdf (opdrachten)
http://static.examenblad.nl/9336110/d/ex2010/vw-1028-a-10-2-c.pdf (correctievoorschrift)
http://www.youtube.com/user/scheikundelessen?feature=watch
let op: de stof is voor havo, maar werkt wel goed om de basis te begrijpen
Idd. Ik hoop 't echt..quote:Op maandag 28 mei 2012 10:43 schreef dramatic het volgende:
je zou maar een 5.5 moeten halen voor dit examen
Scheikunde is m'n laatste kans!
Invullen in de breuk die je opstelt bij een zuur-base reactie zodat je de onbekende kan uitrekenen (meestal dus H3O+ of OH-) vervolgens kan je met de concentratie die je hebt uitgerekend de pH of de pOH (pH=14-pOH) berekenen.quote:Op maandag 28 mei 2012 13:57 schreef Intercam het volgende:
Okee random Scheikunde vraag: Wat moet je kunnen met de pKz/pKb waarden die in binas tabel 49 staan?
pH=-log[H3O+] of pOH=-log[OH-]
De pKz he niet de Kz. Of kan je de pKz ook ergens invullen?quote:Op maandag 28 mei 2012 13:58 schreef zoodan het volgende:
[..]
Invullen in de breuk die je opstelt bij een zuur-base reactie zodat je de onbekende kan uitrekenen (meestal dus H3O+ of OH-) vervolgens kan je met de concentratie die je hebt uitgerekend de pH of de pOH (pH=14-pOH) berekenen.
pH=-log[H3O+] of pOH=-log[OH-]
• Wat moet je kunnen met buffers? Ik weet dat je een buffer krijgt als je een zuur en zijn geconjugeerde base bij elkaar doet met de verhouding [zuur]:[base] 1:10 of 10:1
(geldt dit ook voor een base en zijn geconjugeerde zuur?)
• Wat moet je kunnen met de cis/trans benamingen?
• Wat is dat spiegelisomeren, daar snap ik niks van :S
• Hoe kan je ookalweer aan een stuctuurformule van een polymeer herkennen of een stof een thermoharder of thermoplast is?
• Ik snap bij koolstofchemie nog niet hoe je oxy & yl & oaat moet tekenen? Hoe bepaal je de hoofdgroep..?
Zeeeeer veel dank voor degene die mij hieruit kan helpen
[ Bericht 8% gewijzigd door zoodan op 28-05-2012 14:16:12 ]
ah foutje, pKz=-log(Kz) toch?quote:Op maandag 28 mei 2012 14:01 schreef Intercam het volgende:
[..]
De pKz he niet de Kz. Of kan je de pKz ook ergens invullen?
ah i get it now.. pKz = 10^(-kz) alleen snap ik de purpose helemaal niet.. Ik heb nooit gezien dat de Kz gelijk is aan het aantal H3O+ deeltjes..quote:
en
Kz = 10^-(pKz)
Als je een buffer wil maken van bijvoorbeeld pH 10,5 dan gaat dat het beste met een zuur met een pKz zo dicht mogelijk bij 10,5 en zijn geconjungeerde base. pKz mag in ieder geval niet meer dan 1 verschillen (verhouding HZ/Z- tussen 10:1 en 1:10)
Kz is niet gelijk aan [H30+] maar met Kz kan je [H3o+] wel uitrekenen. Kz = [H3O+] * [Z-] / [HZ]quote:Op maandag 28 mei 2012 14:16 schreef Intercam het volgende:
[..]
ah i get it now.. pKz = 10^(-kz) alleen snap ik de purpose helemaal niet.. Ik heb nooit gezien dat de Kz gelijk is aan het aantal H3O+ deeltjes..fuck.
Als je [H3O+] wil weten noem je die x. Dan is [Z-] ook x en is [HZ] = (M-x) waar M is de concentratie die jij in oplossing hebt gebracht. Je kan dan alles omschrijven en ABC formule gebruiken om [H3o+] uit te rekenen.
Bedoel je met de allerlaatste zin dan als je een buffer wilt maken van bijvoorbeeld een pH van 3,20quote:Op maandag 28 mei 2012 14:52 schreef Sleutel13 het volgende:
pKz is -log(Kz)
en
Kz = 10^-(pKz)
Als je een buffer wil maken van bijvoorbeeld pH 10,5 dan gaat dat het beste met een zuur met een pKz zo dicht mogelijk bij 10,5 en zijn geconjungeerde base. pKz mag in ieder geval niet meer dan 1 verschillen (verhouding HZ/Z- tussen 10:1 en 1:10)
Dan doe je dus het zuur HF en zijn geconjugeerde base F- want de pKz is daar 3,20 (dit kan je toch ook benoemen als de base F- met het geconjugeerde zuur HF?) bij elkaar met de concentratie verhouding [HF]:[F-] tussen de 10:1 en de 1:10?
dus je hebt dan een buffer met een pH van 3,20 als je 4M HF doet bij 20M F-?
De pH zal tussen de 4,20 en 2,20 liggen aan de hand van de verhouding. Verhouding 1:1 geeft 3,20, 10:1 geeft 2,20 en 1:10 geeft 4,20.quote:Op maandag 28 mei 2012 14:59 schreef zoodan het volgende:
[..]
Bedoel je met de allerlaatste zin dan als je een buffer wilt maken van bijvoorbeeld een pH van 3,20
Dan doe je dus het zuur HF en zijn geconjugeerde base F- want de pKz is daar 3,20 (dit kan je toch ook benoemen als de base F- met het geconjugeerde zuur HF?) bij elkaar met de concentratie verhouding [HF]:[F-] tussen de 10:1 en de 1:10?
dus je hebt dan een buffer met een pH van 3,20 als je 4M HF doet bij 20M F-?
Uit de Kz formule kan je de volgende formule afleiden:
pH=pKz - log ( [HZ]/[Z-] )
Als je een pH= 3,20 buffer wil maken met HNO2 en NO2- kan je invullen 3,20 = 3.25 -log ( [HNO2] / [NO2-] )
Thanks, kom je aan die 2,20 en 4,20 door die formule in te vullen aan het eind?quote:Op maandag 28 mei 2012 15:11 schreef Sleutel13 het volgende:
[..]
De pH zal tussen de 4,20 en 2,20 liggen aan de hand van de verhouding. Verhouding 1:1 geeft 3,20, 10:1 geeft 2,20 en 1:10 geeft 4,20.
Uit de Kz formule kan je de volgende formule afleiden:
pH=pKz - log ( [HZ]/[Z-] )
Als je een pH= 3,20 buffer wil maken met HNO2 en NO2- kan je invullen 3,20 = 3.25 -log ( [HNO2] / [NO2-] )
Je zet de constante op zoals die in het correctie model staat.quote:Op maandag 28 mei 2012 12:13 schreef TheDutchguy het volgende:
Kan iemand me uitleggen hoe ze vraag 7 van 2011-2 uitrekenen? Ik snap die evenwichtsvoorwaarde nog en die Kz, maar hoe ze bij die berekening komen snap ik niks van.
http://static.examenblad.nl/9336110/d/ex2010/vw-1028-a-10-2-o.pdf (opdrachten)
http://static.examenblad.nl/9336110/d/ex2010/vw-1028-a-10-2-c.pdf (correctievoorschrift)
Er staat dan eigenlijk; x^2/M-x=kz
kz is gegeven
M is gegeven( die kun je uit de gegeven pH(7,5) berekenen.)
bereken x met graph
De verhouding propanoaat-propaanzuur is dan dus propanoaat delen door propaanzuur
propanoaat= x
propaanzuur= M-x
x/M-x= antwoord

Binas 70E; van beide zijn er 2 en in beide gevallen begint Glu met een G en Lys met een A.
Die G is dus puntgemuteerd naar A.
coderende streng base == base op het mRNA
dus normaal G met intolerantie A
coderende streng base =andere kant= matrijsstreng
G wordt C en A wordt T
dus normaal C met intolerantie T
toch?
http://static.examenblad.nl/9336111/d/ex2011/vw-1028-a-11-1-c.pdf
''Plaats 487 van een aminozuur in aceetaldehyde-dehydrogenase komt overeen met plaats 504 in het polypeptide dat daaraan voorafgaat. De voorafgaande 503 aminozuren zijn gecodeerd door 3*503 = 1509 basen. De puntmutatie treedt op bij de eerste base van het aminozuur 504. De puntmutatie betreft dus base 1509+1 = 1510.''quote:Op maandag 28 mei 2012 17:17 schreef CrosbyStills het volgende:
kan iemand mij alsjeblieft uitleggen hoe vraag 5 van 2010 2 moet??
[ afbeelding ]
Geen examenbundel?
kloppend maken. rechts heb je 1x een lading -1. links heb je -2 en +9 (samen +7). je stopt er 8- bij en ze zijn gelijk.quote:Op maandag 28 mei 2012 17:33 schreef TheDutchguy het volgende:
Ah, dankje Destroyer. Nog een vraagje, bij vraag 15, hoe komen ze aan die 8 elektronen?
http://static.examenblad.nl/9336111/d/ex2011/vw-1028-a-11-1-c.pdf
hopelijk een beetj duidelijk
edit: vraag gelezen..quote:Op maandag 28 mei 2012 17:34 schreef Reimerrr het volgende:
[..]
''Plaats 487 van een aminozuur in aceetaldehyde-dehydrogenase komt overeen met plaats 504 in het polypeptide dat daaraan voorafgaat. De voorafgaande 503 aminozuren zijn gecodeerd door 3*503 = 1509 basen. De puntmutatie treedt op bij de eerste base van het aminozuur 504. De puntmutatie betreft dus base 1509+1 = 1510.''
Geen examenbundel?
[ Bericht 8% gewijzigd door dramatic op 28-05-2012 17:46:01 ]
is dat zo'n batterij?quote:Op maandag 28 mei 2012 17:46 schreef PG18 het volgende:
Moeten we de elektrochemische cel ook kennen? In het boek "Chemie overal" staat er "SE" bij...
Ja.quote:
Oh, tuurlijk, de hele reactie moet 0 wordenquote:Op maandag 28 mei 2012 17:35 schreef dramatic het volgende:
[..]
kloppend maken. rechts heb je 1x een lading -1. links heb je -2 en +9 (samen +7). je stopt er 8- bij en ze zijn gelijk.
hopelijk een beetj duidelijk
[ Bericht 100% gewijzigd door m4urit5 op 28-05-2012 18:24:46 ]
Nee volgens samengevat is de idd SE stof en geen CE stofquote:Op maandag 28 mei 2012 17:46 schreef PG18 het volgende:
Moeten we de elektrochemische cel ook kennen? In het boek "Chemie overal" staat er "SE" bij...
[1] Ik denk niet heel veel, komt weinig voor. De meeste sommen hierover zijn gewoon op te lossen door de evenwichtsvoorwaarde op te schrijven en hiermee te gaan rekenen.quote:Op maandag 28 mei 2012 14:03 schreef zoodan het volgende:
[1]Wat moet je kunnen met buffers? Ik weet dat je een buffer krijgt als je een zuur en zijn geconjugeerde base bij elkaar doet met de verhouding [zuur]:[base] 1:10 of 10:1
(geldt dit ook voor een base en zijn geconjugeerde zuur?)
[2]Wat moet je kunnen met de cis/trans benamingen?
[3]Wat is dat spiegelisomeren, daar snap ik niks van :S
[4]Hoe kan je ookalweer aan een stuctuurformule van een polymeer herkennen of een stof een thermoharder of thermoplast is?
[5]Ik snap bij koolstofchemie nog niet hoe je oxy & yl & oaat moet tekenen? Hoe bepaal je de hoofdgroep..?
[2] Weten dat cis betekent ''twee dezelfde groepen zijn dezelfde kant op gericht t.o.v. de dubbele binding'' en trans ''van twee dezelfde groepen is er een naar 'boven' en een naar onder gericht t.o.v. de dubbele binding'' en daarmee kunnen naamgeven etc.
[3] Een vorm van isomerie waarbij als je de moleculen naast elkaar tekent je ze op een bepaalde manier zo kan draaien dat ze elkaars spiegelbeeld zijn. Ze verschillen niet in eigenschappen en ook niet in structuur.
[4] Een thermoharder is een netwerk molecuul; je kan dan van de ene'' ~~~~'' aan het einde van het molecuul op meerdere manieren naar een andere ''~~~~'' komen (zo herken ik het tenminste altijd)
[5] De 'hoofdgroep'' (de oaat etc.) is dacht ik altijd de zuurrest. De -yl is de rest van een alcohol. (ik heb het nu over esters)
Die waardes staan dus niet in binas en moeten worden gegeven, Kz kan je wel in die breuk gebruiken:quote:Op maandag 28 mei 2012 18:35 schreef dvdsrk het volgende:
hoe bereken/vind in binas je de waardes die je in een concentratiebreuk moet invullen?
pA + qB <> sC + tD =( ([C]^s)([D]^t)/([A]^p)([B]^q) = Kz)
alle concentraties worden dus altijd gegeven?quote:Op maandag 28 mei 2012 18:37 schreef metanite het volgende:
[..]
Die waardes staan dus niet in binas en moeten worden gegeven, Kz kan je wel in die breuk gebruiken:
pA + qB <> sC + tD =( ([C]^s)([D]^t)/([A]^p)([B]^q) = Kz)
Zover ik weet wel, misschien kan iemand mij nog bevestigen?quote:Op maandag 28 mei 2012 18:40 schreef dvdsrk het volgende:
[..]
alle concentraties worden dus altijd gegeven?
Bedankt!quote:Op maandag 28 mei 2012 18:36 schreef m4urit5 het volgende:
[..]
[1] Ik denk niet heel veel, komt weinig voor. De meeste sommen hierover zijn gewoon op te lossen door de evenwichtsvoorwaarde op te schrijven en hiermee te gaan rekenen.
[2] Weten dat cis betekent ''twee dezelfde groepen zijn dezelfde kant op gericht t.o.v. de dubbele binding'' en trans ''van twee dezelfde groepen is er een naar 'boven' en een naar onder gericht t.o.v. de dubbele binding'' en daarmee kunnen naamgeven etc.
[3] Een vorm van isomerie waarbij als je de moleculen naast elkaar tekent je ze op een bepaalde manier zo kan draaien dat ze elkaars spiegelbeeld zijn. Ze verschillen niet in eigenschappen en ook niet in structuur.
[4] Een thermoharder is een netwerk molecuul; je kan dan van de ene'' ~~~~'' aan het einde van het molecuul op meerdere manieren naar een andere ''~~~~'' komen (zo herken ik het tenminste altijd)
[5] De 'hoofdgroep'' (de oaat etc.) is dacht ik altijd de zuurrest. De -yl is de rest van een alcohol. (ik heb het nu over esters)
Alleen hoe weet je welke je moet kiezen van je stof? Bij MnO4- zijn bijvoorbeeld best veel mogelijkheden, welke kies je dan?
de sterkst mogelijke (oxidator v.a. linksboven, reductor v.a. rechtsonder) en afhankelijk welke deeltjes verder aanwezig zijn. MnO4- + 8H+ + 5 e- is bijvoorbeeld wel een erg sterke oxidator, maar kan alleen als er ook H+-jes zijn.quote:Op maandag 28 mei 2012 18:52 schreef zoodan het volgende:
Als je een redoxreactie moet opstellen dan kun je in tabel 48 de halfreacties opzoeken.
Alleen hoe weet je welke je moet kiezen van je stof? Bij MnO4- zijn bijvoorbeeld best veel mogelijkheden, welke kies je dan?
oke, dankje!quote:Op maandag 28 mei 2012 18:47 schreef metanite het volgende:
[..]
Zover ik weet wel, misschien kan iemand mij nog bevestigen?
genoeg om een 4 te halen of is dit maar een klein deel van de punten?
Bij blokschema's vind ik het altijd onduidelijk welke stoffen je moet recirculeren in een vorige reactor onder het mom van "alles wat eruit komt moet er ergens ingaan"
Iemand een denktip hiervoor?
ik denk dat dat zo'n beetje alle stof al is.quote:Op maandag 28 mei 2012 19:05 schreef zoodan het volgende:
ik snap nu de redoxreacties, de zuur base reacties, normale reacties, koolstofchemie een beetje, standaard molberekeningen (beetje titraties enzo), blokschema's een beetje
genoeg om een 4 te halen of is dit maar een klein deel van de punten?
Bij blokschema's vind ik het altijd onduidelijk welke stoffen je moet recirculeren in een vorige reactor onder het mom van "alles wat eruit komt moet er ergens ingaan"
Iemand een denktip hiervoor?
volgens mij wordt over het algemeen zo veel mogelijk hergebruikt (i.v.m. kostenbesparing, milieu...) in een eerder reactievat, echt een tip heb ik hier niet voor, het is vooral goed lezen en het schema duidelijk proberen te houden (doe het eerst met potlood, zodat je fouten niet hoeft door te krassen, maar kan uitgummen, aan het eind niet vergeten alsnog met pen te doen!)
Van DNA komt er soms ook nog wat van in.quote:Op maandag 28 mei 2012 19:05 schreef zoodan het volgende:
ik snap nu de redoxreacties, de zuur base reacties, normale reacties, koolstofchemie een beetje, standaard molberekeningen (beetje titraties enzo), blokschema's een beetje
genoeg om een 4 te halen of is dit maar een klein deel van de punten?
Bij blokschema's vind ik het altijd onduidelijk welke stoffen je moet recirculeren in een vorige reactor onder het mom van "alles wat eruit komt moet er ergens ingaan"
Iemand een denktip hiervoor?
Lijkt mij wel , ben je dan geslaagd? Of heb je nog meer examensquote:Op maandag 28 mei 2012 19:45 schreef zoodan het volgende:
Dus een 4 halen met wat ik zei is goed te doen?
Alleen nog economie en fransquote:Op maandag 28 mei 2012 19:46 schreef metanite het volgende:
[..]
Lijkt mij wel , ben je dan geslaagd? Of heb je nog meer examens
Frans haal ik een 9 of 10 (spreek het vloeiend) en eco gaat ook lukken
Scheikunde: 2008 — 2e tijdvak vraag 6 is een voorbeeld.
er komt altijd wel 1 zo'n rot vraagje, maar hoe begin ik of is er een stappenplan?
Ah nice als ik morgen een 5,5 weet te halen komt het einde van mijn middelbare school carriere ook wel in de buurt (vrijdag nog spaans) netzoals het mooie weerquote:Op maandag 28 mei 2012 19:47 schreef zoodan het volgende:
[..]
Alleen nog economie en frans
Frans haal ik een 9 of 10 (spreek het vloeiend) en eco gaat ook lukken
succes!quote:Op maandag 28 mei 2012 19:51 schreef metanite het volgende:
[..]
Ah nice als ik morgen een 5,5 weet te halen komt het einde van mijn middelbare school carriere ook wel in de buurt (vrijdag nog spaans) netzoals het mooie weer
Jij ook, je andere examens zijn blijkbaar allemaal wel redelijk goed gegaan ? Ik heb denk voor alles tussen de 5,5 en 6,5 heb al spijt van natuur en wiskunde die had ik veel beter kunnen maken. Wiskunde ga ik denk wel herkansen ook al heb ik het gehaaldquote:
Lijkt mij prima haalbaarquote:
zometeen samengevat eens lezenquote:
Ja, idd zo'n beetje alle stof..quote:Op maandag 28 mei 2012 19:10 schreef dvdsrk het volgende:
[..]
ik denk dat dat zo'n beetje alle stof al is.
volgens mij wordt over het algemeen zo veel mogelijk hergebruikt (i.v.m. kostenbesparing, milieu...) in een eerder reactievat, echt een tip heb ik hier niet voor, het is vooral goed lezen en het schema duidelijk proberen te houden (doe het eerst met potlood, zodat je fouten niet hoeft door te krassen, maar kan uitgummen, aan het eind niet vergeten alsnog met pen te doen!)
Ik heb een 5.5 nodig.. En ik moet nog zuur basen doen en titraties/blokschema's..quote:Op maandag 28 mei 2012 19:45 schreef zoodan het volgende:
Dus een 4 halen met wat ik zei is goed te doen?
Dus die 4 haal je zeker, zelfs als je (bijna) niets weet
blokschema's zullen wss niet belangrijk zijn. Er is namelijk geen uitwerkbijlage. Maar wie weetquote:Op maandag 28 mei 2012 20:11 schreef MissEll het volgende:
[..]
Ik heb een 5.5 nodig.. En ik moet nog zuur basen doen en titraties/blokschema's..
Dus die 4 haal je zeker, zelfs als je (bijna) niets weet
Staat best veel nuttigs in! Best veel nieuwe dingen geleerd toen ik hem doorbladerde.quote:Op maandag 28 mei 2012 20:02 schreef dramatic het volgende:
[..]
zometeen samengevat eens lezenmoet goedkomen.. jullie ook succes
Khoop t ook niet.. Maar idd, je weet het nooit helemaal zeker van tevoren..quote:Op maandag 28 mei 2012 20:12 schreef dramatic het volgende:
[..]
blokschema's zullen wss niet belangrijk zijn. Er is namelijk geen uitwerkbijlage. Maar wie weet
Geen garantie bij 2010 II was dat ook zo , maar toen moest je hem overtekenenquote:Op maandag 28 mei 2012 20:12 schreef dramatic het volgende:
[..]
blokschema's zullen wss niet belangrijk zijn. Er is namelijk geen uitwerkbijlage. Maar wie weet
Herkansing is net zo moeilijk of zelfs moeilijker?
Ohhh, stresss..
Nu kraam je toch echt onzin uit, welk vak wil je nou wel graag herkansen. De herkansingen zijn in principe van hetzelfde niveau als de 'normale' examens, ligt er dus aan hoe het onderwerp jou ligt. Ze maken een herkansing echt niet moeilijker -_-quote:Op maandag 28 mei 2012 20:35 schreef MissEll het volgende:
Scheikunde is een vak die je sowieso niet wilt herkansen toch?
Herkansing is net zo moeilijk of zelfs moeilijker?
Ohhh, stresss..
't was eerder een vraag.. Rustig aan.quote:Op maandag 28 mei 2012 20:37 schreef metanite het volgende:
[..]
Nu kraam je toch echt onzin uit, welk vak wil je nou wel graag herkansen. De herkansingen zijn in principe van hetzelfde niveau als de 'normale' examens, ligt er dus aan hoe het onderwerp jou ligt. Ze maken een herkansing echt niet moeilijker -_-
je bent toch wel beter dan ikquote:
Dus eigenlijk zit je hier alleen maar paniek te zaaien ?quote:
Nee..quote:
Stil jij. Ik doe niets.quote:Op maandag 28 mei 2012 20:43 schreef metanite het volgende:
[..]
Dus eigenlijk zit je hier alleen maar paniek te zaaien ?
Waar kan je zien dat er geen uitwerkbijlage is?quote:Op maandag 28 mei 2012 20:12 schreef dramatic het volgende:
[..]
blokschema's zullen wss niet belangrijk zijn. Er is namelijk geen uitwerkbijlage. Maar wie weet
Bij de cito staan er bij de icoontjes geen 2 blaadjesquote:Op maandag 28 mei 2012 20:47 schreef Apostrof het volgende:
[..]
Waar kan je zien dat er geen uitwerkbijlage is?
Precies dezelfde situatie als jou, alles tussen de 5-6,5 ongeveer, spannend nog! en latijn heb ik verneukt hahaquote:Op maandag 28 mei 2012 20:00 schreef metanite het volgende:
[..]
Jij ook, je andere examens zijn blijkbaar allemaal wel redelijk goed gegaan ? Ik heb denk voor alles tussen de 5,5 en 6,5 heb al spijt van natuur en wiskunde die had ik veel beter kunnen maken. Wiskunde ga ik denk wel herkansen ook al heb ik het gehaald
Bij hydrolyse doe je er water bij en bij verzeping doe je er een base(OH-) bijquote:Op maandag 28 mei 2012 20:55 schreef Joeyhill het volgende:
Kan iemand mij trouwens hier het verschil uitleggen tussen hydrolyse en verzeping?
Bij mij ook spannend hoor:P maar kan wib nog altijd herkansen en dan een 8 halen. Als ik in een keer slaag word het denk een lange nachtquote:Op maandag 28 mei 2012 20:52 schreef zoodan het volgende:
[..]
Precies dezelfde situatie als jou, alles tussen de 5-6,5 ongeveer, spannend nog! en latijn heb ik verneukt haha

Thanks! En ontstaan bij beide de beginproducten weer?quote:Op maandag 28 mei 2012 20:56 schreef h.lalala het volgende:
[..]
Bij hydrolyse doe je er water bij en bij verzeping doe je er een base(OH-) bij
Nekhernia krijg ik van dit soort scansquote:Op maandag 28 mei 2012 20:58 schreef zoodan het volgende:
Snapt iemand wat er helemaal onderaan staat? Ik wist niet dat er logica zat in die molecuulformule..?
[ afbeelding ]
haha ja precies!!quote:Op maandag 28 mei 2012 20:57 schreef metanite het volgende:
[..]
Bij mij ook spannend hoor:P maar kan wib nog altijd herkansen en dan een 8 halen. Als ik in een keer slaag word het denk een lange nacht
Deze heb ik ook geprobeerd, ik snapte het ook niet dus ik ga morgen nog even naar mn leraarquote:Op maandag 28 mei 2012 20:58 schreef zoodan het volgende:
Snapt iemand wat er helemaal onderaan staat? Ik wist niet dat er logica zat in die molecuulformule..?
[ afbeelding ]
Wat is je vraag nou precies?quote:Op maandag 28 mei 2012 20:58 schreef zoodan het volgende:
Snapt iemand wat er helemaal onderaan staat? Ik wist niet dat er logica zat in die molecuulformule..?
[ afbeelding ]
Maar ik snap niet hoe je dit kunt zien..?
(haha sorry dat hij schuin is, op mijn computer staat hij gewoon rechtop..?)
Dat ding meet namelijk ook 'bindingen' in een molecuul en niet alleen hele moleculen. Bij H2O zou je bijvoorbeeld niet alleen een piek zijn bij H2O maar ook bij HO (omdat in de structuurformule een O aan een H vast zit) maar bijvoorbeeld niet bij HH want die zijn niet aan elkaar gebonden.
Er stond: Je weet dat er 1 Cl, 1 N en 1 O is.
De vraag was: zitten O aan de Cl vast of zitten de N aan de Cl vast?
Als de O an de Cl vast zit zou je een piek moeten zien bij O + Cl = 16 + 35 = 53
En bij N aan de Cl: N + Cl = 14 + 35 = 51
Er zit echter geen piek bij m/z = 53, dus er bestaat geen binding OCl, er is wel een m/z = 51 welke overeenkomt met een binding NCl.
Ik snap de hele vraag al niet, er wordt een vraag gesteld maar ik snap niet wat je moet doenquote:
aaah ik zie hem! thanks!!quote:Op maandag 28 mei 2012 21:08 schreef Lilliesleaf het volgende:
Volgens mij zit je met het probleem dat je niet snapt hoe zo'n massaspectrometer werkt:
Dat ding meet namelijk ook 'bindingen' in een molecuul en niet alleen hele moleculen. Bij H2O zou je bijvoorbeeld niet alleen een piek zijn bij H2O maar ook bij HO (omdat in de structuurformule een O aan een H vast zit) maar bijvoorbeeld niet bij HH want die zijn niet aan elkaar gebonden.
Er stond: Je weet dat er 1 Cl, 1 N en 1 O is.
De vraag was: zitten O aan de Cl vast of zitten de N aan de Cl vast?
Als de O an de Cl vast zit zou je een piek moeten zien bij O + Cl = 16 + 35 = 53
En bij N aan de Cl: N + Cl = 14 + 35 = 51
Er zit echter geen piek bij m/z = 53, dus er bestaat geen binding OCl, er is wel een m/z = 51 welke overeenkomt met een binding NCl.
Goedzo!
Kijk uit wat je nu zegt! Want dat is ook niet zo! De molecuulformule zegt niks over de manier waarop ze verbonden zijn.. neem.. glucose als voorbeeld met formule C6H12O6quote:Op maandag 28 mei 2012 21:23 schreef zoodan het volgende:
Jep! Ik had dit echter niet gezocht achter een molecuulformule want ik wist niet dat die volgorde ook aangaf dat ze met elkaar gebonden waren zegmaar.
Dit is een van de structuurformules van glucose:
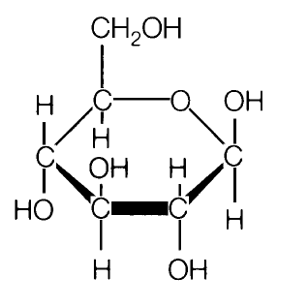
Je kunt glucose net zo goed schrijven als H12O6C6 en het is dan nog steeds glucose.
daarom was die vraag op dat blad ook raar gesteld.quote:Op maandag 28 mei 2012 21:28 schreef Lilliesleaf het volgende:
[..]
Kijk uit wat je nu zegt! Want dat is ook niet zo! De molecuulformule zegt niks over de manier waarop ze verbonden zijn.. neem.. glucose als voorbeeld met formule C6H12O6
Dit is een van de structuurformules van glucose:
[ afbeelding ]
Je kunt glucose net zo goed schrijven als H12O6C6 en het is dan nog steeds glucose.
Welk cijfer moet je ongeveer halen?quote:Op maandag 28 mei 2012 21:29 schreef dramatic het volgende:
[..]
daarom was die vraag op dat blad ook raar gesteld.
Ja!quote:Op maandag 28 mei 2012 20:59 schreef Joeyhill het volgende:
[..]
Thanks! En ontstaan bij beide de beginproducten weer?
Alleen maar dingen beredeneren vanuit informatie uit de Binas en de tekst, de rest erbuiten houden?quote:Op maandag 28 mei 2012 21:32 schreef Lilliesleaf het volgende:
Mijn probleem met scheikunde: Ik weet meer dan de stof en daarom kan ik niet meer 'makkelijk' denken. Ik ben dan altijd op zoek naar oplossingen die naar mijn idee al makkelijk zijn, maar die alweer 3x zo moeilijk zijn als het antwoord waar ze naar op zoek zijn. Met als gevolg: Je komt niet op het goede antwoord.
Zie daar mijn probleem, ik het antwoord is altijd A + B = C ... mijn hoofd doet: Het antwoord is A + B + EDG en je moet ook rekeningen houden met F..quote:Op maandag 28 mei 2012 21:37 schreef Apostrof het volgende:
[..]
Alleen maar dingen beredeneren vanuit informatie uit de Binas en de tekst, de rest erbuiten houden?
Wat meestal in de praktijk ook zo is.. alleen niet.. wat betreft eindexamens.
Echt alleen maar beredeneren met behulp van informatie uit de tekst + Binas + kennis uit klas 4quote:Op maandag 28 mei 2012 21:39 schreef Lilliesleaf het volgende:
[..]
Zie daar mijn probleem, ik het antwoord is altijd A + B = C ... mijn hoofd doet: Het antwoord is A + B + EDG en je moet ook rekeningen houden met F..
Wat meestal in de praktijk ook zo is.. alleen niet.. wat betreft eindexamens.
haha hoe kom je aan al die kennis dan?quote:Op maandag 28 mei 2012 21:39 schreef Lilliesleaf het volgende:
[..]
Zie daar mijn probleem, ik het antwoord is altijd A + B = C ... mijn hoofd doet: Het antwoord is A + B + EDG en je moet ook rekeningen houden met F..
Wat meestal in de praktijk ook zo is.. alleen niet.. wat betreft eindexamens.
zo hoog mogelijkquote:
Ten eerste gewoon aanleg voor beta's en dat ik scheikunde ga studeren, vrienden heb die scheikunde studeren.. veel met hun praat over hoe en wat, af en toe mee ga naar een college.. etc.quote:
(en omdat onze docenten nooit iets �cht structureel hebben uitgelegd en ik daarom geen basis heb om op terug te vallen, als in, stap a leidt tot b leidt tot c en dan STOP! Alles wat ik dus weet is meer via.. die vrienden dan via school
Hmm, oke, een 5 moet zeker lukken!quote:
Succes morgen
een 4 is 1/3 van de punten... moet lukkenquote:Op maandag 28 mei 2012 21:51 schreef MissEll het volgende:
[..]
Hmm, oke, een 5 moet zeker lukken!
Succes morgen
dankje, jij ook
Idd! Dank je welll. :pquote:
Ik sta een 8,5 en wil dit graag zo houden
Aan 20 ml fosforzuuroplossing wordt 40 ml 0,25 M natronloog toegevoegd. De overmaat natronloog wordt getitreerd met 7,2 ml 1,0 M zoutzuur.
Vraag: wat was de concentratie van het fosforzuur (H3PO4)?
You gotta be kidding me bro.quote:Op maandag 28 mei 2012 23:00 schreef Lilliesleaf het volgende:
20 ml fosforzuur vs 40 ml natronloog met een redelijke molariteit. Met andere woorden: natronloog is in overmaat.
Ja maar hoe weet je de concentratie van fosforzuur?quote:Op maandag 28 mei 2012 23:00 schreef Lilliesleaf het volgende:
20 ml fosforzuur vs 40 ml natronloog met een redelijke molariteit. Met andere woorden: natronloog is in overmaat.
eeh.. het staat verder zelf ook in de vraag.quote:
Maar, verder: Die OH- 'tjes van de natronloog trekke alle H+'jes die ze maar te pakken kunnen krijgen van het zwakke zuur naar zich toe, vandaar dat alle drie de H+ 'jes van fosforzuur eraf gaan.
quote:Op maandag 28 mei 2012 22:46 schreef zoodan het volgende:
Hoe weet je trouwens bij deze vraag de reactievergelijking? Want volgens het antwoord worden alle 3 de waterstofatomen uit fosforzuur afgestaan, maar waarom?
Aan 20 ml fosforzuuroplossing wordt 40 ml 0,25 M natronloog toegevoegd. De overmaat natronloog wordt getitreerd met 7,2 ml 1,0 M zoutzuur.
Vraag: wat was de concentratie van het fosforzuur (H3PO4)?
wat was het antwoord? wil ff kijken of ik hem goed heb :pquote:Op maandag 28 mei 2012 22:46 schreef zoodan het volgende:
Hoe weet je trouwens bij deze vraag de reactievergelijking? Want volgens het antwoord worden alle 3 de waterstofatomen uit fosforzuur afgestaan, maar waarom?
Aan 20 ml fosforzuuroplossing wordt 40 ml 0,25 M natronloog toegevoegd. De overmaat natronloog wordt getitreerd met 7,2 ml 1,0 M zoutzuur.
Vraag: wat was de concentratie van het fosforzuur (H3PO4)?
H3O+ + OH- -� 2H2O ?
En n = 1,0 • 7,25•10^-3
Je weet hoeveel zoutzuur je nodig had om het overige natronloog weg te werken (bereken eerst hoeveel mol 7,2 ml/1,0 M zoutzuur is en dan HCl : NaOH als 1 : 1). Nu weet je hoe veel van die 40 ml natronloog naar het fosforzuur is gegaan en hoeveel naar het zoutzuur.quote:Op maandag 28 mei 2012 23:03 schreef h.lalala het volgende:
[..]
Ja maar hoe weet je de concentratie van fosforzuur?
Je weet: fosforzuur : natronloog als 3 : 1 , dus die aantal ml natronloog die naar het fosforzuur is gegaan omrekenen naar mol. Delen door 3. Dan heb je het aantal mol fosforzuur, delen door volume en je hebt concentratie.
.. wat ben je hier aan het doen?quote:Op maandag 28 mei 2012 23:06 schreef h.lalala het volgende:
Ik zou niet verder komen dan reactievergelijking opstellen..
H3O+ + OH- -� 2H2O ?
En n = 1,0 • 7,25•10^-3
Het is fosforzuur met natronloog. Fosfor zuur is H3PO4, aldus machtige binas tabel 66B.
Wat jij doet: H3O+ + OH- is het waterevenwicht, namelijk:
H3O+ + OH- <=> H2O
Dankje!! Is het antwoord 0,42 M? :$quote:Op maandag 28 mei 2012 23:10 schreef Lilliesleaf het volgende:
[..]
Je weet hoeveel zoutzuur je nodig had om het overige natronloog weg te werken (bereken eerst hoeveel mol 7,2 ml/1,0 M zoutzuur is en dan HCl : NaOH als 1 : 1). Nu weet je hoe veel van die 40 ml natronloog naar het fosforzuur is gegaan en hoeveel naar het zoutzuur.
Je weet: fosforzuur : natronloog als 3 : 1 , dus die aantal ml natronloog die naar het fosforzuur is gegaan omrekenen naar mol. Delen door 3. Dan heb je het aantal mol fosforzuur, delen door volume en je hebt concentratie.
Dus omdat de OH- in overmaat is worden alle H-tjes weggehaald?
Hierbij de uitwerking

Ja. Zodra er staat overmaat moet je denken: alles van dat sterke/zwakke zuur (want dat is het meestal) reageert weg.quote:Op maandag 28 mei 2012 23:22 schreef zoodan het volgende:
Pff ik hoop dat er ook een paar vragen zijn die makkelijker zijn dat dit hoor.. :s
Dus omdat de OH- in overmaat is worden alle H-tjes weggehaald?
Hierbij de uitwerking
[ afbeelding ]
Edit: ik snap dat die uitwerking een beetje intimiderend overkomt, heb je nog een titratie-oefening? Ik kan wel even kijken of ik een standaard stappenplan voor je kan schrijven op basis daarvan.
Oke bedankt, pff ik mis echt veel van dit soort kleine tips, zou jij weten waar ik dit soort tips kan vinden? Heeft iemand er misschien een paar?quote:Op maandag 28 mei 2012 23:26 schreef Lilliesleaf het volgende:
[..]
Ja. Zodra er staat overmaat moet je denken: alles van dat sterke/zwakke zuur (want dat is het meestal) reageert weg.
Een paar van mij dan ook haha
Bij evenwicht A + 2B ↔ 3C + D
Stof A toevoegen --> Rechts, om A af te breken
Stof B weghalen -->Links, om B bij te maken
Druk verhogen = volume verkleinen = alle concentraties verhogen -->Links, kant met de minste deeltjes (minste aantal mol=minste aantal deeltjes)
Katalysator toevoegen --> Er gebeurt niks
Temperatuur verlagen-->Links, exotherme kant
Omdat de molariteit anders is. De HCl oplossing is 1,0 mol per liter. De NaOH oplossing 0,25 mol per liter.quote:Op maandag 28 mei 2012 23:29 schreef h.lalala het volgende:
Ik snap dat niet. De verhouding tussen NaOH en HCl is toch 1:1, dus als je weet hoeveel n reageert van HCl, dan is dat toch gelijk aan dat van NaOH. Waarom berekenen zij n van NaOH ook apart uit?
Edit: Dus je kunt niet zomaar zeggen, 7,2 milliliter HCl reageert met 7,2 millilter NaOH, omdat er in de 7,2 milliliter NaOH minder NaOH zit dan HCl in 7,2 milliliter HCl. (Het zijn beide oplossingen van die stof in water)
Vind het btw wel een beetje diep op de theorie ingaan, ik snap het als je hier moeite mee hebt.
Maar hier ook zo'n titratievraag dat ik echt niet kan beantwoorden.
Het schoonmaakmiddel wc-eend bevat volgens het etiket mierenzuur (=methaanzuur, HCOOH).
Uit een wc-eend wordt 25 mL gepipetteerd in een maatkolf van 200 mL. Na aanvuullen met water en homogeniseren wordt hieruit 25 mL overgebracht in een titratievat. Er blijkt 33,43 mL van een 0,2032 M oplossing van natriumhydroxide nodig te zijn. Een dubbelbepaling verbruikt 33,49 mL van deze natronloog.
Vraag: bereken het gehalte mierenzuur in het schoonmaakmiddel in g/L
-.-"
quote:Op maandag 28 mei 2012 23:47 schreef h.lalala het volgende:
Ja klopt, thanks!
Maar hier ook zo'n titratievraag dat ik echt niet kan beantwoorden.
Het schoonmaakmiddel wc-eend bevat volgens het etiket mierenzuur (=methaanzuur, HCOOH).
Uit een wc-eend wordt 25 mL gepipetteerd in een maatkolf van 200 mL. Na aanvuullen met water en homogeniseren wordt hieruit 25 mL overgebracht in een titratievat. Er blijkt 33,43 mL van een 0,2032 M oplossing van natriumhydroxide nodig te zijn. Een dubbelbepaling verbruikt 33,49 mL van deze natronloog.
Vraag: bereken het gehalte mierenzuur in het schoonmaakmiddel in g/L
-.-"
Doel: het mierenzuur in g/L
Wat weet je:
uit de verpakking 25 mL, verdunt met 200-25 = 175 mL water.
Voor 25 mL verdund schoonmaakmiddel 33,43 mL/0,2032 M NaOH 1ste keer nodig en tweede keer 33,49/0,2032 M
Hint woordjes:
Aanvullen met water -> je werkt met een verdunning, op het laatst moet je dit weer terugbrengen naar oorspronkelijke concentratie.
Dubbelbepaling (duplo, triplo etc) -> je rekent met het gemiddeldes van de titraties.
Stap 1: Bepaal van alle stoffen het aantal mol. (te beginnen met de stof waar je de meeste gegevens over hebt)
- NaOH: Bepaal het gemiddelde aantal mL wat je hebt gebruikt. Reken dit om via de molariteit naar aantal mol.
- Mierenzuur: Je weet NaOH : HCOOH als 1 : 1 , want mierenzuur is een eenwaardig zuur.
Stap 2: bepaal de molariteit van de onbekende stof, mierenzuur.
Je wist via stap 1 al hoeveel mol er in de 25 ml verdunde oplossing zat (daar heb je immers mee getitreerd). Bereken hieruit de molariteit.
Snap dat de molariteit in die 25 mL waar je mee getitreerd hebt, gelijk is aan de molariteit uit het vat waar je het hebt uit gehaald, de 200mL.
Je moest terug naar de ongeconcentreerde vorm. Snap daarbij ook dat de M van die 25 mL ongeconcentreerd gelijk is aan de hele verpakking. Je moet dus berekenen hoeveel mol mierenzuur er in die 25 mL zat.
Al het mierenzuur waar je mee hebt getitreerd komt oorspronkelijk uit die 25 mL en zit dus ook volledig in je vat van 200 mL. Bereken dus hoeveel mol mierenzuur je in het vat van 200 mL hebt, en je weet hoeveel mol er in de onverdunde 25 mL zat. Bereken nu met de hoeveelheid mol en het volume de nieuwe molariteit.
Stap 3: Wat was ook alweer het doel?
het aantal g/L. Je hebt de molariteit nu, dus je weet hoeveel mol per liter er in het schoonmaak middel zit. Bereken dus nu met hoeveel gram deze hoeveelheid mol overeen komt.
Dus: 4 stappen.
Voorbereiding - Haal alle gegevens uit het stuk tekst.
Stap 1 - bereken van alle stoffen het aantal mol dat in je titratie voorkomt.
Stap 2 - bereken de molariteit
Stap 3 - bereken het uiteindelijke doel.
ps. Soms is 'het doel' stap 2 al: bereken de molariteit.
Echt top!quote:Op dinsdag 29 mei 2012 00:06 schreef Lilliesleaf het volgende:
Ok. Hoe begin je? Inventariseren van de gegevens.
Doel: het mierenzuur in g/L
Wat weet je:
uit de verpakking 25 mL, verdunt met 200-25 = 175 mL water.
Voor 25 mL verdund schoonmaakmiddel 33,43 mL/0,2032 M NaOH 1ste keer nodig en tweede keer 33,49/0,2032 M
Hint woordjes:
Aanvullen met water -> je werkt met een verdunning, op het laatst moet je dit weer terugbrengen naar oorspronkelijke concentratie.
Dubbelbepaling (duplo, triplo etc) -> je rekent met het gemiddeldes van de titraties.
Stap 1: Bepaal van alle stoffen het aantal mol. (te beginnen met de stof waar je de meeste gegevens over hebt)
- NaOH: Bepaal het gemiddelde aantal mL wat je hebt gebruikt. Reken dit om via de molariteit naar aantal mol.
- Mierenzuur: Je weet NaOH : HCOOH als 1 : 1 , want mierenzuur is een eenwaardig zuur.
Stap 2: bepaal de molariteit van de onbekende stof, mierenzuur.
Je wist via stap 1 al hoeveel mol er in de 25 ml verdunde oplossing zat (daar heb je immers mee getitreerd). Bereken hieruit de molariteit.
Snap dat de molariteit in die 25 mL waar je mee getitreerd hebt, gelijk is aan de molariteit uit het vat waar je het hebt uit gehaald, de 200mL.
Je moest terug naar de ongeconcentreerde vorm. Snap daarbij ook dat de M van die 25 mL ongeconcentreerd gelijk is aan de hele verpakking. Je moet dus berekenen hoeveel mol mierenzuur er in die 25 mL zat.
Al het mierenzuur waar je mee hebt getitreerd komt oorspronkelijk uit die 25 mL en zit dus ook volledig in je vat van 200 mL. Bereken dus hoeveel mol mierenzuur je in het vat van 200 mL hebt, en je weet hoeveel mol er in de onverdunde 25 mL zat. Bereken nu met de hoeveelheid mol en het volume de nieuwe molariteit.
Stap 3: Wat was ook alweer het doel?
het aantal g/L. Je hebt de molariteit nu, dus je weet hoeveel mol per liter er in het schoonmaak middel zit. Bereken dus nu met hoeveel gram deze hoeveelheid mol overeen komt.
Dus: 4 stappen.
Voorbereiding - Haal alle gegevens uit het stuk tekst.
Stap 1 - bereken van alle stoffen het aantal mol dat in je titratie voorkomt.
Stap 2 - bereken de molariteit
Stap 3 - bereken het uiteindelijke doel.
ps. Soms is 'het doel' stap 2 al: bereken de molariteit.
[ Bericht 0% gewijzigd door h.lalala op 29-05-2012 00:30:24 ]
Hiervoor heb je toch ook de dichtheid nodig?quote:Op dinsdag 29 mei 2012 00:06 schreef Lilliesleaf het volgende:
- NaOH: Bepaal het gemiddelde aantal mL wat je hebt gebruikt. Reken dit om via de molariteit naar aantal mol.
Je hebt het aantal mL wat je gebruikt hebt en het aantal mol per liter. Dus dan gewoon mL omrekenen naar L en dat keer de molariteit.quote:Op dinsdag 29 mei 2012 00:31 schreef dvdsrk het volgende:
[..]
Hiervoor heb je toch ook de dichtheid nodig?
Edit: zie ook dit
quote:Op zondag 27 mei 2012 16:33 schreef WalterMelon het volgende:
[..]
http://webcc.corlaercollege.nl/scheikunde/mol.png
uit tabel 99 volgens mij wel maar wat bedoel je met dat rare streepje?quote:Op dinsdag 29 mei 2012 07:41 schreef dramatic het volgende:
moet je trouwens kunnen spelen met die elektronenschillen, en uit binas 99 kunnen halen dat een stof 2+ is? en zo'n raar streepje kunnen bedenken bij NH3?
Alle examens die ik tot nu toe heb gezien daarover gingen over massaspectometrie. Je moet aan de hand van de massa van delen van een molecuul iets herleiden. Snap het zelf ook vaak niet, alles foutquote:Op dinsdag 29 mei 2012 09:35 schreef zoodan het volgende:
Pff ik snap analyse ect niet echt, wat moet ik daar mee kunnen :S
jepquote:Op dinsdag 29 mei 2012 09:59 schreef Lutte het volgende:
Alleen (g) en (aq) in de evenwichtsvoorwaarde toch?
-yl groep aan moet
Waar moet die?
Pfff ik heb zo stress voor die 4 hahaha
die propaan zijn dus 3 ctjes, aan de 2de zit die metoxy, dus een O ertussen en aan de andere kant 1 Ctje vanwege het metoxy
maar waar moet the methyl dan?
Jep die stap snap ik, maar waarom heet het dan niet buthyl ipv methylquote:Op dinsdag 29 mei 2012 10:33 schreef TheDutchguy het volgende:
Die kan alleen aan het propaan zitten aan het middelste C atoom (tegenover de ester). Als die aan de buitenkant zou zitten, zou het geen propaan zijn maar butaan.
De o gaat bv naar beneden vanaf het middelste C atoom, en de methyl groep naar boven.
hmmm ik vind dat -yl nog steeds erg lastigquote:Op dinsdag 29 mei 2012 10:36 schreef TheDutchguy het volgende:
Omdat die niet aan de ester vast zit, maar aan de andere kant van het C atoom
De o gaat bv naar beneden vanaf het middelste C atoom, en de methyl groep naar boven.
Dit antwoord werd gegeven op hoe vraag 5( de onderste ) moest.

Waarom is het 487 + 17? "Dit komt overeen met plaats 504 in het polypeptide dat daaraan voorafgaat."??? Dit is echt abracedabra voor me... haha
In het tekstje voor vraag 3 staat dat er 17 aminozuureenheden (als signaalpeptide oid) vooraf gaan voordat het de echte eiwitcode ''begint''. Deze moet je er dus nog bij optellen.quote:Op dinsdag 29 mei 2012 11:47 schreef CrosbyStills het volgende:
''Plaats 487 van een aminozuur in aceetaldehyde-dehydrogenase komt overeen met plaats 504 in het polypeptide dat daaraan voorafgaat. De voorafgaande 503 aminozuren zijn gecodeerd door 3*503 = 1509 basen. De puntmutatie treedt op bij de eerste base van het aminozuur 504. De puntmutatie betreft dus base 1509+1 = 1510.''
Dit antwoord werd gegeven op hoe vraag 5( de onderste ) moest.
[ afbeelding ]
Waarom is het 487 + 17? "Dit komt overeen met plaats 504 in het polypeptide dat daaraan voorafgaat."??? Dit is echt abracedabra voor me... haha
Als je de veelvoud van een reactievergeking opschrijft (vraag 1) is het dan fout? Dat je bijvoorbeeld elk getal ervoor *3 hebt gedaan
wel netjes beargumenteerd natuurlijk.. Punt waard?quote:Op dinsdag 29 mei 2012 17:13 schreef Duderd het volgende:
o kom op.. vraag 6.. ik had dat de drinkwater voorziening dan niet belast word.
Raar dat ik als enige tijd tekort had btw, zal wel aan mij liggen.
(2 weken geleden haalde ik een 1,4 op een proefexamen en wist ik amper wat mol was, echt heel veel geleerd in de afgelopen dagen voor scheikunde
Maar dat stond in je binasquote:
66B. Nooit gezienquote:
Nooo ik had nog gekeken maar ik zie hem nu pas rechtsonderinquote:Op dinsdag 29 mei 2012 17:50 schreef v-eraax het volgende:
En het stond ook in de tekst bij opdracht 1. Stond letterlijk ethanoaat (CH3COO-) blabla
verder klopte mijn halfreactie namelijk wel helemaal (ik had CH3COOC genomen als stof...) facking dommmm
45-47 puntjes.
hmm daar verbaas ik me over want je bent echt goed in scheikunde, je hebt in ieder geval een voldoende!quote:Op dinsdag 29 mei 2012 18:11 schreef Lilliesleaf het volgende:
Ja hoor.. ik kan alle stof aan mensen uitleggen, maar zodra ik het zelf moet doen, ben ik een typisch gevalletje 'I can count to potato'. Lang leve faalangst.
45-47 puntjes.
Ik had ook alles keer 3 in de eerste reactievergelijking.quote:Op dinsdag 29 mei 2012 16:56 schreef zoodan het volgende:
En..? Ik heb wel stomme foutjes gemaakt dus benieuwd..
Als je de veelvoud van een reactievergeking opschrijft (vraag 1) is het dan fout? Dat je bijvoorbeeld elk getal ervoor *3 hebt gedaan
53 punten btw, sta echt verstelt haal normaal altijd 5jes voor scheikunde
Klopt, heel erg goed zelfs. Ronde een 9 goed zelfs.. alleen.. juist omdat ik een goed cijfer op scheikunde belangrijk vind, raak ik in de stress v��r het examen en ik paniek tijdens het examen.. en dan kan ik niet meer helder denken.quote:Op dinsdag 29 mei 2012 18:13 schreef zoodan het volgende:
[..]
hmm daar verbaas ik me over want je bent echt goed in scheikunde, je hebt in ieder geval een voldoende!
Idd ik had ook minstens een 8 verwacht van jou, jij bent echt goed in scheikunde! Maar ik snap wat je bedoelt, dat heb ik dus bij wiskunde en ik baal er zo van dat mn beste vak niet zo goed ging. Maar je hebt alsnog wel rond de 7quote:Op dinsdag 29 mei 2012 18:20 schreef Lilliesleaf het volgende:
[..]
Klopt, heel erg goed zelfs. Ronde een 9 goed zelfs.. alleen.. juist omdat ik een goed cijfer op scheikunde belangrijk vind, raak ik in de stress v��r het examen en ik paniek tijdens het examen.. en dan kan ik niet meer helder denken.
ben bang dat dat gewoon een regel is die je kan aannemen bij blokschema´s.quote:Op dinsdag 29 mei 2012 18:44 schreef PG18 het volgende:
Vraag 16, waar in de tekst staat dat het azijnzuuranhydride weer van R2 naar R1 gaat? Ik kan het niet vinden. En toch krijg je een punt als je wel een stroom van 3 vanuit R2 naar R1 tekent. Klacht
Ik dacht dat je alleen wat in de tekst staat in een blokschema moet zetten.quote:Op dinsdag 29 mei 2012 18:50 schreef Duderd het volgende:
[..]
ben bang dat dat gewoon een regel is die je kan aannemen bij blokschema´s.
Nee (helaas) moet je rekening houden dat stoffen gerecirculeerd worden..quote:Op dinsdag 29 mei 2012 18:52 schreef PG18 het volgende:
[..]
Ik dacht dat je alleen wat in de tekst staat in een blokschema moet zetten.
Hoe zit het trouwens met vraag 18? Ik dacht dat dat vocht azijnzuur zou verdunnen waardoor juist meer nodig is om het resultaat te behalen?quote:Op dinsdag 29 mei 2012 18:52 schreef PG18 het volgende:
[..]
Ik dacht dat je alleen wat in de tekst staat in een blokschema moet zetten.
Eeh.. de hele opdracht ging erover dan er azijnzuuranhydride nodig was bij dat hout (en het hout zat in R1).. Hoe wil je er bewerkt hout uit krijgen als het niet bewerkt kan worden omdat er geen azijnzuuranhydride in ging?quote:Op dinsdag 29 mei 2012 18:52 schreef PG18 het volgende:
[..]
Ik dacht dat je alleen wat in de tekst staat in een blokschema moet zetten.
Fuckquote:Op dinsdag 29 mei 2012 18:55 schreef Lilliesleaf het volgende:
[..]
Eeh.. de hele opdracht ging erover dan er azijnzuuranhydride nodig was bij dat hout (en het hout zat in R1).. Hoe wil je er bewerkt hout uit krijgen als het niet bewerkt kan worden omdat er geen azijnzuuranhydride in ging?
Goed, jullie hebben gelijk!
Vorig jaar was het 0,8 (die was ook goed te doen toen ik 'm ging oefenen)
M'n gevoel zegt 0,4-0,6
Echt?quote:Op dinsdag 29 mei 2012 19:48 schreef kingtoppie het volgende:
Ik heb maar 17 van de 24 vragen gemaakt wegens tijdgebrek.
Na 2 uur serieus?quote:Op dinsdag 29 mei 2012 19:50 schreef Lutte het volgende:
[..]
Echt?Hier waren de meeste na twee uur klaar.. Klote
2 uur...? Lijkt me eigenlijk te kort om het goed gemaakt te kunnen hebben.
Maarja verdomme natuurkunde wiB en scheikunde die niet optimaal gingen nu
[ Bericht 6% gewijzigd door kingtoppie op 29-05-2012 20:03:45 ]
Wat een onzin is dat zeg. Ik heb die n weggelaten omdat de co�fficient van die stof toch gewoon 1 was.quote:Op dinsdag 29 mei 2012 17:46 schreef Apostrof het volgende:
Vraag 13 0 punten omdat je n bent vergeten is frustrerend
Vond hem trouwens flink makkelijk. Ach ja ik heb zeker 55/70 punten, dus ik ben tevreden. ^^
[ Bericht 2% gewijzigd door Haardkoor op 29-05-2012 20:24:30 ]
Dat is gewoon niet zo slim.. Dat heeft niks met co�fficientie te maken.quote:Op dinsdag 29 mei 2012 19:58 schreef Haardkoor het volgende:
[..]
Wat een onzin is dat zeg. Ik heb die n weggelaten omdat de co�fficient van die stof toch gewoon 1 was.
En bij vraag 23 had ik dit:
Vond hem trouwens flink makkelijk. Ach ja ik heb zeker 55/70 punten, dus ik ben tevreden. ^^
Eens. Het is wel essentieel omdat het om polymeren gaat.quote:Op dinsdag 29 mei 2012 20:07 schreef kingtoppie het volgende:
[..]
Dat is gewoon niet zo slim.. Dat heeft niks met co�fficientie te maken.
Ik heb die hele vraag ook fout, daar niet van..
toch zo'n 45 punten
Moet je maar biologie doenquote:Op dinsdag 29 mei 2012 20:15 schreef dramatic het volgende:
.. waarom geen DNA verdomme, mn beste onderdeelvorig jaar was dat een enorm stuk van de stof.
toch zo'n 45 punten
vervelend, dat had ik dus bij Engels..quote:Op dinsdag 29 mei 2012 18:20 schreef Lilliesleaf het volgende:
[..]
Klopt, heel erg goed zelfs. Ronde een 9 goed zelfs.. alleen.. juist omdat ik een goed cijfer op scheikunde belangrijk vind, raak ik in de stress v��r het examen en ik paniek tijdens het examen.. en dan kan ik niet meer helder denken.
Ik heb volgens mij wel volle punten op al die lastige bereken vragenquote:Op dinsdag 29 mei 2012 20:12 schreef Lilliesleaf het volgende:
[..]
Eens. Het is wel essentieel omdat het om polymeren gaat.
Ik heb die hele vraag ook fout, daar niet van..
quote:
Welke evolutie?quote:Op dinsdag 29 mei 2012 20:16 schreef dramatic het volgende:
[..]graag gedaan maar niet op een school vol evolutieontkenners.
Ja wat nou evolutie?quote:
Nu snap ik het!
God is een duitser!
jwz god kan alles maken uit niks, ook zichzelf.quote:
Generato spontano enzoo.quote:Op dinsdag 29 mei 2012 20:38 schreef dramatic het volgende:
[..]
jwz god kan alles maken uit niks, ook zichzelf.
BAM
.. dat had ik..quote:
en dat is fout
verkeerd gelezen zullen we maar zeggen
 Op
Op  Op
Op