SES School, Studie en Onderwijs
Wiskunde in de brugklas, Frans voor het examen of een studie Personeel en Arbeid? Moeilijke formulieren van DUO? Iets weten over studiefinanciering of studentenverenigingen? Dit is het forum voor leerkrachten, scholieren en studenten, van brugklas tot uni



Mja covariantiematrix ken ik wel, maar ik vroeg me af of er ook zoiets was als een soort methode/geval/etc was die direct een relatie beschrijft tussen 2 verschillende matricesquote:Op maandag 10 januari 2011 21:55 schreef GlowMouse het volgende:
[..]
Een functie is geen grootheid die afhankelijk van het toeval een bepaalde waarde aanneemt, dus die kun je niet bestuderen in de kansrekening. Vectoren van toevalsvariabelen zijn wel heel gangbaar, en dan krijg je een covariantiematrix. Zoek daar maar eens op


Je kunt een matrix vectoriserenquote:Op maandag 10 januari 2011 23:11 schreef koffiegast het volgende:
[..]
Mja covariantiematrix ken ik wel, maar ik vroeg me af of er ook zoiets was als een soort methode/geval/etc was die direct een relatie beschrijft tussen 2 verschillende matrices
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Ik kom toch nog terug op dat ding van gisteren:
vraag 1 a
Waarom is Cy eigenlijk nul? (of Cj) x y z = i j k
vraag 1 a
Waarom is Cy eigenlijk nul? (of Cj) x y z = i j k
Blues ain't nothing but a good man feeling bad...


Je moet de integraal van 0 t/m t nemen, en dan zie je ook dat je dt beter iets van dx kan zijn omdat je anders twee t's hebt. Daarna kun je r(t) wel juist bepalen want dat gaat nu fout. De c_x/y/z vallen dan uiteraard allemaal weg.
Je wilt dat r(0) is zoals in het plaatje, en dat doe je door r(t) = r(0) + die integraal te pakken.
Je wilt dat r(0) is zoals in het plaatje, en dat doe je door r(t) = r(0) + die integraal te pakken.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Thenk yoe, ik snap trouwens nog steeds niet wanneer je nou radian of degrees gebruikt op je GR. Ik probeer ze gewoon allebei en dan het logisch antwoord neem ik v_v
Blues ain't nothing but a good man feeling bad...


Altijd radialen, tenzij het duidelijk over graden gaat (opgemeten met een geodriehoek ofzo).
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


In mijn boek staat de volgende vuistregel:
Bij toevoeren van warmte verschuift een evenwicht naar de endotherme kant. Dat is de kans met het grootste aantal deeltjes.
Dit vetgedrukte is mij niet duidelijk.
Stel we hebben:
N2 + O2 <> 2NO
De vorming van NO is endotherm. Dus bij een temperatuurstijging verschuift het evenwicht naar NO, maar waarom is deze kant de kant met het grootste aantal deeltjes??
Bij toevoeren van warmte verschuift een evenwicht naar de endotherme kant. Dat is de kans met het grootste aantal deeltjes.
Dit vetgedrukte is mij niet duidelijk.
Stel we hebben:
N2 + O2 <> 2NO
De vorming van NO is endotherm. Dus bij een temperatuurstijging verschuift het evenwicht naar NO, maar waarom is deze kant de kant met het grootste aantal deeltjes??


Links en rechts staan twee deeltjes, dus de vuistregel biedt hier geen uitkomst.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Ik denk dat je het als volgt kunt verklaren: stel je hebt een molecuul A en een molecuul B die door zich met elkaar te verbinden het molecuul AB vormen. Tenzij A en B uitzonderlijk stabiele moleculen zijn, zal AB op een lager energieniveau zitten dan A en B, omdat er energie vrijkomt bij de vorming van de binding tussen A en B (ΔH < 0). Als het energieverschil klein is en de reactie niet totaal afloopt, zul je een evenwicht krijgen: A + B <-> AB.quote:Op woensdag 12 januari 2011 12:36 schreef Warren het volgende:
In mijn boek staat de volgende vuistregel:
Bij toevoeren van warmte verschuift een evenwicht naar de endotherme kant. Dat is de kanst met het grootste aantal deeltjes.
Dit vetgedrukte is mij niet duidelijk.
Stel we hebben:
N2 + O2 <> 2NO
De vorming van NO is endotherm. Dus bij een temperatuurstijging verschuift het evenwicht naar NO, maar waarom is deze kant de kant met het grootste aantal deeltjes??
Op het moment dat er warmte toegevoerd wordt, komt er energie beschikbaar om de binding in AB te breken en dus het verschil tussen de energieniveaus te overbruggen. Toevoeren van energie zorgt er dus voor dat het evenwicht verschuift naar de gedissocieerde kant, A en B.


Klein vraagje, over iets van mechanica.
Je hebt de totale versnelling die je bijv kan ontbinden in een tangentiale en normale versnelling.
Als de tangentiale snelheid nul is. Is de tangentiale versnelling dan per defenitie nul?
Je hebt de totale versnelling die je bijv kan ontbinden in een tangentiale en normale versnelling.
Als de tangentiale snelheid nul is. Is de tangentiale versnelling dan per defenitie nul?
Blues ain't nothing but a good man feeling bad...


Nee, hij kan eerst negatief zijn en daarna positief worden.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Lyolyrc, bedankt.. ik doelde meer op waarom er een endotherme kant kan zijn terwijl het aantal deeltjes links en rechts gelijk is. Maar zoals Glowmouse zegt, biedt zo'n vuistregel dus niet altijd uitkomst.
Ik heb nog een vraag:
Men lost 2,0 mol ammoniumchloride in water op tot 1,0 Liter.
Vraag: Hoeveel liter ammoniakgas van p=p0 en T= 298K moet men in deze oplossing inleiden om pH op 9,2 te brengen?
Ik heb een andere redenering en ik kom niet op het juiste anwtwoord.
NH4 + H2O --> NH3- + H3O+
Kz = [NH3-] [H3O+] / [NH4]
Kz = 5,6 x 10-10
Ik bereken eerst hoeveel H30+ er zit.
x2/2,0 = 5,6 x 10-10
x = h30+ = 4,73*10^-5.
De pH moet naar 9,2 dus de [H30+] moet omlaag van 4,73*10^-5 naar 6,31*10^-10... klopt dit? hoe kom ik er achter hoeveel ammoniak ik dan nodig heb??
Ik heb nog een vraag:
Men lost 2,0 mol ammoniumchloride in water op tot 1,0 Liter.
Vraag: Hoeveel liter ammoniakgas van p=p0 en T= 298K moet men in deze oplossing inleiden om pH op 9,2 te brengen?
Ik heb een andere redenering en ik kom niet op het juiste anwtwoord.
NH4 + H2O --> NH3- + H3O+
Kz = [NH3-] [H3O+] / [NH4]
Kz = 5,6 x 10-10
Ik bereken eerst hoeveel H30+ er zit.
x2/2,0 = 5,6 x 10-10
x = h30+ = 4,73*10^-5.
De pH moet naar 9,2 dus de [H30+] moet omlaag van 4,73*10^-5 naar 6,31*10^-10... klopt dit? hoe kom ik er achter hoeveel ammoniak ik dan nodig heb??


Ik had de vraag iets anders opgevat, vandaar het antwoord dat ik heb gegeven. Door je af te vragen waarom er een endotherme kant kan zijn als er links en rechts evenveel deeltjes zijn, verwissel je regel en vuistregel. Dat bij warmte toevoeren het evenwicht naar de endotherme kant verschuift is een feit. Dat volgt immers uit de wetten van de thermodynamica. Dat er aan de endotherme kant meestal meer deeltjes staan, dat is de vuistregel.quote:Op vrijdag 14 januari 2011 13:09 schreef Warren het volgende:
Lyolyrc, bedankt.. ik doelde meer op waarom er een endotherme kant kan zijn terwijl het aantal deeltjes links en rechts gelijk is. Maar zoals Glowmouse zegt, biedt zo'n vuistregel dus niet altijd uitkomst.
Dit klopt niet. Ammonium is NH4+, niet NH4. Bij het afstaan van een proton (H+) onstaat er NH3, dat is ammoniak. NH3- bestaat niet eens, want dat zou betekenen dat het stikstofatoom 9 elektronen om zich heen heeft, wat in strijd is met de octetregel.quote:Ik heb nog een vraag:
Men lost 2,0 mol ammoniumchloride in water op tot 1,0 Liter.
Vraag: Hoeveel liter ammoniakgas van p=p0 en T= 298K moet men in deze oplossing inleiden om pH op 9,2 te brengen?
Ik heb een andere redenering en ik kom niet op het juiste anwtwoord.
NH4 + H2O --> NH3- + H3O+
Kz = [NH3-] [H3O+] / [NH4]
De juiste reactievergelijking wordt dus:
NH4+ + H2O <- -> NH3 + H3O+
Omdat NH4+ een zwakke base is, ligt het evenwicht niet totaal naar rechts. Verderop zal ik nog laten zien waar het evenwicht ligt.
De evenwichtsvoorwaarde wordt dan:
Kz = [NH3]*[H3O+] / [NH4+]
Je methode van berekenen klopt, maar de uitkomst niet. Je moet inderdaad stellen dat er x mol NH3 en ook x mol H3O+ is gevormd en dat er nog 2 - x mol NH4+ over is. Als we dan even aannemen dat x klein is (dat betekent dat het evenwicht sterk naar links ligt), dan heb je:quote:Kz = 5,6 x 10-10
Ik bereken eerst hoeveel H30+ er zit.
x2/2,0 = 5,6 x 10-10
x = h30+ = 4,73*10^-5.
x2/2,0 = 5,6 * 10-10
x = √(2,0 * 5,6 * 10-10) = 3,3 * 10-5
Hieruit volgt dat x inderdaad erg klein is, eigenlijk verwaarloosbaar klein. Ammonium dissocieert dus nagenoeg niet in water!
Nee. Uit de evenwichtsvoorwaarde volgt:quote:De pH moet naar 9,2 dus de [H30+] moet omlaag van 4,73*10^-5 naar 6,31*10^-10... klopt dit? hoe kom ik er achter hoeveel ammoniak ik dan nodig heb??
pKz = pH - log([NH3]/[NH4+])
pH - pKz = log([NH3]/[NH4+])
10(pH - pKz) = [NH3]/[NH4+]
Invullen van de gewenste pH (9,2) en pKz (-log(5,6 * 10-10)) geeft:
[NH3]/[NH4+] = 0,89
Met andere woorden, [NH3] moet 0,89 * 2,0 = 1,78 M worden. Het kleine beetje NH3 dat er gevormd wordt bij oplossen van de ammoniumchloride is uiteraard verwaarloosbaar.
Het molair volume is 24,5 dm3/mol onder gegeven omstandigheden. Dat betekent dat er 24,5 * 1,78 = 43,6 dm3 NH3 nodig is.
[ Bericht 0% gewijzigd door lyolyrc op 14-01-2011 17:45:44 ]


Bedankt voor deze uitleg. Ik heb als een kip zonder kop de reactievergelijking en evenwichtsvoorwaarde gekopieerd uit een andere topic waar iemand met hetzelfde probleem kwam.. maar ik heb niet opgemerkt dat die niet klopte. Excuses voor het bezorgen van extra werk.
Het is nu veel helderder.
- Ik vond het ten eerste raar dat men voor [NH4+] 2,0 mol/L nam.. maar aangezien het een zwakke zuur is, is het wel logisch want maar een klein gedeelte gaat over in H30+ ionen.
- Ik vond het ook raar dat al het NH3 afkomstig zou zijn van het ammoniakgas, maar aangezien x verwaarloosbaar klein is, lijkt het nu wel logisch.
- In feite laat deze berekening (x2/2,0 = 5,6 * 10-10
x = (2,0 * 5,6 * 10-10) = 3,3 * 10-5) alleen zien dat x verwaarloosbaar klein is en met dit gegeven doe je niks voor het eindantwoord.
Het is nu veel helderder.
- Ik vond het ten eerste raar dat men voor [NH4+] 2,0 mol/L nam.. maar aangezien het een zwakke zuur is, is het wel logisch want maar een klein gedeelte gaat over in H30+ ionen.
- Ik vond het ook raar dat al het NH3 afkomstig zou zijn van het ammoniakgas, maar aangezien x verwaarloosbaar klein is, lijkt het nu wel logisch.
- In feite laat deze berekening (x2/2,0 = 5,6 * 10-10
x = (2,0 * 5,6 * 10-10) = 3,3 * 10-5) alleen zien dat x verwaarloosbaar klein is en met dit gegeven doe je niks voor het eindantwoord.


Maakt niet uit. De volgende die op iets dergelijks googlet, vindt dan ook deze uitleg waar het wel goed staat.quote:Op vrijdag 14 januari 2011 23:29 schreef Warren het volgende:
Bedankt voor deze uitleg. Ik heb als een kip zonder kop de reactievergelijking en evenwichtsvoorwaarde gekopieerd uit een andere topic waar iemand met hetzelfde probleem kwam.. maar ik heb niet opgemerkt dat die niet klopte. Excuses voor het bezorgen van extra werk.
Het ligt inderdaad aan de heel beperkte dissociatie. Als je de fractie die wel omzet naar NH3 er afhaalt, dan heb je 1,9999665 mol/l, wat we natuurlijk gewoon afronden op 2,0 M.quote:Het is nu veel helderder.
- Ik vond het ten eerste raar dat men voor [NH4+] 2,0 mol/L nam.. maar aangezien het een zwakke zuur is, is het wel logisch want maar een klein gedeelte gaat over in H30+ ionen.
Als x veel groter was geweest, had je die fractie uiteraard in mindering moeten brengen op de benodigde hoeveelheid NH3 (g).quote:- Ik vond het ook raar dat al het NH3 afkomstig zou zijn van het ammoniakgas, maar aangezien x verwaarloosbaar klein is, lijkt het nu wel logisch.
Deze berekening heb ik gedaan met de aanname dat x te verwaarlozen is. Als uit de berekening was gevolgd dat x een substantiële fractie was geweest van 2,0 M, dan had ik de berekening moeten herhalen met de abc-formule. En die fractie had ik dan ook verrekend met de 1,78 M NH3.quote:- In feite laat deze berekening (x2/2,0 = 5,6 * 10-10
x = (2,0 * 5,6 * 10-10) = 3,3 * 10-5) alleen zien dat x verwaarloosbaar klein is en met dit gegeven doe je niks voor het eindantwoord.


lyolyrc, je bent een held voor het helder uitleggen van de materie 
Ik heb nog een kort vraagje n.a.v. een vraag uit een Scheikunde 1,2 examen.
Om het even kort te houden: in de vraag komt deze zin voor:
"Bij het blok legering wordt het aluminium omgezet tot aluminiumhydroxide"
Nou moet je dus hiervan een halfreactie nemen. In het antw. model staat: Al + 3 OH- --> Al(OH)3 + 3e-. Maar deze komt in binas niet voor. In binas staat wel: Al + 4OH- --> Al(OH)4- + 3e-.
Hoe zit dit nu? Ik ben een beetje in de war... welke vergelijking klopt dan?
Ik heb nog een kort vraagje n.a.v. een vraag uit een Scheikunde 1,2 examen.
Om het even kort te houden: in de vraag komt deze zin voor:
"Bij het blok legering wordt het aluminium omgezet tot aluminiumhydroxide"
Nou moet je dus hiervan een halfreactie nemen. In het antw. model staat: Al + 3 OH- --> Al(OH)3 + 3e-. Maar deze komt in binas niet voor. In binas staat wel: Al + 4OH- --> Al(OH)4- + 3e-.
Hoe zit dit nu? Ik ben een beetje in de war... welke vergelijking klopt dan?


Beide reactievergelijkingen zijn op zich correct. Zie ook deze tabel in wikipedia bij -2.31 en -2.33 V. Maar aluminiumhydroxide is Al(OH)3. Al(OH)4- is een andere stof die tetrahydroxyaluminaat heet.quote:Op zondag 16 januari 2011 23:44 schreef Warren het volgende:
lyolyrc, je bent een held voor het helder uitleggen van de materie
Ik heb nog een kort vraagje n.a.v. een vraag uit een Scheikunde 1,2 examen.
Om het even kort te houden: in de vraag komt deze zin voor:
"Bij het blok legering wordt het aluminium omgezet tot aluminiumhydroxide"
Nou moet je dus hiervan een halfreactie nemen. In het antw. model staat: Al + 3 OH- --> Al(OH)3 + 3e-. Maar deze komt in binas niet voor. In binas staat wel: Al + 4OH- --> Al(OH)4- + 3e-.
Hoe zit dit nu? Ik ben een beetje in de war... welke vergelijking klopt dan?
Maar je moet voor een redoxreactie 2 halfreacties hebben. De eerste is gemakkelijk, namelijk de oxidatie van aluminium: Al (s) -> Al3+ + 3 e-
Omdat ik het gevoel had dat er nog wat nuttige en noodzakelijke extra informatie in het examen stond, heb ik het hele examen maar even opgezocht.
In het examen staat:
Deze halfreactie staat ook in Binas: O2 (g) + 2 H2O (l) + 4 e- -> 4 OH-quote:Bij het gaasje reageert zuurstof uit de lucht met water onder vorming van hydroxide-ionen.
Dan hoef je alleen nog maar de elektronen in balans te brengen door 4x de halfreactie van aluminium op te tellen bij 3x de halfreactie van zuurstof en water.
Al (s) -> Al3+ + 3 e- |4x|
O2 (g) + 2 H2O (l) + 4 e- -> 4 OH- |3x|
-------------------------------------------------------------------------------------- +
Je zou dan dit verwachten:
4 Al (s) + 3 O2 (g) + 6 H2O (l) -> 4 Al3+ + 12 OH-
Maar als je even een stukje terug bladert in Binas, staat er een tabel met de oplosbaarheid in water van verschillende zouten (bij mij tabel 45a). Je vindt dan dat aluminiumhydroxide slecht oplosbaar is. Met andere woorden hydroxide en aluminum vormen een neerslag, dus de totaalreactie wordt:
4 Al (s) + 3 O2 (g) + 6 H2O (l) -> 4 Al(OH)3 (s)


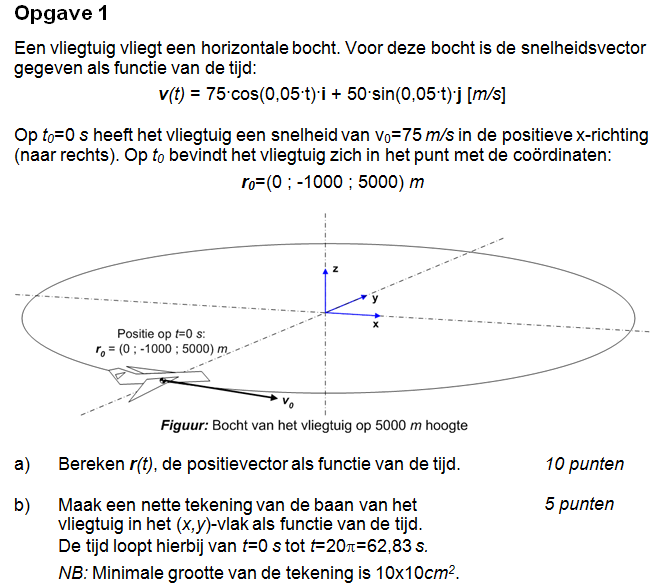
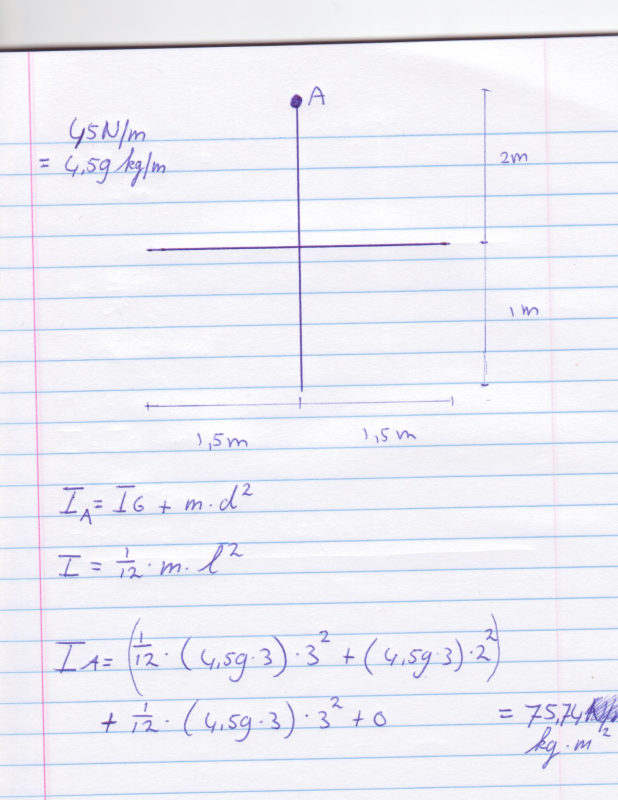
Ik was net bezig met het traagheidsmoment van het stelsel om as A van het stelsel van staven hieronder te bepalen. Ik heb er geen antwoorden bij, dus ik vroeg me af of ik deze wel goed heb aangepakt?
Eerst de algemenen formule daarna de formule voor een staaf. Eerst heb ik de horizontale staaf gedaan en daarna gewoon de verticale er bij opgeteld. Klopt dit wel?
Eerst de algemenen formule daarna de formule voor een staaf. Eerst heb ik de horizontale staaf gedaan en daarna gewoon de verticale er bij opgeteld. Klopt dit wel?
Blues ain't nothing but a good man feeling bad...


Ik zie niet echt goed wat het precies is, is het een soort + profiel ofzo?quote:Op woensdag 19 januari 2011 14:35 schreef GoodGawd het volgende:
Ik was net bezig met het traagheidsmoment van het stelsel om as A van het stelsel van staven hieronder te bepalen. Ik heb er geen antwoorden bij, dus ik vroeg me af of ik deze wel goed heb aangepakt?
Eerst de algemenen formule daarna de formule voor een staaf. Eerst heb ik de horizontale staaf gedaan en daarna gewoon de verticale er bij opgeteld. Klopt dit wel?
[ afbeelding ]


wie kan mij uitleggen, hoe de formule van de halveringsdikte precies werkt?
in het boek staat de formule I (n) = I (0) × (1/2)n
I(n) = de intensiteit na n halveringsdiktes (in W/m²)
bij dikte x geldt x= n × d1/2 (met x en d1/2 in gelijke eenheden).
ik snap niet precies wat ik hiermee moet doen, wat ik waar in moet vullen?
kan iemand dit verduidelijken voor mij?
alvast bedankt
in het boek staat de formule I (n) = I (0) × (1/2)n
I(n) = de intensiteit na n halveringsdiktes (in W/m²)
bij dikte x geldt x= n × d1/2 (met x en d1/2 in gelijke eenheden).
ik snap niet precies wat ik hiermee moet doen, wat ik waar in moet vullen?
kan iemand dit verduidelijken voor mij?
alvast bedankt


Ja het, zie het als een ijzeren constructie van een kruis, uit 1 stuk metaal.quote:Op vrijdag 21 januari 2011 14:25 schreef vaasinbloem het volgende:
[..]
Ik zie niet echt goed wat het precies is, is het een soort + profiel ofzo?Bij het elkaar optellen, heb je dan geen probleem met de overlapping?
Blues ain't nothing but a good man feeling bad...


Een kruis met een rotatiepunt aan de top toch? Die A? Als ik het even snel bekijk heb je gebruikt gemaakt van (en dan maal 2):quote:Op zondag 23 januari 2011 12:18 schreef GoodGawd het volgende:
[..]
Ja het, zie het als een ijzeren constructie van een kruis, uit 1 stuk metaal.
?
http://homepages.which.ne(...)s/MOI/MOIproofs.html
Zo ja, dat is een formule als de rotatie in het middelpunt zit en niet aan de top.
Volgens mij moet je deze gebruiken:
Ik zou eerst het hele grid maken en telkens rekenen en dan telkens kleine stukjes eruit halen. De rotatiepunt moet hetzelfde blijven (boven 2).
1 2 3
4 5 6
7 8 9
Dus eerst 1-9, dan 258, 1-6, 1-3, 2.
2
5
8
1 2 3
4 5 6
1 2 3
2
Kan iemand dit bevestigen dat het klopt? En of het makkelijker kan, vind het nogal omslachtig namelijk. Is er niet op internet een kant en klare formule te vinden?


Ik neem aan dat het hier gaat over straling, die gedeeltelijk doorgelaten wordt door een materiaal? Dat materiaal heeft dan een halveringsdikte, een maat voor hoeveel straling er wordt doorgelaten. Als je straling door een materiaal stuurt, is de intensiteit van die straling na één halveringsdikte nog maar de helft van de oorspronkelijke intensiteit. Voor de intensiteit na n halveringsdiktes geldt dan je eerste formule. I (n) is die gezochte intensiteit, I(0) is de oorspronkelijke intensiteit, en bij n vul je het aantal halveringsdiktes dat je materiaal dik is in.quote:Op zondag 23 januari 2011 12:00 schreef snellehenk het volgende:
wie kan mij uitleggen, hoe de formule van de halveringsdikte precies werkt?
in het boek staat de formule I (n) = I (0) × (1/2)n
I(n) = de intensiteit na n halveringsdiktes (in W/m²)
bij dikte x geldt x= n × d1/2 (met x en d1/2 in gelijke eenheden).
ik snap niet precies wat ik hiermee moet doen, wat ik waar in moet vullen?
kan iemand dit verduidelijken voor mij?
alvast bedankt
De tweede formule geeft aan hoe je n kan berekenen, n=x/d1/2, met x de dikte van je materiaal, en d1/2 de halveringsdikte van je materiaal. Dat x en d1/2 gelijke eenheden moeten hebben betekent dat je niet de ene in meters mag zetten als de andere in centimeters staat, de eenheden moeten gelijk zijn.
Ik hoop dat het wat duidelijker is nu
The biggest argument against democracy is a five minute discussion with the average voter.


Ja het ging idd over de straling, bedankt (Y)quote:Op zondag 23 januari 2011 15:38 schreef M.rak het volgende:
[..]
Ik neem aan dat het hier gaat over straling, die gedeeltelijk doorgelaten wordt door een materiaal? Dat materiaal heeft dan een halveringsdikte, een maat voor hoeveel straling er wordt doorgelaten. Als je straling door een materiaal stuurt, is de intensiteit van die straling na één halveringsdikte nog maar de helft van de oorspronkelijke intensiteit. Voor de intensiteit na n halveringsdiktes geldt dan je eerste formule. I (n) is die gezochte intensiteit, I(0) is de oorspronkelijke intensiteit, en bij n vul je het aantal halveringsdiktes dat je materiaal dik is in.
De tweede formule geeft aan hoe je n kan berekenen, n=x/d1/2, met x de dikte van je materiaal, en d1/2 de halveringsdikte van je materiaal. Dat x en d1/2 gelijke eenheden moeten hebben betekent dat je niet de ene in meters mag zetten als de andere in centimeters staat, de eenheden moeten gelijk zijn.
Ik hoop dat het wat duidelijker is nu.
Het begint al duidelijker te worden, maar zou je misschien nog iets duidelijker voor me kunnen maken, door een voorbeeld te geven?
alvast bedankt

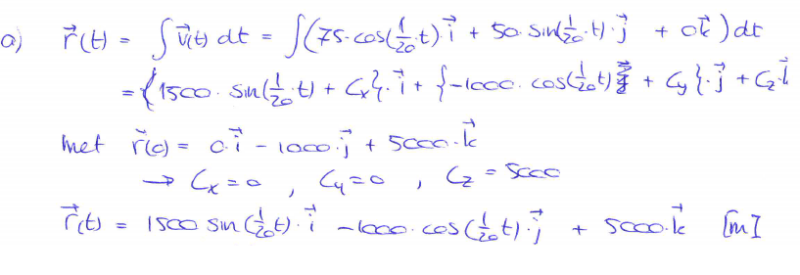

 ?
?