SES School, Studie en Onderwijs
Wiskunde in de brugklas, Frans voor het examen of een studie Personeel en Arbeid? Moeilijke formulieren van DUO? Iets weten over studiefinanciering of studentenverenigingen? Dit is het forum voor leerkrachten, scholieren en studenten, van brugklas tot uni



Ik heb een opgave waarin gevraagd wordt om een polymeer te maken van 2 stoffen. Echter, de benzeenringen in de polymeer hebben volgens het antwoordmodel de aansluitende bindingen op een andere plek zitten dan bij de originele verbinding. Is dit een fout in het boek? Zo nee, waarom is dit zo?


Ja, dat is fout in het boek. Ik heb zelf wel eens polyesters gemaakt met tereftaalzuur (1,4-benzeendicarbonzuur) en isoftaalzuur (1,3-benzeendicarbonzuur). Het maakt flink uit voor de fysische eigenschappen van het polymeer welke van de ftaalzuurisomeren je kiest. Dat geldt ongetwijfeld ook voor benzeendiamines.quote:Op maandag 19 mei 2014 15:51 schreef m.w. het volgende:
Ik heb een opgave waarin gevraagd wordt om een polymeer te maken van 2 stoffen. Echter, de benzeenringen in de polymeer hebben volgens het antwoordmodel de aansluitende bindingen op een andere plek zitten dan bij de originele verbinding. Is dit een fout in het boek? Zo nee, waarom is dit zo?
[ afbeelding ]


Hartelijk bedankt voor het antwoord! Er staan wel meer fouten in maar daar ga ik jullie niet mee pesten. Zou eigenlijk niet mogen voor een toelatingsexamen van de UU...


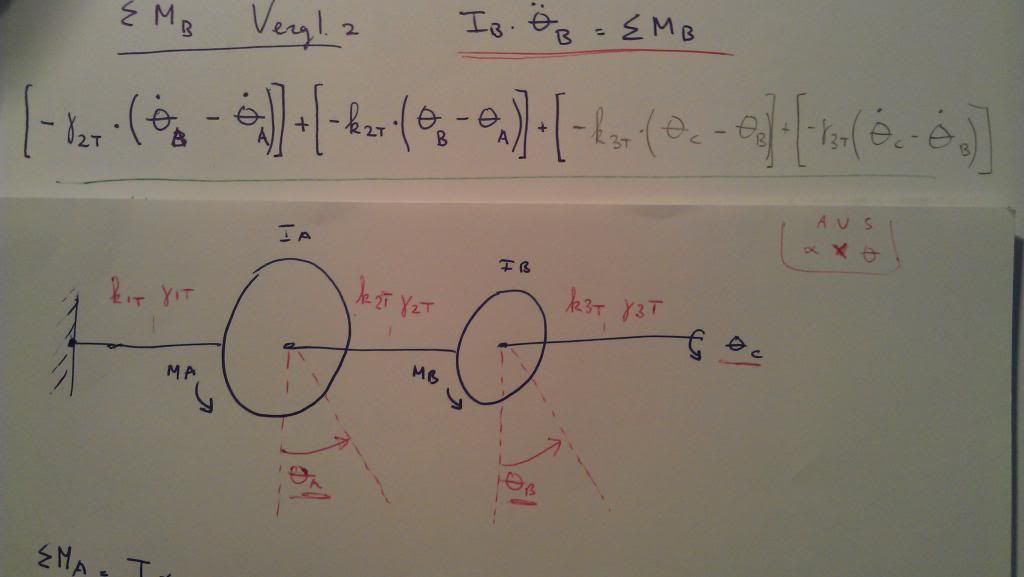
Hallo ik ben bezig met het opstellen van een paar differentiaal verglijkingen om een systeem te modelleren. Ben al een eind op weg maar ik twijfel nog over een klein stukje. Het gaat om het volgende:
Twee rotor bladen die aan een as zitten die rond draait. Links zit de as aan de muur vast en kan niet draaien. Er komt dus torsie in de stang, de gamma van demping en k van vering zijn eigenschappen van de stang.
Mijn aanpak is dat ik eerst momenten vergelijking opstel van rotor A. (Dat is gelukt)
Hier:
Twee rotor bladen die aan een as zitten die rond draait. Links zit de as aan de muur vast en kan niet draaien. Er komt dus torsie in de stang, de gamma van demping en k van vering zijn eigenschappen van de stang.
Mijn aanpak is dat ik eerst momenten vergelijking opstel van rotor A. (Dat is gelukt)
Hier:
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Vervolgens van rotor B. Alleen hier ben ik niet geheel zeker van mij zaak:
Het deel geschreven met pen is goed volgens mij. Het deel met potlood twijfel ik over. Rechts is dus een input, de stang draait daar met bepaalde rotatie. Ik neem daar ook het verschil tussen verdraaiing van rotor B en de verdraaiing van de input, maar moet dat wel.. Het gaat er nu dus alleen nog even om hoe ik die krachten rechts van rotor B ga vatten.
Is it zo simpel dat als ik gewoon verdraaiing van C uit die formule laat t klopt...hmm
Iemand?
[ Bericht 3% gewijzigd door GoodGawd op 22-05-2014 16:32:46 ]Blues ain't nothing but a good man feeling bad...


Ik heb 2 vragen waarvan ik niet weet hoe ik ze moet uitrekenen.
Vraag 1: concentratie oplossing is 13.3M. Hoeveel ml moet verdund worden tot 1 litet om een oplossing van 0.10 M te krijgen?
Vraag 2: De dichtheid van geconcentreerd zoutzuur dat 37% hcl bevat is 1.9 g/ml. Welk volume van deze oplossing moet verdund worden tot 500 ml om een oplossing van 250 mM HCL te krijgen?
Hoe reken je dit uit? Of kan iemand de berekeningen maken en alle gezette stappen plaatsen?
Vraag 1: concentratie oplossing is 13.3M. Hoeveel ml moet verdund worden tot 1 litet om een oplossing van 0.10 M te krijgen?
Vraag 2: De dichtheid van geconcentreerd zoutzuur dat 37% hcl bevat is 1.9 g/ml. Welk volume van deze oplossing moet verdund worden tot 500 ml om een oplossing van 250 mM HCL te krijgen?
Hoe reken je dit uit? Of kan iemand de berekeningen maken en alle gezette stappen plaatsen?


Ik neem aan dat M staat voor molair en niet molail.quote:Op vrijdag 23 mei 2014 23:14 schreef Aladeen het volgende:
Ik heb 2 vragen waarvan ik niet weet hoe ik ze moet uitrekenen.
Vraag 1: concentratie oplossing is 13.3M. Hoeveel ml moet verdund worden tot 1 litet om een oplossing van 0.10 M te krijgen?
Vraag 2: De dichtheid van geconcentreerd zoutzuur dat 37% hcl bevat is 1.9 g/ml. Welk volume van deze oplossing moet verdund worden tot 500 ml om een oplossing van 250 mM HCL te krijgen?
Hoe reken je dit uit? Of kan iemand de berekeningen maken en alle gezette stappen plaatsen?
Vraag 1:
De hoeveelheid stof voor en na elke verdunning is hetzelfde dus n1=n2 (a)
Concentratie wordt gedefinieerd als de hoeveelheid opgeloste stof in mol per volume-eenheid oplossing C = n/V (b)
uit (a) en (b) volgt dan:
C1.V1=C2.V2 (=de verdunningsregel)
In opgave 1 wordt gezocht naar V1
V1=V2.C2/C1
Vraag 2
Eerst massaprocent(= m1/m2) omzetten naar concentratie(=n/V)
Zet m1 om in hoeveelheid stof: n = m1/M (c)
Zet m2 om in volume: m2/ρ = V (d)
We substitueren (c) en (d) in C=n/V
C=(m1/M) / (m2/ρ)
C=m%.ρ/M
Nu je C1 weet kun je weer de verdunningsregel toepassen om V1 te berekenen.
Hoop dat het nu duidelijk is.


Kan iemand mij helpen met differentieren:
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


quote:Op zondag 25 mei 2014 04:01 schreef whatevr het volgende:
Kan iemand mij helpen met differentieren:Dat kan je niet bepalen zonder meer informatie.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.
SES / [Bèta wiskunde] Huiswerk- en vragentopic.
Waarschijnlijk willen ze dat de functie differentieerbaar is en vanaf x = 1 een rechte lijn is.
Schrijf even g(x) voor de rechte lijn, x > 1.
Dan moet dus gelden (continuiteit)
f(1) = 3 + 7 + 2 = 12 = g(1)
en
f ' (x) = 6x + 7
Er moet gelden (differentieerbaarheid)
f ' (1) = 6 + 7 = 13 = g ' (1)
Met g(1) = 12 en g'(1) = 13 en gegeven dat g een rechte lijn is volgt inderdaad g(x) = 13x - 1
[ Bericht 17% gewijzigd door Anoonumos op 25-05-2014 10:48:34 ]


Thxquote:Op zaterdag 24 mei 2014 23:59 schreef Supertolll het volgende:
[..]
Ik neem aan dat M staat voor molair en niet molail.
Vraag 1:
De hoeveelheid stof voor en na elke verdunning is hetzelfde dus n1=n2 (a)
Concentratie wordt gedefinieerd als de hoeveelheid opgeloste stof in mol per volume-eenheid oplossing C = n/V (b)
uit (a) en (b) volgt dan:
C1.V1=C2.V2 (=de verdunningsregel)
In opgave 1 wordt gezocht naar V1
V1=V2.C2/C1
Vraag 2
Eerst massaprocent(= m1/m2) omzetten naar concentratie(=n/V)
Zet m1 om in hoeveelheid stof: n = m1/M (c)
Zet m2 om in volume: m2/ρ = V (d)
We substitueren (c) en (d) in C=n/V
C=(m1/M) / (m2/ρ)
C=m%.ρ/M
Nu je C1 weet kun je weer de verdunningsregel toepassen om V1 te berekenen.
Hoop dat het nu duidelijk is.


Aha, Dank voor uw uitlegquote:Op zondag 25 mei 2014 10:42 schreef Anoonumos het volgende:
[..]
Dat kan je niet bepalen zonder meer informatie.
SES / [Bèta wiskunde] Huiswerk- en vragentopic.
Waarschijnlijk willen ze dat de functie differentieerbaar is en vanaf x = 1 een rechte lijn is.
Schrijf even g(x) voor de rechte lijn, x > 1.
Dan moet dus gelden (continuiteit)
f(1) = 3 + 7 + 2 = 12 = g(1)
en
f ' (x) = 6x + 7
Er moet gelden (differentieerbaarheid)
f ' (1) = 6 + 7 = 13 = g ' (1)
Met g(1) = 12 en g'(1) = 13 en gegeven dat g een rechte lijn is volgt inderdaad g(x) = 13x - 1


Wil iemand mij aub, in een stappenplan uitleggen hoe ik de horizontale asymptoot van een hyperbolische functie moet bepalen??
Het is heel belangrijk en moet heel duidelijk en netjes in een stappenplan staan, want ik ben namelijk een beetje traag van begrip en dit moet ik leren voor een toets.
Alvast bedankt !
Het is heel belangrijk en moet heel duidelijk en netjes in een stappenplan staan, want ik ben namelijk een beetje traag van begrip en dit moet ik leren voor een toets.
Alvast bedankt !


Deze vraag moet je in het beta wiskunde topic stellen, hier. Geef ook een voorbeeld van het soort vraagstukken dat je geacht wordt op te lossen en laat zien wat je zelf al hebt gedaan en waarom het niet lukt.quote:Op vrijdag 30 mei 2014 01:33 schreef hanskarel het volgende:
Wil iemand mij aub, in een stappenplan uitleggen hoe ik de horizontale asymptoot van een hyperbolische functie moet bepalen??
Het is heel belangrijk en moet heel duidelijk en netjes in een stappenplan staan, want ik ben namelijk een beetje traag van begrip en dit moet ik leren voor een toets.
Alvast bedankt !
Overigens vermoed ik dat je functies bedoelt waarvan de grafiek een hyperbool is. Een dergelijke functie mag je geen hyperbolische functie noemen, want dat is namelijk heel iets anders.


Hoyhoy.
Ben bezig met GMAT voorbereiding en heb een vraag over de uitleg bij één van de testvragen.
If x is a positive integer, what is the remainder when 7^12x+3 + 3 is divided by 5?
A. 0
B. 1
C. 2
D. 3
E. 4
Het patroon van de macht van 7 ken ik, een cycle van 4 (met als units digit 7, 9, 3 of 1).
Echter wordt bij de uitleg aangegeven dat 12x+3 een multiple van 4 moet zijn en daar vat ik het even niet meer:
Met die laatste informatie wil ik het begrijpen, maar als je 12X als 12X (en dus niet 4*3X) beschouwt zou het toch ook (stel x=3) (12*3)+3 kunnen zijn, dan krijgt de macht een units digit van 9 en daarmee de uitkomst van 7^12x+3 een units digit 7 (want gezien de cycle is de units digit van 7^9 = 7^1).
Ik heb het idee dat ik iets compleet over het hoofd zie, maar ik vraag mij af wat..
Ben bezig met GMAT voorbereiding en heb een vraag over de uitleg bij één van de testvragen.
If x is a positive integer, what is the remainder when 7^12x+3 + 3 is divided by 5?
A. 0
B. 1
C. 2
D. 3
E. 4
Het patroon van de macht van 7 ken ik, een cycle van 4 (met als units digit 7, 9, 3 of 1).
Echter wordt bij de uitleg aangegeven dat 12x+3 een multiple van 4 moet zijn en daar vat ik het even niet meer:
Een uitleg op een andere website geeft aan: 12x+3=4*(3x)+3quote:12x is a multiple of 4 since x is an integer, so 7^12x would end in a 1, just like 7^4 or 7^8.
7^12x+3 would then correspond to 7^3 or 7^7 (multiple of 4 plus 3), and would therefore end in a 3.
Met die laatste informatie wil ik het begrijpen, maar als je 12X als 12X (en dus niet 4*3X) beschouwt zou het toch ook (stel x=3) (12*3)+3 kunnen zijn, dan krijgt de macht een units digit van 9 en daarmee de uitkomst van 7^12x+3 een units digit 7 (want gezien de cycle is de units digit van 7^9 = 7^1).
Ik heb het idee dat ik iets compleet over het hoofd zie, maar ik vraag mij af wat..


Er staat dat 12x een veelvoud van 4 is, niet dat 12x + 3 dat is.
En volgens mij is het niet voldoende om naar de unit digit van de macht te kijken (zoals jij bij 39 doet).
712x + 3 = 712x * 73
712x = (74)3x
eindigt op een 1.omdat 74 eindigt op een 1.
73 eindigt op een 3
Dus het product 712x * 73 eindigt op een 3.
En volgens mij is het niet voldoende om naar de unit digit van de macht te kijken (zoals jij bij 39 doet).
712x + 3 = 712x * 73
712x = (74)3x
eindigt op een 1.omdat 74 eindigt op een 1.
73 eindigt op een 3
Dus het product 712x * 73 eindigt op een 3.


O, ik zie het al ja. Het was helemaal niet de bedoeling om naar de unit digit te kijken bij 39, maar dat gebeurde uit een soort automatisme (bij een vraag als deze) toch.quote:Op zondag 8 juni 2014 15:33 schreef Anoonumos het volgende:
Er staat dat 12x een veelvoud van 4 is, niet dat 12x + 3 dat is.
En volgens mij is het niet voldoende om naar de unit digit van de macht te kijken (zoals jij bij 39 doet).
712x + 3 = 712x * 73
712x = (74)3x
eindigt op een 1.omdat 74 eindigt op een 1.
73 eindigt op een 3
Dus het product 712x * 73 eindigt op een 3.
Dan ben ik blij dat m'n berekeningen in principe goed zijn, alleen dat 39 (bij m'n voorbeeld) natuurlijk een remainder van 3 geeft en het dus gelijk staat aan 7^3.
Dank! Hopelijk is het weer een wake-up call, want dit soort simpele foutjes maak ik iets te vaak voor deze test.


Ik heb een vraagje, waarom geleidt een metaal elektriciteit? Want waarom geleidt bijvoorbeeld koolstof geen elektriciteit, maar een metaal wel?


Metalen bevatten vrije elektronen die dus vrij kunnen bewegen en zo voor geleiding van stroom kunnen zorgen.quote:Op zondag 8 juni 2014 23:42 schreef netchip het volgende:
Ik heb een vraagje, waarom geleidt een metaal elektriciteit? Want waarom geleidt bijvoorbeeld koolstof geen elektriciteit, maar een metaal wel?
Op woensdag 20 april 2011 23:38 schreef luckass het volgende:
bazen zijn alleen vindbaar voor de chicks.
bazen zijn alleen vindbaar voor de chicks.


Je vergist je een beetje. Koolstof geleidt ook electriciteit. Heb je wel eens een gewone zink-koolstof batterij opengemaakt?quote:Op zondag 8 juni 2014 23:42 schreef netchip het volgende:
Ik heb een vraagje, waarom geleidt een metaal elektriciteit? Want waarom geleidt bijvoorbeeld koolstof geen elektriciteit, maar een metaal wel?


Hebben ze 1 vrije elektron in hun buitenste schil? Of meer? Of maakt dat eigenlijk niet uit?quote:Op zondag 8 juni 2014 23:50 schreef yosander het volgende:
[..]
Metalen bevatten vrije elektronen die dus vrij kunnen bewegen en zo voor geleiding van stroom kunnen zorgen.
Verkeerde voorbeeld genomen danquote:Op maandag 9 juni 2014 00:03 schreef Riparius het volgende:
[..]
Je vergist je een beetje. Koolstof geleidt ook electriciteit. Heb je wel eens een gewone zink-koolstof batterij opengemaakt?


Onzin. Ik heb vroeger zoveel batterijen uit elkaar gehaald en ik heb er niets aan overgehouden. Dan bedoel ik natuurlijk geen batterijen die kwik of zo bevatten, maar de klassieke zink-koolstof batterij. Daar zit verder niet meer in dan bruinsteen en salmiak. Een leuk proefje was altijd om het koolstaafje en een stuk van het zinken omhulsel in een citroen te steken, dan kun je een lampje op de citroen laten branden. Ik heb ook wel zelf batterijen gemaakt door het koolstaafje en het zinken bekertje in een jampot te hangen met daarin een salmiakoplossing (kon je vroeger gewoon bij de drogist kopen).quote:Op maandag 9 juni 2014 11:29 schreef netchip het volgende:
Verkeerde voorbeeld genomen danIk heb nog nooit een batterij opengemaakt, schijnt ook niet erg gezond te zijn...


Ik wist al niet welk soort batterijen je bedoeldequote:Op maandag 9 juni 2014 13:26 schreef Riparius het volgende:
[..]
Onzin. Ik heb vroeger zoveel batterijen uit elkaar gehaald en ik heb er niets aan overgehouden. Dan bedoel ik natuurlijk geen batterijen die kwik of zo bevatten, maar de klassieke zink-koolstof batterij. Daar zit verder niet meer in dan bruinsteen en salmiak. Een leuk proefje was altijd om het koolstaafje en een stuk van het zinken omhulsel in een citroen te steken, dan kun je een lampje op de citroen laten branden. Ik heb ook wel zelf batterijen gemaakt door het koolstaafje en het zinken bekertje in een jampot te hangen met daarin een salmiakoplossing (kon je vroeger gewoon bij de drogist kopen).
Lijkt me een leuk experiment


Ja, ze zijn er nog steeds, maar je moet er wel naar zoeken. Hoe goedkoper hoe beter. Die grote 1,5 volt batterijen (type D of R20) bijvoorbeeld die (vroeger) in draagbare radio's en zaklantaarns werden gebruikt, en natuurlijk de platte 4,5 volt batterij, type 3R12 (zo eentje dus). Die was favoriet om uit elkaar te halen, want dan had je meteen drie cellen.quote:Op maandag 9 juni 2014 13:32 schreef netchip het volgende:
[..]
Ik wist al niet welk soort batterijen je bedoeldeWorden zink-koolstof batterijen tegenwoordig nog verkocht? Ik zie eigenlijk alleen batterijen liggen, waarvan ik weet dat ik die niet open moet maken (IKEA batterijen enzo).
Lijkt me een leuk experiment


In de generatie van de grootouders trad er zowel aan de zijde van de vader als aan de zijde van de moeder een ernstige recessieve ziekte op.
Ik heb in de afbeelding mijn redenatie neergezet. Klopt het? De kans dat vraagteken de ziekte zal hebben komt bij mijn berekeningen op 1/64.
Ik heb in de afbeelding mijn redenatie neergezet. Klopt het? De kans dat vraagteken de ziekte zal hebben komt bij mijn berekeningen op 1/64.


Hebben die grootouders niet 2/6 = 1/3 kans op het recessieve gen? Omdat je weet dat ze niet ziek zijn blijft R R, r R en R r over,
En in jouw geval: de 1/4 kans op het vraagteken is al de vermenigvuldigde kansen van zijn ouders (1/2 * 1/2) dus dan moet je niet ook nog 1/2 * 1/2 * 1/4 doen.
Ik zou zeggen
Kans dat een grootouder het recessieve gen heeft is 1/3.
Dus kans dat een ouder het recessieve gen heeft is 1/6.
Dus kans dat het kind twee recessieve genen heeft is 1/6 * 1/6 = 1/36.
En in jouw geval: de 1/4 kans op het vraagteken is al de vermenigvuldigde kansen van zijn ouders (1/2 * 1/2) dus dan moet je niet ook nog 1/2 * 1/2 * 1/4 doen.
Ik zou zeggen
Kans dat een grootouder het recessieve gen heeft is 1/3.
Dus kans dat een ouder het recessieve gen heeft is 1/6.
Dus kans dat het kind twee recessieve genen heeft is 1/6 * 1/6 = 1/36.
| Forum Opties | |
|---|---|
| Forumhop: | |
| Hop naar: | |