SES School, Studie en Onderwijs
Wiskunde in de brugklas, Frans voor het examen of een studie Personeel en Arbeid? Moeilijke formulieren van DUO? Iets weten over studiefinanciering of studentenverenigingen? Dit is het forum voor leerkrachten, scholieren en studenten, van brugklas tot uni



Waarom heet die eerste stof 3-chloor-1-buteen in plaats van 3-chloorbuteen?
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


zoek het begrip van configuratie is op;) bovendien, dubbele bindingen maken een molecuul minder beweeglijk...


Die dubbele binding van buteen kan toch aan de zijkant (1-) of op de middelste plek zitten (2-) ?quote:Op zondag 27 februari 2011 14:06 schreef GlowMouse het volgende:
Waarom heet die eerste stof 3-chloor-1-buteen in plaats van 3-chloorbuteen?
gr gr


Ok, maar wat ik niet snap is dat bij vraag a gevraagd wordt:quote:Op zondag 27 februari 2011 14:26 schreef kevintjuhh2 het volgende:
zoek het begrip van configuratie is op;) bovendien, dubbele bindingen maken een molecuul minder beweeglijk...
En bij vraag e heb je dezelfde stof..quote:Er zijn vier stereo-isomeren met de systematische naam: 4-chloor-2-penteen.
a. Leg uit waardoor er vier isomeren zijn.
Er is een dubbele binding die cis-trans isomerie veroorzaakt en er is een asymmetrisch Catoom
(C4).
b. Hoe worden in de naamgeving deze isomeren van elkaar onderscheiden ?
De vier isomeren zijn dus cis-D-, cis-L-, trans-D- en trans-L-4-chloor-2-penteen.
[ Bericht 5% gewijzigd door Warren op 27-02-2011 14:46:49 ]


Ik heb een oplossing van FeCl en een oplossing van KSCN, die voeg ik bij elkaar en er ontstaat een nieuw mengsel.
Vervolgens voeg ik AgNO3 - kristallen erbij, wat is de reactie die dan ontstaat?
Ik dacht iets met redox, maar kom er niet uit
Vervolgens voeg ik AgNO3 - kristallen erbij, wat is de reactie die dan ontstaat?
Ik dacht iets met redox, maar kom er niet uit


neerslag?quote:Op zondag 27 februari 2011 17:56 schreef marsPlanets het volgende:
Ik heb een oplossing van FeCl en een oplossing van KSCN, die voeg ik bij elkaar en er ontstaat een nieuw mengsel.
Vervolgens voeg ik AgNO3 - kristallen erbij, wat is de reactie die dan ontstaat?
Ik dacht iets met redox, maar kom er niet uit


Jouw analyse klopt gewoon, aangenomen dat zowel de L- als D-configuratie aanwezig is. De opgave vertelt echter niet welke isomeren van 2,4-dichloorpentaan aanwezig zijn en daarom is het antwoord van de opgave ook niet zo specifiek. Overigens zou ik zelf liever R- en S-nomenclatuur gebruiken, omdat daarmee de absolute configuratie wordt vastgelegd.quote:Op zondag 27 februari 2011 14:38 schreef Warren het volgende:
[..]
Ok, maar wat ik niet snap is dat bij vraag a gevraagd wordt:
[..]
En bij vraag e heb je dezelfde stof..
Ben benieuwd waar jij FeCl vandaan wil gaan halen.quote:Op zondag 27 februari 2011 17:56 schreef marsPlanets het volgende:
Ik heb een oplossing van FeCl en een oplossing van KSCN, die voeg ik bij elkaar en er ontstaat een nieuw mengsel.
Vervolgens voeg ik AgNO3 - kristallen erbij, wat is de reactie die dan ontstaat?
Ik dacht iets met redox, maar kom er niet uit
En dat is inderdaad het antwoord. En welk neerslag? Hint: fotografie.quote:


Bedankt! Maar weet jij misschien wat ze bedoelen met het vetgedruktequote:Op maandag 28 februari 2011 15:18 schreef lyolyrc het volgende:
[..]
Jouw analyse klopt gewoon, aangenomen dat zowel de L- als D-configuratie aanwezig is. De opgave vertelt echter niet welke isomeren van 2,4-dichloorpentaan aanwezig zijn en daarom is het antwoord van de opgave ook niet zo specifiek. Overigens zou ik zelf liever R- en S-nomenclatuur gebruiken, omdat daarmee de absolute configuratie wordt vastgelegd.
(1) Bij afsplitsing van één HCl-molecuul ontstaan 4-chloor-1-penteen,
en cis- en trans-4-chloor-2-penteen, waarbij de configuratie aan het asymmetrische C-atoom
niet verandert.
Bedoelen ze hiermee te zeggen dat die L-en D-configuraties er niet in aanwezig zijn?


Blijkbaar was mijn eerste uitleg nog niet duidelijk genoeg, dus dan probeer ik het nog een keer. In 2,4-dichloorpentaan zijn twee stereocentra aanwezig. Na afsplitsen van een molecuul HCl wordt er een dubbele binding gevormd (cis of trans) en blijft er nog één stereocentrum over. Dat stereocentrum heeft of de R- of de S-configuratie. Die configuratie van het overgebleven stereocentrum is hetzelfde als voor afsplitsing van HCl.quote:Op dinsdag 1 maart 2011 12:33 schreef Warren het volgende:
[..]
Bedankt! Maar weet jij misschien wat ze bedoelen met het vetgedrukte
(1) Bij afsplitsing van één HCl-molecuul ontstaan 4-chloor-1-penteen,
en cis- en trans-4-chloor-2-penteen, waarbij de configuratie aan het asymmetrische C-atoom
niet verandert.
Bedoelen ze hiermee te zeggen dat die L-en D-configuraties er niet in aanwezig zijn?
Zoals ik al zei: L en D zou ik hier niet gebruiken, omdat dat meer gebruikelijk is bij biologische moleculen, terwijl R en S de absolute configuratie vastlegt.
Even een voorbeeld met een plaatje: stel je hebt 2S,4R-dichloorpentaan en HCl splitst zich af bij het 2e koolstofatoom. Het 4e koolstofatoom heeft voor afsplitsing de R-configuratie en zal dat na HCl-afsplitsing ook hebben. Links staat het isomeer van 1-penteen en rechts de isomeren van 2-penteen. De configuratie van het vierde koolstofatoom is bij dichloorpentaan al R, bij alle producten blijft dat R. Was die configuratie S geweest, dan was dat ook S gebleven na afsplitsing van HCl bij het tweede koolstofatoom. Dat is wat er bedoeld wordt met de dikgedrukte zin.


Lyolyrc, bedankt  . Ik snap nu wat met de configuratie van het asymmetrische C-atoom wordt bedoeld. Hiermee is de zaak opgehelderd.
. Ik snap nu wat met de configuratie van het asymmetrische C-atoom wordt bedoeld. Hiermee is de zaak opgehelderd.


Ik heb dringend hulp nodig met deze buffer vraag!
Je lost 0,84 g NaHCO3 op in 1,0 L water.
Daarbij voeg je een oplossing van 1 L met 1,06g Na2CO3.
Daarbij voeg je 250mL 0,10 M HNO3-oplossing toe.
Bereken de pH.
De eerste 2 vormen dus een buffer. De H3O+ van HNO3 ( sterk zuur ) reageert met CO3 uit de 1e oplossing, er is echter een overmaat aan H3O+ waardoor al het CO3 opreageert, hoe word de bufferformule dan??
Kz = [H3O+] * 0 / [HCO3]
Dit kan niet want de onbekende, H3O+ valt dan weg omdat je met 0 vermenigvuldigt. Hoe werkt dit?
Je lost 0,84 g NaHCO3 op in 1,0 L water.
Daarbij voeg je een oplossing van 1 L met 1,06g Na2CO3.
Daarbij voeg je 250mL 0,10 M HNO3-oplossing toe.
Bereken de pH.
De eerste 2 vormen dus een buffer. De H3O+ van HNO3 ( sterk zuur ) reageert met CO3 uit de 1e oplossing, er is echter een overmaat aan H3O+ waardoor al het CO3 opreageert, hoe word de bufferformule dan??
Kz = [H3O+] * 0 / [HCO3]
Dit kan niet want de onbekende, H3O+ valt dan weg omdat je met 0 vermenigvuldigt. Hoe werkt dit?


Om te beginnen is het handig om eerst eens te berekenen hoeveel mol van elke stof aanwezig is:quote:Op dinsdag 8 maart 2011 11:10 schreef Dae1337 het volgende:
Ik heb dringend hulp nodig met deze buffer vraag!
Je lost 0,84 g NaHCO3 op in 1,0 L water.
Daarbij voeg je een oplossing van 1 L met 1,06g Na2CO3.
Daarbij voeg je 250mL 0,10 M HNO3-oplossing toe.
Bereken de pH.
De eerste 2 vormen dus een buffer. De H3O+ van HNO3 ( sterk zuur ) reageert met CO3 uit de 1e oplossing, er is echter een overmaat aan H3O+ waardoor al het CO3 opreageert, hoe word de bufferformule dan??
Kz = [H3O+] * 0 / [HCO3]
Dit kan niet want de onbekende, H3O+ valt dan weg omdat je met 0 vermenigvuldigt. Hoe werkt dit?
NaHCO3: 0,84/84,01 = 0,010 mol = 10 mmol
Na2CO3: 1,06/105,99 = 0,010 mol = 10 mmol
HNO3: 0,10*0,250 = 0,025 mol = 25 mmol
Als je het zuur bij de buffer gooit, gaan er twee reacties optreden. In eerste instantie wordt het carbonaat een keer geprotoneerd, zodat bicarbonaat wordt gevormd:
CO32- + H3O+ -> HCO3-
Er is echter slechts 10 mmol carbonaat, wat reageert met 10 mmol zuur, waardoor er nog 15 mmol zuur overblijft. Het restant van het zuur gaat reageren met bicarbonaat, wat leidt tot de vorming van koolzuur. Deze stof splitst zich weer in koolstofdioxide dat uit de oplossing bubbelt en water:
HCO3- + H3O+ -> H2CO3 -> H2O + CO2
Omdat er in totaal 20 mmol bicarbonaat is en 15 mmol zuur, zal er nog 5 mmol bicarbonaat overblijven dat een evenwicht instelt met het water:
HCO3- + H2O <-> CO32- + H3O+
Hierbij hoort de evenwichtsconstante: Ka = [H3O+][CO32-]/[HCO3-]
Laten we stellen dat van de 5 mmol HCO3- er x mmol wordt gedeprotoneerd, wat x mmol CO32- en x mmol H3O+ geeft.
Substitueer deze getallen in de evenwichtsvoorwaarde:
Ka = (x/2,25)(x/2,25)/((5*10-3 - x)/2,25)
Dit geeft de vergelijking: x2 + 2,25*Ka*x - 2,25*5*10-3*Ka = 0
Oplossen geeft x = 7,26*10-7
pH = -log([H3O+]) = -log(7,26*10-7/2,25) = 6,49
Je kunt deze waarde eventueel nog controleren met de Henderson-Hasselbalchvergelijking.


Jij bent mijn held! Duizendmaal dank! Mijn leraar geeft echter een ander antwoord, nl. pH = 5,87. Leraren zijn echter ook mensen die foutjes kunnen maken.quote:Op dinsdag 8 maart 2011 15:22 schreef lyolyrc het volgende:
[..]
Om te beginnen is het handig om eerst eens te berekenen hoeveel mol van elke stof aanwezig is:
NaHCO3: 0,84/84,01 = 0,010 mol = 10 mmol
Na2CO3: 1,06/105,99 = 0,010 mol = 10 mmol
HNO3: 0,10*0,250 = 0,025 mol = 25 mmol
Als je het zuur bij de buffer gooit, gaan er twee reacties optreden. In eerste instantie wordt het carbonaat een keer geprotoneerd, zodat bicarbonaat wordt gevormd:
CO32- + H3O+ -> HCO3-
Er is echter slechts 10 mmol carbonaat, wat reageert met 10 mmol zuur, waardoor er nog 15 mmol zuur overblijft. Het restant van het zuur gaat reageren met bicarbonaat, wat leidt tot de vorming van koolzuur. Deze stof splitst zich weer in koolstofdioxide dat uit de oplossing bubbelt en water:
HCO3- + H3O+ -> H2CO3 -> H2O + CO2
Omdat er in totaal 20 mmol bicarbonaat is en 15 mmol zuur, zal er nog 5 mmol bicarbonaat overblijven dat een evenwicht instelt met het water:
HCO3- + H2O <-> CO32- + H3O+
Hierbij hoort de evenwichtsconstante: Ka = [H3O+][CO32-]/[HCO3-]
Laten we stellen dat van de 5 mmol HCO3- er x mmol wordt gedeprotoneerd, wat x mmol CO32- en x mmol H3O+ geeft.
Substitueer deze getallen in de evenwichtsvoorwaarde:
Ka = (x/2,25)(x/2,25)/((5*10-3 - x)/2,25)
Dit geeft de vergelijking: x2 + 2,25*Ka*x - 2,25*5*10-3*Ka = 0
Oplossen geeft x = 7,26*10-7
pH = -log([H3O+]) = -log(7,26*10-7/2,25) = 6,49
Je kunt deze waarde eventueel nog controleren met de Henderson-Hasselbalchvergelijking.
Bedankt nogmaals


quote:De pH in de dikke darm varieert van 7,5 tot 8,0. Daarom komen in de dikke darm
vrijwel geen carbonzuren voor maar vooral de zuurresten van carbonzuren.
Daarom staan in dit schema niet de namen van de carbonzuren, maar de namen
van de zuurresten pyruvaat, lactaat, acetaat, butanoaat en propanoaat.
Bereken hoe groot de molverhouding propanoaat : propaanzuur in de dikke darm
tenminste is. Maak gebruik van Binas-tabel 49.
Geen moeilijke vraag, alleen in het antwoord gebruiken ze de pH van 7,5. Aangezien de pH varieert tussen 7,5 en 8,0, zou ik de pH van 7,75 nemen. Is dat fout?
Alvast bedankt.


Het antwoord op deze vraag is meer tekstverklaren dan bètawetenschapquote:Op vrijdag 11 maart 2011 12:49 schreef Warren het volgende:
[..]
[ afbeelding ]
Geen moeilijke vraag, alleen in het antwoord gebruiken ze de pH van 7,5. Aangezien de pH varieert tussen 7,5 en 8,0, zou ik de pH van 7,75 nemen. Is dat fout?
Alvast bedankt.
Let op het woordje 'tenminste'. Aangezien bij lagere pH meer zuur en minder zuurrest aanwezig is, zal de verhouding tussen zuurrest en zuur bij pH 7,5 het kleinst zijn. En omdat je de minimale verhouding tussen die twee moet bepalen, moet je rekenen met de laagste pH.quote:Bereken hoe groot de molverhouding propanoaat : propaanzuur in de dikke darm
tenminste is.


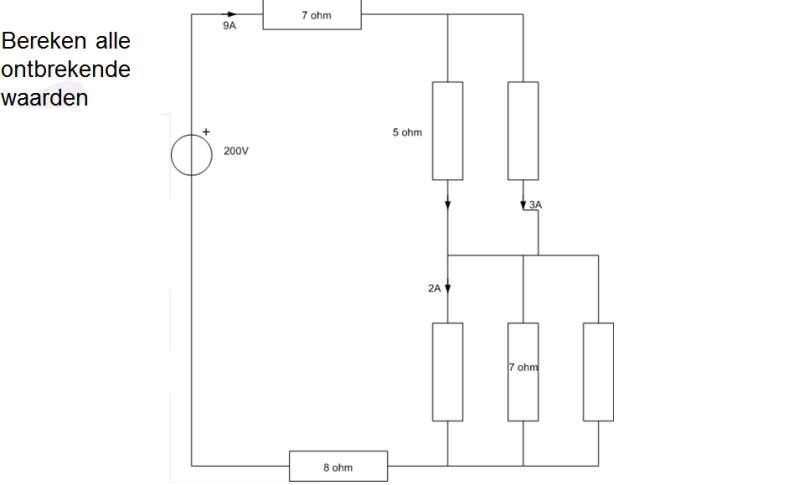
Beetje simpel basisvraag, ben weer even aan het opfrissen elektrotechniek:
De eerste 2 weerstanden zijn 5 en 10 met 6 e 3 ampere denk ik. Maar hoe pak ik die 3 andere weerstanden aan?
De eerste 2 weerstanden zijn 5 en 10 met 6 e 3 ampere denk ik. Maar hoe pak ik die 3 andere weerstanden aan?
Blues ain't nothing but a good man feeling bad...


Oh wacht ik denk dat ik het weet. Je berekent nog even de spanning over de 8 ohm weerstand. Vervolgens trekt je alle spanningen van de Bron spanning af. Dan hou je getal voor de spanning over de 3 weerstanden over. En dan is het eitje.
Correct?
Correct?
Blues ain't nothing but a good man feeling bad...


Dat is volgens mij correct. Wat krijg je voor waarden?
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


Spanning over 8Ohm weerstand 72V.
Spanning over de 3 weerstanden is 35V.
vlnr. 17,5 ohm, 7 ohm, 17,5 ohm
vlnr. 2 A, 5 A, 2 A
Spanning over de 3 weerstanden is 35V.
vlnr. 17,5 ohm, 7 ohm, 17,5 ohm
vlnr. 2 A, 5 A, 2 A
Blues ain't nothing but a good man feeling bad...


Klopt allemaalquote:Op woensdag 16 maart 2011 15:11 schreef GoodGawd het volgende:
Spanning over 8Ohm weerstand 72V.
Spanning over de 3 weerstanden is 35V.
vlnr. 17,5 ohm, 7 ohm, 17,5 ohm
vlnr. 2 A, 5 A, 2 A
The biggest argument against democracy is a five minute discussion with the average voter.


Ik kreeg er zelf twee tegenstrijdige antwoorden uit:quote:Wordt de pH van de oplossing hoger, of lager wanneer een half kopje bakpoeder
in plaats van een kwart kopje wordt gebruikt, of krijg je een oplossing met
dezelfde pH (298 K)? Geef een verklaring voor je antwoord.
- Aan de ene kant dacht ik dat de pH hetzelfde zou zijn aangezien de Kb, Kz, en Kw niet veranderen als je meer bakpoeder toevoegt. Ook zie je nergens in de formule dat de [H3O+] afhankelijk is van de hoeveelheid bakpoeder.
- Aan de andere kant dacht ik dat de pH hoger zou worden omdat HCO3- met water als base reageert omdat het een amfolyt is en Kb>Kz. Als je meer HCO3- toevoegt, heb je meer OH- ionen en dus een hogere pH, want het evenwicht ligt meer rechts bij HCO3- + H2O <> H2CO3 + OH-
Het antwoordenmodel zegt:
Waarom is het ene antwoord "correcter" dan het andere? (Hoe is de tegenstrijdigheid te verklaren?)quote:Voorbeelden van een juist antwoord zijn:
− Volgens de gegeven formule is de [H3O+] niet afhankelijk van de
hoeveelheid bakpoeder die wordt opgelost, dus krijg je een oplossing
met dezelfde pH wanneer de dubbele hoeveelheid bakpoeder wordt
gebruikt. 2 punten
of
− Kw, Kz en Kb zijn constanten (bij 298 K), dus krijg je een oplossing met
dezelfde pH wanneer de dubbele hoeveelheid bakpoeder wordt
gebruikt. 2 punten
Indien een antwoord is gegeven als: „Natriumwaterstofcarbonaat is
(overwegend) een base, dus als je meer oplost per liter wordt de pH hoger.”
1 punt
Alvast bedankt.


oke, ik moet een paar vragen doen waar ik niks van snap, hopelijk kunnen jullie helpen.
Ik moest een experiment doen, waarbij ik 3 stoffen moest mensen: Natriumthiosulfaatoplossing (Na2S2O3), gedestilleerd water en waterstofchlorideoplossing (zoutzuur, HCl).
Ik heb 5 metingen gedaan, de hoeveelheden van elke vloeistof in mL:
Meting 1 2 3 4 5
Na2S2O3 10 15 20 25 30
gedes. water 35 30 25 20 15
zoutzuur 5 5 5 5 5
Nu moet ik bij elke meting de [S2O3²-] bepalen. Maar ik heb geen idee hoe?
Ook moet ik nog een paar vragen beantwoorden over medicijnen, met massa% en oplossen van jood etc. kan iemand me hierbij helpen?
alvast bedankt!
Ik moest een experiment doen, waarbij ik 3 stoffen moest mensen: Natriumthiosulfaatoplossing (Na2S2O3), gedestilleerd water en waterstofchlorideoplossing (zoutzuur, HCl).
Ik heb 5 metingen gedaan, de hoeveelheden van elke vloeistof in mL:
Meting 1 2 3 4 5
Na2S2O3 10 15 20 25 30
gedes. water 35 30 25 20 15
zoutzuur 5 5 5 5 5
Nu moet ik bij elke meting de [S2O3²-] bepalen. Maar ik heb geen idee hoe?
Ook moet ik nog een paar vragen beantwoorden over medicijnen, met massa% en oplossen van jood etc. kan iemand me hierbij helpen?
alvast bedankt!


hmm, die eerste:quote:Op zondag 20 maart 2011 15:26 schreef hussyfan11 het volgende:
oke, ik moet een paar vragen doen waar ik niks van snap, hopelijk kunnen jullie helpen.
Ik moest een experiment doen, waarbij ik 3 stoffen moest mensen: Natriumthiosulfaatoplossing (Na2S2O3), gedestilleerd water en waterstofchlorideoplossing (zoutzuur, HCl).
Ik heb 5 metingen gedaan, de hoeveelheden van elke vloeistof in mL:
Meting 1 2 3 4 5
Na2S2O3 10 15 20 25 30
gedes. water 35 30 25 20 15
zoutzuur 5 5 5 5 5
Nu moet ik bij elke meting de [S2O3²-] bepalen. Maar ik heb geen idee hoe?
Ook moet ik nog een paar vragen beantwoorden over medicijnen, met massa% en oplossen van jood etc. kan iemand me hierbij helpen?
alvast bedankt!
werk eerst de reactievergelijkingen uit, gebruik binas tabel 48,
je hebt aanwezig:
S203 2-, H2O, H +, CL-
kijk naar sterkste oxidator en reductor... (cl en s2o3) en schrijf halfvergelijkingen en totaalvergelijking op
dan kijk hoeveel ml je toevoegd van alles, en reken dit om naar mol. (je weet molair?)
vergelijk molverhoudingen in de reactievergelijkingen en klaar is kees:D


Bedankt! Maar ik weet niet hoe ik omreken van ml naar mol?quote:Op zondag 20 maart 2011 17:30 schreef kevintjuhh2 het volgende:
[..]
hmm, die eerste:
werk eerst de reactievergelijkingen uit, gebruik binas tabel 48,
je hebt aanwezig:
S203 2-, H2O, H +, CL-
kijk naar sterkste oxidator en reductor... (cl en s2o3) en schrijf halfvergelijkingen en totaalvergelijking op
dan kijk hoeveel ml je toevoegd van alles, en reken dit om naar mol. (je weet molair?)
vergelijk molverhoudingen in de reactievergelijkingen en klaar is kees:D


nou je hebt wss de molariteit van de gebruikte oplossingen gekregen (of je hebt de oplossingen zelf gemaakt), bijv 1.0 M (molair) wat beteken 1 mol per liter...
heb jij 5 ml dan heb je 5 milli mol (of 5 * 10^-3 * 1 mol) snap je?
heb jij 5 ml dan heb je 5 milli mol (of 5 * 10^-3 * 1 mol) snap je?


ah bedankt!quote:Op zondag 20 maart 2011 18:48 schreef kevintjuhh2 het volgende:
nou je hebt wss de molariteit van de gebruikte oplossingen gekregen (of je hebt de oplossingen zelf gemaakt), bijv 1.0 M (molair) wat beteken 1 mol per liter...
heb jij 5 ml dan heb je 5 milli mol (of 5 * 10^-3 * 1 mol) snap je?
edit: ik kom er toch niet helemaal uit, kun je misschien eentje voor doen?
[ Bericht 13% gewijzigd door hussyfan11 op 20-03-2011 20:36:27 ]


hmm, ik zal dan een iets andere pakken, dan snap je het miss eerder:P
ik los 20 gram jood op in 150 ml water, bereken de concentratie I-, (ga er hierbij vanuit dat het volume door het oplossen van jood niet veranderd)
20 gram jood = 20 / molaire massa jood (I2 let op 2x) = 20 / ( 2*126,9)
echter opgelost levert dit weer I- (aq) is dus weer 2x zoveel molair als I2 (s)...
dus in de oplossing krijg je uiteindelijk 20 / 126.9 = 0.158 mol I- = 1.58 * 10^-1 mol
dit zit in 150 ml. maar molair (of concentratie) is per liter. dus je doet aantal mol / aantal liter --> 1.58 * 10^-1 / 0.150 = 1.05 mol per liter...
ik los 20 gram jood op in 150 ml water, bereken de concentratie I-, (ga er hierbij vanuit dat het volume door het oplossen van jood niet veranderd)
20 gram jood = 20 / molaire massa jood (I2 let op 2x) = 20 / ( 2*126,9)
echter opgelost levert dit weer I- (aq) is dus weer 2x zoveel molair als I2 (s)...
dus in de oplossing krijg je uiteindelijk 20 / 126.9 = 0.158 mol I- = 1.58 * 10^-1 mol
dit zit in 150 ml. maar molair (of concentratie) is per liter. dus je doet aantal mol / aantal liter --> 1.58 * 10^-1 / 0.150 = 1.05 mol per liter...


ik snap het nu bijna, alleen weet ik niet hoe ik dit bereken met de gegevens die ik heb.quote:Op zondag 20 maart 2011 21:17 schreef kevintjuhh2 het volgende:
hmm, ik zal dan een iets andere pakken, dan snap je het miss eerder:P
ik los 20 gram jood op in 150 ml water, bereken de concentratie I-, (ga er hierbij vanuit dat het volume door het oplossen van jood niet veranderd)
20 gram jood = 20 / molaire massa jood (I2 let op 2x) = 20 / ( 2*126,9)
echter opgelost levert dit weer I- (aq) is dus weer 2x zoveel molair als I2 (s)...
dus in de oplossing krijg je uiteindelijk 20 / 126.9 = 0.158 mol I- = 1.58 * 10^-1 mol
dit zit in 150 ml. maar molair (of concentratie) is per liter. dus je doet aantal mol / aantal liter --> 1.58 * 10^-1 / 0.150 = 1.05 mol per liter...
Ik heb dus een mengsel van gedestilleerd water, zoutzuur en natriumthiosulfaatoplossing waarvan ik alleen weet hoeveel ml ik van elke stof heb, geen massa, en nu moet ik de concentratie S2O3 berekenen. ;p


mwah je moet de molariteit van thio weten, dat staat wss in de vraag... anders weet ik het ook niet... [hcl] kan je nog uitrekenen adhv ph...


geen idee of ik het in t goede topic plaats...
weet iemand wanneer je bij levensverzekeringswiskunde bij een kleine 'a' een streepje zet?
Ik dacht bij het berekenen van pensioen gerelateerde dingen.. Maar in de uitwerkingen blijkt dat niet zo te zijn. Weet iemand dit??
weet iemand wanneer je bij levensverzekeringswiskunde bij een kleine 'a' een streepje zet?
Ik dacht bij het berekenen van pensioen gerelateerde dingen.. Maar in de uitwerkingen blijkt dat niet zo te zijn. Weet iemand dit??


In een topic tijdje terug had ik deze vraag ook:
Toen was de conclusie:
4 kopen en dan als volg schakelen:
2serie
-
2serie
En deze 2 in serie weer parallel. Maar nu kwam ik dit weer tegen en dacht hoe kan dat?
Want 12V/100A in serie daar komt toch uit: 24V/100A...
Of zie ik dit verkeerd omdat dit spannings bronnen zijn dus tel je stroom bijelkaar op.
Toen was de conclusie:
4 kopen en dan als volg schakelen:
2serie
-
2serie
En deze 2 in serie weer parallel. Maar nu kwam ik dit weer tegen en dacht hoe kan dat?
Want 12V/100A in serie daar komt toch uit: 24V/100A...
Of zie ik dit verkeerd omdat dit spannings bronnen zijn dus tel je stroom bijelkaar op.
Blues ain't nothing but a good man feeling bad...


12V/100Ah in serie daar komt uit: 24V/100Ah
Je moet inderdaad 4 stukken van [2 in serie] in parallel hebben.
Je moet inderdaad 4 stukken van [2 in serie] in parallel hebben.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Staat er ook een getal bij?quote:Op zondag 20 maart 2011 22:41 schreef Mekkalomp het volgende:
geen idee of ik het in t goede topic plaats...
weet iemand wanneer je bij levensverzekeringswiskunde bij een kleine 'a' een streepje zet?
Ik dacht bij het berekenen van pensioen gerelateerde dingen.. Maar in de uitwerkingen blijkt dat niet zo te zijn. Weet iemand dit??
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


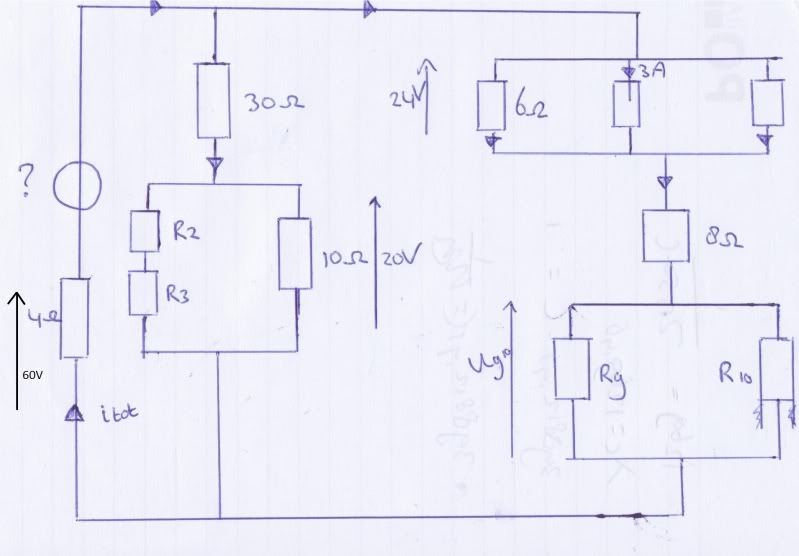
Ik word gek:
Zie hierboven een sommetje dat gegeven werd in 't college. Dit gaf hij zo op. Vervolgens heeft hij alles uitgewerkt. Ik heb dus alle waarde en antwoorden en hoe hij dingen oplost mbv subsitutie. Bij onder andere R9/R10 en R2/R3.
Nu heb ik dus dit, das heel simpel:
Maar nu zie ik niet meer waar ik verder moet.... Ik weet dat de 15A zich opsplitst door het middelste weerstanden blok 5A lopen en door het rechtse weerstanden blok 10A. Maar ik zie even niet hoe ik er kom.
Kan iemand even een voorzet geven? Daarna kom ik er wel uit (:
Zie hierboven een sommetje dat gegeven werd in 't college. Dit gaf hij zo op. Vervolgens heeft hij alles uitgewerkt. Ik heb dus alle waarde en antwoorden en hoe hij dingen oplost mbv subsitutie. Bij onder andere R9/R10 en R2/R3.
Nu heb ik dus dit, das heel simpel:
Maar nu zie ik niet meer waar ik verder moet.... Ik weet dat de 15A zich opsplitst door het middelste weerstanden blok 5A lopen en door het rechtse weerstanden blok 10A. Maar ik zie even niet hoe ik er kom.
Kan iemand even een voorzet geven? Daarna kom ik er wel uit (:
Blues ain't nothing but a good man feeling bad...


Door de weerstand van 10 Ohm gaat 2 A. Dat kun je sowieso nog toevoegen. Ik vraag me trouwens af of je ooit R2 en R3 kunt bepalen. Die weerstanden staan in serie en zijn daarom te vervangen door een weerstand R2 + R3. Maar hoe kun je ze afzonderlijk bepalen als je niet tenminste de spanning over een van beide afzonderlijk weet?quote:Op dinsdag 22 maart 2011 22:43 schreef GoodGawd het volgende:
Ik word gek:
[ afbeelding ]
Zie hierboven een sommetje dat gegeven werd in 't college. Dit gaf hij zo op. Vervolgens heeft hij alles uitgewerkt. Ik heb dus alle waarde en antwoorden en hoe hij dingen oplost mbv subsitutie. Bij onder andere R9/R10 en R2/R3.
Nu heb ik dus dit, das heel simpel:
[ afbeelding ]
Maar nu zie ik niet meer waar ik verder moet.... Ik weet dat de 15A zich opsplitst door het middelste weerstanden blok 5A lopen en door het rechtse weerstanden blok 10A. Maar ik zie even niet hoe ik er kom.
Kan iemand even een voorzet geven? Daarna kom ik er wel uit (:


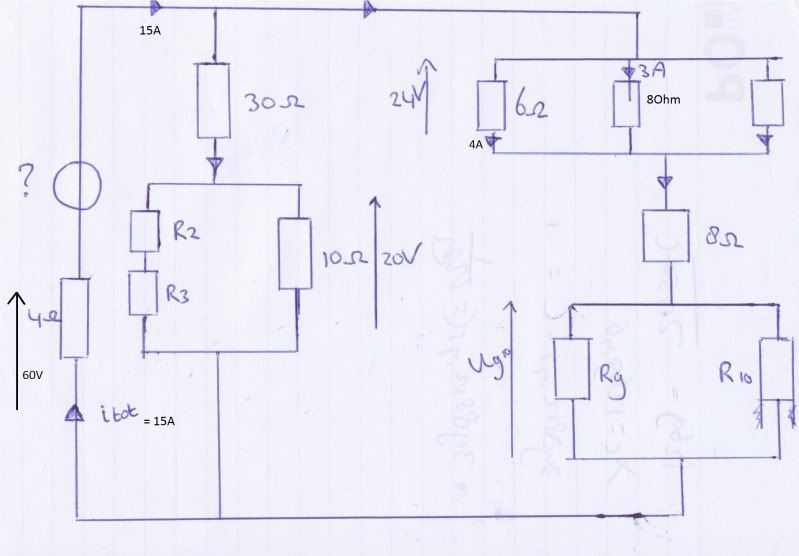
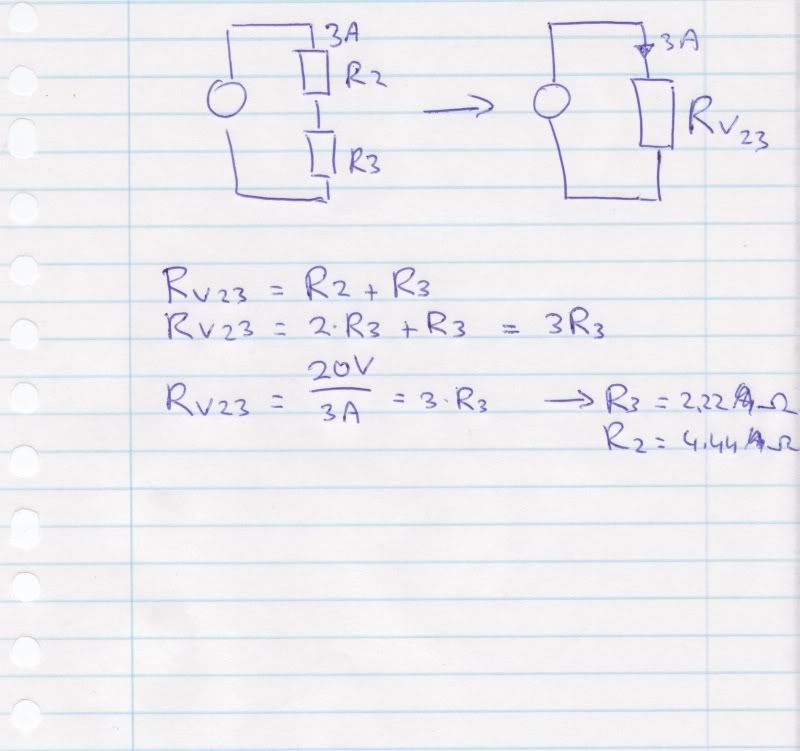
Het stukje uitvergroot, spanningsbron dus zien als 20V :
Zo werd dat vandaag in 't college gedaan, mbv subsitutie. Maar om daar te komen moet ik toch eerst er achter komen hoe ik de stap daarvoor zet. Want die 3A heb ik nog niet.
Dit ziet er ook leuk uit trouwens, maar ik zie die hele subsitutie niet meer waar ik dat vanmiddag nog wel door had.
Zo werd dat vandaag in 't college gedaan, mbv subsitutie. Maar om daar te komen moet ik toch eerst er achter komen hoe ik de stap daarvoor zet. Want die 3A heb ik nog niet.
Dit ziet er ook leuk uit trouwens, maar ik zie die hele subsitutie niet meer waar ik dat vanmiddag nog wel door had.
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.Blues ain't nothing but a good man feeling bad...


quote:Op dinsdag 22 maart 2011 23:53 schreef GoodGawd het volgende:
Het stukje uitvergroot, spanningsbron dus zien als 20V :
[ afbeelding ]
Zo werd dat vandaag in 't college gedaan, mbv subsitutie. Maar om daar te komen moet ik toch eerst er achter komen hoe ik de stap daarvoor zet. Want die 3A heb ik nog niet.
Dit ziet er ook leuk uit trouwens, maar ik zie die hele subsitutie niet meer waar ik dat vanmiddag nog wel door had. Uit de uitwerking die je hier geeft, leid ik af dat je weet hoe R2 en R3 zich tot elkaar verhouden. Want je stelt R2 = 2*R3. Als je niet weet hoe die twee zich verhouden, of wat de spanning over een van beide is, zou je R2 en R3 niet kunnen bepalen.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.
Uit de uitwerking die je hier geeft, leid ik af dat je weet hoe R2 en R3 zich tot elkaar verhouden. Want je stelt R2 = 2*R3. Als je niet weet hoe die twee zich verhouden, of wat de spanning over een van beide is, zou je R2 en R3 niet kunnen bepalen.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


Oh verrek! Ja lampje brandt weer! Er werd iets onder de som geschreven, maar dat kon ik niet lezen dus nam ik dat niet over. Dacht dat het gewoon wat gebrabbel was. Maar dat waren de verhoudingen, kan niet anders. Bij R9 en R10 is de verhouding: R10 = 4xR9. (leid ik af uit mijn aantekeningen)
Maar nu dit bekend is, moet ik nog de stap ervoor weten....Hmm...
Maar nu dit bekend is, moet ik nog de stap ervoor weten....Hmm...
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.
[ Bericht 16% gewijzigd door GoodGawd op 23-03-2011 00:12:42 ]Blues ain't nothing but a good man feeling bad...


quote:Op woensdag 23 maart 2011 00:07 schreef GoodGawd het volgende:
Oh verrek! Ja lampje brandt weer! Er werd iets onder de som geschreven, maar dat kon ik niet lezen dus nam ik dat niet over. Dacht dat het gewoon wat gebrabbel was. Maar dat waren de verhoudingen, kan niet anders. Bij R9 en R10 is de verhouding: R10 = 4xR9. (leid ik af uit mijn aantekeningen)
Maar nu dit bekend is, moet ik nog de stap ervoor weten....Hmm...Het zou zomaar kunnen dat er nog iets gegeven was over de weerstand rechtsboven. Anders zou ik het ook niet weten.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.


quote:Op woensdag 23 maart 2011 00:07 schreef GoodGawd het volgende:
Oh verrek! Ja lampje brandt weer! Er werd iets onder de som geschreven, maar dat kon ik niet lezen dus nam ik dat niet over. Dacht dat het gewoon wat gebrabbel was. Maar dat waren de verhoudingen, kan niet anders. Bij R9 en R10 is de verhouding: R10 = 4xR9. (leid ik af uit mijn aantekeningen)
Maar nu dit bekend is, moet ik nog de stap ervoor weten....Hmm...De spanning over weerstand 9 en 10 is niet bekend, of wel? Als die bekend is, is het uit te rekenen, anders gaat het geloof ik niet met de waarden die er nu staan.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.The biggest argument against democracy is a five minute discussion with the average voter.


Nee is niet bekend. Ik denk dat dat ik de eerste aftakking 5A als gegeven moet geven. Dan lukt het allemaal wel (:
Blues ain't nothing but a good man feeling bad...


Ik blijf toch het gevoel houden dat er nog iets is met de weerstand rechtsboven. Als hij onbekend is, zou er minimaal R7 bij moeten staan. Is hij wel bekend, zou de grootte van de weerstand vermeld moeten staan. Maar juist omdat er niets staat, zou het zomaar kunnen zijn dat je iets vergeten bent. Ook het "gekrabbel" onder de schakeling, dat je niet hebt overgenomen, kan nog belangrijke informatie hebben bevat.quote:Op woensdag 23 maart 2011 15:17 schreef GoodGawd het volgende:
Nee is niet bekend. Ik denk dat dat ik de eerste aftakking 5A als gegeven moet geven. Dan lukt het allemaal wel (:


Ik ben bezig met de Taylorreeks, en nu is het de bedoeling dat ik wortel(1,1) bereken tot op 4 significante cijfers nauwkeurig door middel van de taylorreeks.
Ik heb wel de formule maar de afgeleide van wortel(1,1) is gewoon 0, dus ik kan er niet veel mee.
Ik heb wel de formule maar de afgeleide van wortel(1,1) is gewoon 0, dus ik kan er niet veel mee.
Drawing a confession out of someone is like doing a beautiful dance. A beautiful dance, with a chainsaw.


Je kunt wortel(x) rond x=1 benaderen.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Stel de formule als wortel (x,y)?quote:Op donderdag 24 maart 2011 15:26 schreef KeizerKuzco het volgende:
Ik ben bezig met de Taylorreeks, en nu is het de bedoeling dat ik wortel(1,1) bereken tot op 4 significante cijfers nauwkeurig door middel van de taylorreeks.
Ik heb wel de formule maar de afgeleide van wortel(1,1) is gewoon 0, dus ik kan er niet veel mee.


Maar als ik de taylorbenadering geef voor wortel(x) rond x=1 dan vergeet ik die 0,1 uit de wortel. Of kan ik die dan nog apart benaderen met een tweede taylorreeks?
Drawing a confession out of someone is like doing a beautiful dance. A beautiful dance, with a chainsaw.


Het hele idee is dat je hem benadert met een benadering vanaf punt 1. Met de taylor stel je een alternatieve formule op die, hoe meer termen die heeft, hoe preciezer wordt over een wijder bereik. Er is ook een formule die ik zo niet uit mijn hoofd weet waarmee je na kunt gaan hoe precies een taylorbenadering is dacht ik.quote:Op donderdag 24 maart 2011 15:35 schreef KeizerKuzco het volgende:
Maar als ik de taylorbenadering geef voor wortel(x) rond x=1 dan vergeet ik die 0,1 uit de wortel. Of kan ik die dan nog apart benaderen met een tweede taylorreeks?


Als ik rond x = 1 doe, dan krijg ik zoiets.
f(1) + f'(1)*(x-1) + 1/2f''(1)*(x-1)^2 + 1/3f'''(1)*(x-1)^3
Ik weet ook wel hoe ik wortel(x) af moet leiden, maar moet ik dan gewoon invullen in de formule?
f(1) + f'(1)*(x-1) + 1/2f''(1)*(x-1)^2 + 1/3f'''(1)*(x-1)^3
Ik weet ook wel hoe ik wortel(x) af moet leiden, maar moet ik dan gewoon invullen in de formule?
Drawing a confession out of someone is like doing a beautiful dance. A beautiful dance, with a chainsaw.


1/3 is fout. En nu nog kijken hoe je de foutterm klein genoeg krijgt.
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


1/6 mijn fout.
Als ik nu ga invullen, en ik vul 1,1 in voor x dan krijg ik:
1 + 0,05 - 1,25*10^-3 + 6,25*10^-5 = 1,0488
Met mijn rekenmachine zie ik dat wortel(1,1) inderdaad 1,048808848 is.
Wat bedoel je met de foutterm? Ik moet er inderdaad voor zorgen dat de rest kleiner is dan 5*10^-4
Als ik nu ga invullen, en ik vul 1,1 in voor x dan krijg ik:
1 + 0,05 - 1,25*10^-3 + 6,25*10^-5 = 1,0488
Met mijn rekenmachine zie ik dat wortel(1,1) inderdaad 1,048808848 is.
Wat bedoel je met de foutterm? Ik moet er inderdaad voor zorgen dat de rest kleiner is dan 5*10^-4
Drawing a confession out of someone is like doing a beautiful dance. A beautiful dance, with a chainsaw.


Zie Cauchy's estimate op http://en.wikipedia.org/wiki/Taylor%27s_theorem
eee7a201261dfdad9fdfe74277d27e68890cf0a220f41425870f2ca26e0521b0


Ik snap niks van die remainder, maar dat eerste deel is tenminste af.
Bedankt he
Bedankt he
Drawing a confession out of someone is like doing a beautiful dance. A beautiful dance, with a chainsaw.


Ik heb nog 2 vragen waar ik niet uit kom.
Bij de eerste is er een verhaaltje ervoor: Jodiumtinctuur bevat 2,0 massa% jood, 2,5 massa% natriumjodide (of kaliumjodide) en 48% ethanol.
Waardoor lost in jodiumtinctuur zowel het apolaire jood als de twee jodidezouten op?
De 2e vraag:
Geef de vergelijking van de reactie waarin een molecuul povidonjood (voor te stellen als PV(I2)n ) een molecuul jood afstaat.
Wat voor reactie zal dit worden? Loopt deze reactie vanzelf? Ik snap niet zo goed hoe de reactie zal lopen.
Alvast bedankt!
[ Bericht 0% gewijzigd door hussyfan11 op 24-03-2011 19:38:33 ]
Bij de eerste is er een verhaaltje ervoor: Jodiumtinctuur bevat 2,0 massa% jood, 2,5 massa% natriumjodide (of kaliumjodide) en 48% ethanol.
Waardoor lost in jodiumtinctuur zowel het apolaire jood als de twee jodidezouten op?
De 2e vraag:
Geef de vergelijking van de reactie waarin een molecuul povidonjood (voor te stellen als PV(I2)n ) een molecuul jood afstaat.
Wat voor reactie zal dit worden? Loopt deze reactie vanzelf? Ik snap niet zo goed hoe de reactie zal lopen.
Alvast bedankt!
[ Bericht 0% gewijzigd door hussyfan11 op 24-03-2011 19:38:33 ]


Voor oplossen is het van belang dat de op te lossen stof en het oplosmiddel graag bij elkaar in de buurt zitten. Dat betekent dat apolaire stoffen graag in een apolair of weinig polair oplosmiddel zitten, terwijl polaire stoffen en zouten graag in een polair oplosmiddel vertoeven.quote:Op donderdag 24 maart 2011 19:19 schreef hussyfan11 het volgende:
Ik heb nog 2 vragen waar ik niet uit kom.
Bij de eerste is er een verhaaltje ervoor: Jodiumtinctuur bevat 2,0 massa% jood, 2,5 massa% natriumjodide (of kaliumjodide) en 48% ethanol.
Waardoor lost in jodiumtinctuur zowel het apolaire jood als de twee jodidezouten op?
De jodidezouten lossen daarom op in een polair oplosmiddel, in dit geval water. Jood wil juist een apolair of minder polair oplosmiddel, in dit geval ethanol. Ethanolmoleculen richten de apolaire staart op de joodmoleculen, zodat elk joodmolecuul totaal omsloten wordt door ethanol. De polaire alcoholgroep van elk ethanolmolecuul is op het omringende water is gericht, zodat de waterige oplossing en de ethanoloplossing zich ook met elkaar vermengen.
Met deze notatie voor povidonjood zou ik zeggen:quote:De 2e vraag:
Geef de vergelijking van de reactie waarin een molecuul povidonjood (voor te stellen als PV(I2)n ) een molecuul jood afstaat.
Wat voor reactie zal dit worden? Loopt deze reactie vanzelf? Ik snap niet zo goed hoe de reactie zal lopen.
Alvast bedankt!
PV(I2)n -> PV(I2)n-1 + I2


Bedankt! Dit helpt me echt!quote:Op donderdag 24 maart 2011 19:55 schreef lyolyrc het volgende:
[..]
Voor oplossen is het van belang dat de op te lossen stof en het oplosmiddel graag bij elkaar in de buurt zitten. Dat betekent dat apolaire stoffen graag in een apolair of weinig polair oplosmiddel zitten, terwijl polaire stoffen en zouten graag in een polair oplosmiddel vertoeven.
De jodidezouten lossen daarom op in een polair oplosmiddel, in dit geval water. Jood wil juist een apolair of minder polair oplosmiddel, in dit geval ethanol. Ethanolmoleculen richten de apolaire staart op de joodmoleculen, zodat elk joodmolecuul totaal omsloten wordt door ethanol. De polaire alcoholgroep van elk ethanolmolecuul is op het omringende water is gericht, zodat de waterige oplossing en de ethanoloplossing zich ook met elkaar vermengen.
[..]
Met deze notatie voor povidonjood zou ik zeggen:
PV(I2)n -> PV(I2)n-1 + I2


Nu met kernenergie dagelijks in het nieuws mogen wij van de docent gaan beredeneren wat de voor- en tegenargumenten van kernenergie, gezien vanuit de natuurkunde.
Buiten rendement, radioactiviteit en halfwaardetijd kan ik enkel economische en milieu argumenten bedenken.
Iemand die mij wat dieper vanuit de natuurkunde kan helpen kijken op kernenergie?
Buiten rendement, radioactiviteit en halfwaardetijd kan ik enkel economische en milieu argumenten bedenken.
Iemand die mij wat dieper vanuit de natuurkunde kan helpen kijken op kernenergie?


Ik vind dit nog steeds een van de meest interessante artikelen die er op het web te vinden zijn:quote:Op zondag 27 maart 2011 18:37 schreef Blaqman het volgende:
Nu met kernenergie dagelijks in het nieuws mogen wij van de docent gaan beredeneren wat de voor- en tegenargumenten van kernenergie, gezien vanuit de natuurkunde.
Buiten rendement, radioactiviteit en halfwaardetijd kan ik enkel economische en milieu argumenten bedenken.
Iemand die mij wat dieper vanuit de natuurkunde kan helpen kijken op kernenergie?
http://www.ornl.gov/info/ornlreview/rev26-34/text/colmain.html
Bij een normaal werkende kerncentrale blijft het afval opgesloten zitten. Je houdt er altijd controle over. Bij een met kolen gestookte centrale wordt het radioactieve materiaal het milieu in gepompt.
Good intentions and tender feelings may do credit to those who possess them, but they often lead to ineffective — or positively destructive — policies ... Kevin D. Williamson


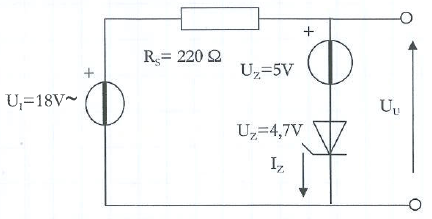
Ik probeer iemand te helpen met zenerdiodes. Omdat het al even geleden is ben ik aan het oefenen, maar ik zit vast bij de volgende schakeling:
Hierbij is Ui een wisselspanning met effectieve waarde 18V.
Als Ui hoog is, staat de zenerdiode in doorlaatrichting en wordt de uitgang ongeveer 5V (+drempelspanning). Als Ui laag, staat de zener in sper en wordt de uitgang ongeveer 0,3V.
Maar wat gebeurt er als Ui tussen deze spanningen zit? Wordt dat een steile lijn of een gemiddelde waarde?
Hierbij is Ui een wisselspanning met effectieve waarde 18V.
Als Ui hoog is, staat de zenerdiode in doorlaatrichting en wordt de uitgang ongeveer 5V (+drempelspanning). Als Ui laag, staat de zener in sper en wordt de uitgang ongeveer 0,3V.
Maar wat gebeurt er als Ui tussen deze spanningen zit? Wordt dat een steile lijn of een gemiddelde waarde?
Doei


In volgende 2 opgaven zit ik altijd de klooien met de wrijving coëfficiënten. Bij de eerste geven ze je de statische wrijving coëfficiënt. Zoals je in het VLS tekeningetje ziet passen ze de statische toe bij het wiel dat de aandrijving levert. T wiel dat vrij rolt heeft geen wrijving blijkbaar.
In som 2, krijg je de kinetische en statische. Daarin passen ze de statische toe op het wiel dat slipt en de statische gebruiken ze niet.
http://img10.imageshack.us/img10/7900/fsgdf.png (copy/paste deze link)
Wat is nou het verschil tussen een wiel die aandrijving heeft en een wiel dat vrij rolt. Als ik het oppervlak tussen die 2 wielen onder loep zou nemen zou ik niet echt een verschil kunnen verzinnen. Mij lijkt dat een vrij lopend wiel ook die zelfde statische wrijving heeft...?
In som 2, krijg je de kinetische en statische. Daarin passen ze de statische toe op het wiel dat slipt en de statische gebruiken ze niet.
http://img10.imageshack.us/img10/7900/fsgdf.png (copy/paste deze link)
Wat is nou het verschil tussen een wiel die aandrijving heeft en een wiel dat vrij rolt. Als ik het oppervlak tussen die 2 wielen onder loep zou nemen zou ik niet echt een verschil kunnen verzinnen. Mij lijkt dat een vrij lopend wiel ook die zelfde statische wrijving heeft...?
Blues ain't nothing but a good man feeling bad...


Ik denk dat ze aannemen dat er geen kracht achter een vrij lopend wiel zit. Deze rolt dus mee (remt niet en versnelt niet) en het gewicht van de wielen mogen verwaarloosd worden, dus er is geen inertia.quote:Op dinsdag 29 maart 2011 14:04 schreef GoodGawd het volgende:
In volgende 2 opgaven zit ik altijd de klooien met de wrijving coëfficiënten. Bij de eerste geven ze je de statische wrijving coëfficiënt. Zoals je in het VLS tekeningetje ziet passen ze de statische toe bij het wiel dat de aandrijving levert. T wiel dat vrij rolt heeft geen wrijving blijkbaar.
In som 2, krijg je de kinetische en statische. Daarin passen ze de statische toe op het wiel dat slipt en de statische gebruiken ze niet.
[ http://img10.imageshack.us/img10/7900/fsgdf.png (copy/paste deze link) ]
Wat is nou het verschil tussen een wiel die aandrijving heeft en een wiel dat vrij rolt. Als ik het oppervlak tussen die 2 wielen onder loep zou nemen zou ik niet echt een verschil kunnen verzinnen. Mij lijkt dat een vrij lopend wiel ook die zelfde statische wrijving heeft...?
Doei


ik heb een vraagje over Mechanica, hoop dat er iemand is die me kan helpen:
Het berekenen op sterkte vind ik een makkie, maar op stijfheid lukt me maar niet.
Ik dacht eraan om eerst:
W te berekenen, dan I en daarna de hoogte (h).
Het berekenen op sterkte vind ik een makkie, maar op stijfheid lukt me maar niet.
Ik dacht eraan om eerst:
W te berekenen, dan I en daarna de hoogte (h).
★★★


Het is nogal lang geleden voor mij, maar ik denk dat je het volgende moet doen:quote:Op dinsdag 5 april 2011 20:10 schreef ajacied4lf het volgende:
ik heb een vraagje over Mechanica, hoop dat er iemand is die me kan helpen:
[ afbeelding ]
Het berekenen op sterkte vind ik een makkie, maar op stijfheid lukt me maar niet.
Ik dacht eraan om eerst:
W te berekenen, dan I en daarna de hoogte (h).
Er bestaan formules voor de maximale doorbuiging van balken. Je gebruikt de formule die van toepassing is op deze situatie en je stelt de maximale doorbuiging gelijk aan de toelaatbare doorbuiging. Hiermee bereken je het oppervlaktetraagheidsmoment I. Vervolgens bereken je de hoogte weer met behulp van de formule voor I.
In mijn mechanicaboek vond ik voor de maximale doorbuiging in deze situatie: -5wL4/(384EI). Mijn boek gebruikt mogelijk andere symbolen dan je gewend bent. In deze formule is w gelijk aan q in jouw plaatje, L is de lengte van de balk, E is de elasticiteitsmodulus en I het oppervlaktetraagheidsmoment.
Ik heb zelf de berekening al uitgevoerd, maar ik twijfel een beetje aan de uitkomst. Mocht deze benadering niet goed zijn, dan biedt het misschien nog aanknopingspunten voor de juiste benadering.


Ik heb morgen een natuurkunde toets en ik zit nu een beetje op internet te oefenen met een vraagstuk dat vorig jaar ook in de toets zat. Het betreft het volgende vraagstuk : http://www.natuurkunde.nl/artikelen/view.do?supportId=2062 en ik snap er geen ene moer van ook al staan de uitwerkingen eronder. Iemand die het wel snapt? 
Neem het leven niet te serieus, je overleeft het toch niet.


Allereerst is het natuurlijk belangrijk om te bekijken wat je precies moet berekenen en hoe je daar uit kan komen. Gegeven is dat een bal stil blijft liggen, dat betekent dat de resulterende kracht op een object in de trein nul moet zijn. Je kan voor een object in de trein (bv een bal) een krachtendiagram opstellen waarbij je alle krachten op de bal tekent. Je hoe groot de middelpuntzoekende versnelling is (als functie van de snelheid v), dan is het een kwestie van alles invullen en oplossen.quote:Op woensdag 6 april 2011 21:26 schreef rubensanti het volgende:
Ik heb morgen een natuurkunde toets en ik zit nu een beetje op internet te oefenen met een vraagstuk dat vorig jaar ook in de toets zat. Het betreft het volgende vraagstuk : http://www.natuurkunde.nl/artikelen/view.do?supportId=2062 en ik snap er geen ene moer van ook al staan de uitwerkingen eronder. Iemand die het wel snapt?
Het is misschien een beetje (te) kort uitgelegd, als het niet duidelijk is zal je iets specifieker moeten zeggen waar je het niet meer volgt
The biggest argument against democracy is a five minute discussion with the average voter.


Dat de bal stil blijft liggen komt volgens mij doordat Fn = Fz. Ik heb alleen geen flauw benul hoe ik de v kan uitrekenen. Ook met het krachtendiagram erbij heb ik gewoon te weinig gegevens, namelijk alleen dat de helling 9 graden is en dat de straal 500 meter is. Bij de uitwerkingen doen ze dit:quote:Op woensdag 6 april 2011 21:42 schreef M.rak het volgende:
[..]
Allereerst is het natuurlijk belangrijk om te bekijken wat je precies moet berekenen en hoe je daar uit kan komen. Gegeven is dat een bal stil blijft liggen, dat betekent dat de resulterende kracht op een object in de trein nul moet zijn. Je kan voor een object in de trein (bv een bal) een krachtendiagram opstellen waarbij je alle krachten op de bal tekent. Je hoe groot de middelpuntzoekende versnelling is (als functie van de snelheid v), dan is het een kwestie van alles invullen en oplossen.
Het is misschien een beetje (te) kort uitgelegd, als het niet duidelijk is zal je iets specifieker moeten zeggen waar je het niet meer volgt.
Alleen de normaalkracht hoeft te worden ontbonden in:
F nx = F n·cos en F ny = F n·sin
En dan...
F = m·a >>
F z + F n = m·a
oor de x-richting levert dit op:
0 + F n·cos = m· 2·r
Voor de y-richting levert dit op:
-m·g + F n·sin = 0
Combineren van deze twee geeft v = 28 m/s
Ik snap alleen niet wat je hier kan invullen en vooral die laatste combinatie geeft me hoofdpijn
Neem het leven niet te serieus, je overleeft het toch niet.


Bijna, je vergeet echter dat de trein onder een hoek staat, waardoor de normaalkracht zowel een x-component als een y-component heeft. De y-component moet nu gelijk zijn aan de zwaartekracht, zo is er geen resulterende kracht in de verticale richting. In de horizontale richting moet er natuurlijk wel een resulterende kracht zijn (itt wat ik in m'n eerdere post zei, dat klopte niet), namelijk de middelpuntzoekende kracht.quote:Op woensdag 6 april 2011 21:52 schreef rubensanti het volgende:
[..]
Dat de bal stil blijft liggen komt volgens mij doordat Fn = Fz.
Deze middelpuntzoekende kracht heeft als formule Fmpz=mv2/r. Je weet dat de x-component van de normaalkracht de enige kracht in de horizontale richting is, deze moet dus de middelpuntzoekende kracht 'leveren' (de Fmpz is geen kracht die bovenop de andere krachten werkt, het is een resultante van de werkende krachten).
Probeer het nu nog eens helemaal uit te schrijven van het begin (liefst zonder uitwerkingen ernaast
The biggest argument against democracy is a five minute discussion with the average voter.


Je bedoeltquote:Op woensdag 6 april 2011 22:12 schreef lyolyrc het volgende:
Hou er ook even rekening mee dat er een fout staat in de uitwerking!
SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.?The biggest argument against democracy is a five minute discussion with the average voter.


quote:Op woensdag 6 april 2011 22:14 schreef M.rak het volgende:
[..]
Je bedoeltInderdaad.SPOILEROm spoilers te kunnen lezen moet je zijn ingelogd. Je moet je daarvoor eerst gratis Registreren. Ook kun je spoilers niet lezen als je een ban hebt.?


Ik snap eigenlijk nog steeds niet hoe ik de som aan moet pakken. Zouden jullie misschien een kleine tip kunnen geven met hoe ik moet beginnen. Ik zit nu al een uur naar de hoek van 9 graden en de straal van 500 te kijken maar ik heb geen idee hoe ik dit kan omrekenen naar Fc omdat ik geen massa heb 
[ Bericht 10% gewijzigd door rubensanti op 06-04-2011 23:18:59 ]
[ Bericht 10% gewijzigd door rubensanti op 06-04-2011 23:18:59 ]
Neem het leven niet te serieus, je overleeft het toch niet.


Bedoel je met Fc de middelpuntzoekende kracht? In dat geval, je hoeft deze kracht ook niet precies uit te rekenen. Ik zal het stap voor stap proberen uit te leggenquote:Op woensdag 6 april 2011 22:28 schreef rubensanti het volgende:
Ik snap eigenlijk nog steeds niet hoe ik de som aan moet pakken. Zouden jullie misschien een kleine tip kunnen geven met hoe ik moet beginnen. Ik zit nu al een uur naar de hoek van 9 graden en de straal van 500 te kijken maar ik heb geen idee hoe ik dit kan omrekenen naar Fc omdat ik geen massa heb
• Je weet dat de krachten in de verticale richting elkaar op moeten heffen, hieruit kan je een uitdrukking vinden voor de normaalkracht.
• Je weet dat de resulterende kracht, de x-component van de normaalkracht, de gelijk is aan mv2/r.
• Met deze informatie kan je nu v uitrekenen
De massa heb je hierin niet nodig, omdat deze wegvalt als je alles opschrijft.
The biggest argument against democracy is a five minute discussion with the average voter.


Ja die heb ik een tijd geleden wel gehad, maar ik zie het verband niet.
Neem het leven niet te serieus, je overleeft het toch niet.


Alle krachten in x-richting optellen en gelijkstellen aan m*ax.quote:Op woensdag 6 april 2011 22:39 schreef rubensanti het volgende:
Ja die heb ik een tijd geleden wel gehad, maar ik zie het verband niet.
Ook alle krachten in y-richting optellen en gelijstellen aan m*ay.
Als twee krachten tegengesteld werken, een van beide negatief nemen.
Dit geeft je twee uitdrukkingen, waarbij je uiteindelijk de een kunt omwerken en substitueren in de ander. Dan valt m ook weg, zoals M.rak zegt.


Nee, ay=0 (bedenk zelf waarom), ax=v2/r (Fx=mv2/r).quote:Op woensdag 6 april 2011 22:47 schreef rubensanti het volgende:
ax=mv2/r
en
ay=mv2/r
Bedoelen jullie dit?
Probeer zelf goed te kijken of je begrijpt waarom dit geldt, dat is namelijk essentieel bij zo'n soort vragen. Als je eenmaal in de gaten hebt hoe het werkt, stelt het niet zo veel meer voor.
The biggest argument against democracy is a five minute discussion with the average voter.


Die uitdrukkingen kloppen niet, want a = v2/r.quote:Op woensdag 6 april 2011 22:47 schreef rubensanti het volgende:
ax=mv2/r
en
ay=mv2/r
Bedoelen jullie dit?
Nee, wat ik bedoel is dat je kijkt welke krachten je hebt in x-richting en welke in y-richting en die stel je gelijk aan de massa keer de versnelling in die richting.
In x-richting heb je de x-component van FN. Die stel je gelijk aan de max.
FNx = max
In y-richting heb je 2 krachten, tel die op en stel ze gelijk aan m*ay.


ay= 0 omdat de Fny en de Fz elkaar opheffen? en de enigste kracht die er is is de Fxn.
0= v2/r is dit die van y?
En wat kan ik doen met de hoek van 9 graden?
0= v2/r is dit die van y?
En wat kan ik doen met de hoek van 9 graden?
Neem het leven niet te serieus, je overleeft het toch niet.


ay is inderdaad nul omdat de Fny en de Fz elkaar opheffen, dat weet je omdat de bal stil blijft liggen (eigenlijk nogal een nutteloze toevoeging, in principe geldt dit altijd lijkt me).quote:Op woensdag 6 april 2011 23:08 schreef rubensanti het volgende:
ay= 0 omdat de Fny en de Fz elkaar opheffen? en de enigste kracht die er is is de Fxn.
0= v2/r is dit die van y?
En wat kan ik doen met de hoek van 9 graden?
0= v2/r, wat bedoel je daarmee? In de y-richting hoef je de Fmpz helemaal niet te gebruiken, die geldt alleen in de x-richting. In de y-richting geldt ay=0, in de x-richting geldt ax= v2/r.
Met de hoek kan je de normaalkracht in componenten ontbinden (x- en y-component).
The biggest argument against democracy is a five minute discussion with the average voter.


Ik ben nu gewoon een beetje dingetjes aan het proberen, en net had ik g=v2/r
geeft v= 70 , en dan dit vermenigvuldigen met sin(9) kom ik op 28,8 m/s. Kan dit kloppen?
geeft v= 70 , en dan dit vermenigvuldigen met sin(9) kom ik op 28,8 m/s. Kan dit kloppen?
Neem het leven niet te serieus, je overleeft het toch niet.


Met dingetjes proberen kom je er niet, het is wel de bedoeling dat je weet wat je doet natuurlijk. Probeer het eens stap voor stap netjes op te schrijven. In principe moet het, met de tips die gegeven zijn, nu wel lukken om de oplossing uit te schrijven.quote:Op woensdag 6 april 2011 23:19 schreef rubensanti het volgende:
Ik ben nu gewoon een beetje dingetjes aan het proberen, en net had ik g=v2/r
geeft v= 70 , en dan dit vermenigvuldigen met sin(9) kom ik op 28,8 m/s. Kan dit kloppen?
Bij een proefwerk of examen zal je de uitkomst namelijk niet gegeven krijgen, waardoor je niet naar dat antwoord toe kan werken. Voor zomaar iets proberen zal je ook geen punten krijgen, voor het netjes uitwerken van de gegevens wel.
The biggest argument against democracy is a five minute discussion with the average voter.


Ik dacht:
mg = mv2/r
g = v2/r
v = wortel( g*r)
dan krijg je wortel(9,81 * 500) = 70
en dan 70 * sin(9) om de schuine zijde van het krachtendiagram te krijgen, maar ik weet niet of dat ergens opslaat. Maar het komt wel uit op 28,8 m/s en volgens de uitwerking is het 28 m/s.
Het probleem is dat ik ondanks de tips nog steeds niet echt weet wat ik er mee kan doen ( ben niet zo'n natuurkunde baas ) en met iets proberen kan je nog altijd puntjes scoren als je het goed doet
mg = mv2/r
g = v2/r
v = wortel( g*r)
dan krijg je wortel(9,81 * 500) = 70
en dan 70 * sin(9) om de schuine zijde van het krachtendiagram te krijgen, maar ik weet niet of dat ergens opslaat. Maar het komt wel uit op 28,8 m/s en volgens de uitwerking is het 28 m/s.
Het probleem is dat ik ondanks de tips nog steeds niet echt weet wat ik er mee kan doen ( ben niet zo'n natuurkunde baas ) en met iets proberen kan je nog altijd puntjes scoren als je het goed doet
Neem het leven niet te serieus, je overleeft het toch niet.


Hoe kom je aan die eerste regel, mg = mv2/r ?quote:Op woensdag 6 april 2011 23:33 schreef rubensanti het volgende:
Ik dacht:
mg = mv2/r
g = v2/r
v = wortel( g*r)
dan krijg je wortel(9,81 * 500) = 70
en dan 70 * sin(9) om de schuine zijde van het krachtendiagram te krijgen, maar ik weet niet of dat ergens opslaat. Maar het komt wel uit op 28,8 m/s en volgens de uitwerking is het 28 m/s.
Het probleem is dat ik ondanks de tips nog steeds niet echt weet wat ik er mee kan doen ( ben niet zo'n natuurkunde baas ) en met iets proberen kan je nog altijd puntjes scoren als je het goed doet
The biggest argument against democracy is a five minute discussion with the average voter.


Waarom zouden die gelijk moeten zijn?quote:
Tip: Kijk eens goed naar het plaatje in de uitwerking, daar staan de verschillende krachten getekend.
The biggest argument against democracy is a five minute discussion with the average voter.


Ik zag in mijn natuurkunde boek een sommetje dat er een beetje op leek en daar gebruikten ze dat.
krachten in de y richting zijn Fn en Fz, en in de x richting de Fmpz. Maar wat bedoelen jullie precies met de componenten ontbinden?
krachten in de y richting zijn Fn en Fz, en in de x richting de Fmpz. Maar wat bedoelen jullie precies met de componenten ontbinden?
Neem het leven niet te serieus, je overleeft het toch niet.


Op welk niveau studeer/leer je eigenlijk, rubensanti? Zodat duidelijk is op welk niveau ik je het beste kan helpen.


Ik zit nu in 5VWO N&T. We zijn nu bezig met het hoofdstuk kromme banen, en ik snap het eigenlijk wel alleen bij deze som zie het gewoon niet.
Neem het leven niet te serieus, je overleeft het toch niet.


Tja, bij dat sommetje geldt dat misschien, die gelijkheden moet je voor iedere som opnieuw bekijkenquote:Op woensdag 6 april 2011 23:41 schreef rubensanti het volgende:
Ik zag in mijn natuurkunde boek een sommetje dat er een beetje op leek en daar gebruikten ze dat.
krachten in de y richting zijn Fn en Fz, en in de x richting de Fmpz. Maar wat bedoelen jullie precies met de componenten ontbinden?
De normaalkracht staat niet recht, maar schuin (vanwege de hoek van 9o). Deze kracht bestaat uit een component (een soort gedeelte) in de x-richting en een component in de y-richting. Het nut hiervan is dat je, in dit geval, de y-component van de normaalkracht gelijk kan stellen aan de zwaartekracht.
In dit plaatje zie je ook dat de schuine pijl als het ware wordt gevormd door een horizontaal deel en een verticaal deel.
The biggest argument against democracy is a five minute discussion with the average voter.


Toen ik op het VWO zat, deden wij dit soort sommen niet. Dit soort dingen oplossen heb ik pas op de universiteit bij werktuigbouwkunde geleerd.quote:Op woensdag 6 april 2011 23:50 schreef rubensanti het volgende:
Ik zit nu in 5VWO N&T. We zijn nu bezig met het hoofdstuk kromme banen, en ik snap het eigenlijk wel alleen bij deze som zie het gewoon niet.
Ik denk persoonlijk dat we dan te abstract bezig zijn.
Je kunt de normaalkracht ontbinden in twee componenten, eentje in x-richting en een in y-richting. Zie het plaatje van M.rak. Het is in de uitwerking ook met stippenlijntjes aangegeven.
Met goniometrische formules kun dat doen. Hier geldt: sin(α) = FNx/FN en cos(α) = FNy/FN. Dit kun je omwerken tot: FNx=FNsin(α) en FNy = FNcos(α)
Die componenten gebruik je weer om een krachtenbalans in x-richting en een krachtenbalans in y-richting op te stellen.


Ik meen dat wij dit soort sommen ook wel eens gehad hebben op de middelbare, maar daar kan ik me in vergissen. Dat we te abstract bezig zijn zou inderdaad kunnen, ik studeer zelf natuurkunde, dus daar kan ik wel eens last van hebbenquote:Op donderdag 7 april 2011 00:01 schreef lyolyrc het volgende:
[..]
Toen ik op het VWO zat, deden wij dit soort sommen niet. Dit soort dingen oplossen heb ik pas op de universiteit bij werktuigbouwkunde geleerd.
Ik denk persoonlijk dat we dan te abstract bezig zijn.
The biggest argument against democracy is a five minute discussion with the average voter.


Je zou mij totaal zijn kwijtgeraakt, als ik toen zo'n som had moeten doen. Ik kijk even of ik het nu via dm kan afhandelen.quote:Op donderdag 7 april 2011 00:20 schreef M.rak het volgende:
[..]
Ik meen dat wij dit soort sommen ook wel eens gehad hebben op de middelbare, maar daar kan ik me in vergissen. Dat we te abstract bezig zijn zou inderdaad kunnen, ik studeer zelf natuurkunde, dus daar kan ik wel eens last van hebben. Excuses in dat geval, ik hoop dat het voor rubensanti evengoed wat duidelijker is geworden.


Gelukt via dm!  Nog even de uitwerking voor de liefhebber:
Nog even de uitwerking voor de liefhebber:
Krachtenbalans voor de x-richting:
FN sin(α) = ma
Gebruikmakend van a = v2/r geeft dit:
FN sin(α) = mv2/r
Krachtenbalans voor de y-richting:
Fz + FNcos(α) = 0
Invullen van Fz = mg en toevoegen van een minteken, want FNy en Fz zijn tegengesteld gericht geeft dit:
-mg + FNcos(α) = 0
Werk de laatste formule om tot:
FN = mg/cos(α)
En substitueer dit in de formule voor de x-richting:
mgsin(α)/cos(α) = mv2/r
Dit kun je vereenvoudigen tot:
mgtan(α) = mv2/r
Streep m aan beide kanten weg en werk de formule om tot een expressie voor v:
v = √(grtan(α))
Invullen geeft v = 28 m/s.
Krachtenbalans voor de x-richting:
FN sin(α) = ma
Gebruikmakend van a = v2/r geeft dit:
FN sin(α) = mv2/r
Krachtenbalans voor de y-richting:
Fz + FNcos(α) = 0
Invullen van Fz = mg en toevoegen van een minteken, want FNy en Fz zijn tegengesteld gericht geeft dit:
-mg + FNcos(α) = 0
Werk de laatste formule om tot:
FN = mg/cos(α)
En substitueer dit in de formule voor de x-richting:
mgsin(α)/cos(α) = mv2/r
Dit kun je vereenvoudigen tot:
mgtan(α) = mv2/r
Streep m aan beide kanten weg en werk de formule om tot een expressie voor v:
v = √(grtan(α))
Invullen geeft v = 28 m/s.


nog bedankt voor de hulp van gister, ik kreeg de opgave op het proefwerk  . Verder ging de toets goed, jullie zijn echt helden!
. Verder ging de toets goed, jullie zijn echt helden!
Neem het leven niet te serieus, je overleeft het toch niet.


Altijd handig om te weten wat er mogelijk op een toets gevraagd gaat worden.quote:Op donderdag 7 april 2011 10:25 schreef rubensanti het volgende:
nog bedankt voor de hulp van gister, ik kreeg de opgave op het proefwerk. Verder ging de toets goed, jullie zijn echt helden!
Ik heb ooit een boek opgespoord op basis waarvan een docent mechanicatentamens samenstelde.
| Forum Opties | |
|---|---|
| Forumhop: | |
| Hop naar: | |